1、选择题
A.核外电子数
B.最外层电子数
C.核电荷数
D.中子数
参考答案:C
本题解析:元素由原子的质子数决定,核电荷数与质子数相等。
本题难度:简单
2、选择题 下列元素的原子半径最大的是
A.氮
B.磷
C.氧
D.硫
参考答案:B
本题解析:四者在周期表中的位置关系为:上周期? N? O?
下周期? P? S
利用:同周期,由左到右,原子半径逐渐减小,同主族,由上到下,原子半径逐渐增大,故选B
本题难度:简单
3、填空题 (16分)
A、B、C、D、E、F均为常见的短周期元素,原子序数依次增大,已知:
①? A元素中的一种原子没有中子.
②? B元素原子最外层电子数是次外层电子数的2倍.
③? C元素最高正价与最低负价的代数和为2.
④? A与D能以原子个数比1:1、2:1形成两种液态化合物.
⑤? E2+离子的电子层结构与氖原子相同.
⑥? F元素有多种化合价,且常温下F元素的单质与强碱溶液反应,可得到两种含F元素
的化合物.
⑦? C、F两种元素质子数之和是B元素质子数的4倍.
回答下列问题:
(1)A元素中没有中子的同位素的原子组成符号为?,F简单阴离子的结构示意图?,化合物AFD的电子式为?,B2A2的结构式为?.
(2)由C、F两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里C、F两种原子最外层均达到8个电子的稳定结构.X遇水蒸气可形成一种常见的漂白性物质.则X的分子式?;分子中C、F原子间的化学键的类型为?(填“极性键”或“非极性键”),属于?分子(填“极性”或“非极性”),X与水反应的化学方程式为?.
(3)B、C两种元素可形成一种硬度比金刚石还大的化合物Y.在化合物Y中,B、C两原子以单键相结合,且每个原子的最外层均达到8个电子的稳定结构.则Y的化学式为?,Y的硬度比金刚石硬度大的原因是?.
参考答案:
 (1)A:11H(1分);Cl-?(1分);?(2分);H―C≡C―H(2分)?
(1)A:11H(1分);Cl-?(1分);?(2分);H―C≡C―H(2分)?
(2)NCl3(2分);极性键(1分);极性(1分);? NCl3+3H2O=NH3+3HClO(2分)
(3)C3N4(2分)二者均为原子晶体,N的原子半径比C的原子半径小,C―N键长比
C―C键长短,C―N键能比C―C键能大,所以C3N4的硬度比金刚石硬度大.(2分)
本题解析:略
本题难度:一般
4、填空题 (6分)? A、B、C三种元素都是短周期元素。含有A元素的物质,在无色火焰上灼烧时产生黄色火焰;B2是自然界中最轻的气体, A元素与C元素位于同一周期,B2在C2中燃烧产生苍白色火焰,且可形成共价化合物。根据以上条件回答:
① 写出A、B的元素符号:A?,B?。
② 写出C元素最高价氧化物对应水化物的化学式?。
参考答案:(6分)
①? Na ,? H②? HClO4
本题解析:焰色反应为黄色的物质中必含有Na元素;B2是自然界中最轻的气体,即为H2;燃烧时产生苍白色火焰的为H2与CL2反应;
C元素为CL元素,其最高价为+7价,对应的氧化物化学式为HClO4
本题难度:简单
5、选择题 下列各组物质中互为同位素的是( )
A.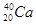 和
和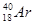
B.D和T
C.H2O和H2O2
D.O3和O2
参考答案:B
本题解析:同位素是指具有相同的质子数而不同质量数的同一元素的不同核素互成为同位素,A中质子数不同,C、D中微粒不是核素,所以正确的答案是B。
本题难度:一般