1��ʵ���� ��֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ����ʾ��ͼ�е�װ�ÿ���ʵ�ָ÷�Ӧ���ش���������
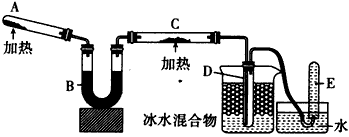
(1)A�м����������_______________��������Ӧ�Ļ�ѧ����ʽ��_______________��
(2)B����������____________����������_______________
(3)ʵ��ʱ��C�й۲쵽��������____________��������Ӧ�Ļ�ѧ����ʽ��___________________��
(4)ʵ��ʱ��D�й۲쵽��������___________��D���ռ�����������____________����������ʵķ�����
������________________��
�ο��𰸣�(1)�Ȼ�狀���ʯ�ң�2NH4Cl+Ca(OH)2 CaCl2+2NH3��+2H2O
CaCl2+2NH3��+2H2O
(2)��ʯ�ң����ﰱ��
(3)��ɫ��ĩ����Ϻ�ɫ��2NH3+3CuO N2+3Cu+3H2O
N2+3Cu+3H2O
(4)�Թ��ڳ�����ɫҺ�壻��ˮ���ú�ɫʯ����ֽ���飬��ֽ����ɫ������ˮ����ͭ��δ���飬��ĩ����ɫ
���������
�����Ѷȣ�һ��
2��ѡ���� Ϊ��֤����ˮ������ɻ�ԭ���ǽ���������ʵ�飬��ʵ���в������������˳����ȷ����(��?��)
��ȡ�������ۼ�ˮ�Ƴ�����Һ? �ڼ������
�ۼ������Ƶ�Cu(OH)2����Һ? �ܼӼ���ϡ����
���ټ���ֱ������? �����Һ���к�ֱ����Һ�ʼ���
A���٢ڢܢݢۢ�
B���٢ܢڢۢݢ�
C���٢ܢڢޢۢ�
D���٢ݢۢܢޢ�
�ο��𰸣�C
�������������ˮ���ʵ��IJ���Ϊ��ȡ���������ۼ�����ˮ�����Һ���ڵ�����Һ�м���3��5��ϡ��������Һ��м����ӡ���ȴ������ˮ��������ɻ�ԭ���������ǣ�������Cu��OH��2����Һ����������Ӧ�����ڼ��������£����ԣ�����ȴ�����Һ���ȼ���NaOH��Һ��pH�����ԣ�Ȼ���ټ�������Cu��OH��2����Һ��Һ��ˮԡ���ȣ���ʵ������ש��ɫ�������������Ը�ʵ���в��������������ȷ˳��Ϊ���٢ܢڢޢۢݣ���ѡC��
������������۽̲Ļ���֪ʶ����Ҫ�ǿ����˵���ˮ�⣬�Լ�����Cu��OH��2����Һ�Լ��������Ƿ���������Ӧ��������ע��ò�����ǰ��˳����Ŀ�ϼ�����������ѧ������˼ά�����淶�Ͻ���ʵ�����������
�����Ѷȣ���
3��ʵ���� ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ���������µ�ʵ��װ�á�

��1��ʵ������װ��A�Ʊ�SO2��ijͬѧ��ʵ��ʱ���ִ�A�ķ�Һ©��������©����Һ��δ���£�����Ϊԭ������ǣ�_______________________________��
��2��ʵ������װ��E�Ʊ�Cl2���䷴Ӧ�Ļ�ѧ��ѧ����ʽΪ��MnO2+4HCl(Ũ) MnCl2+Cl2��+2H2O������6mol��HCl�μӷ�Ӧ����ת�Ƶĵ�������Ϊ_______________________��
MnCl2+Cl2��+2H2O������6mol��HCl�μӷ�Ӧ����ת�Ƶĵ�������Ϊ_______________________��
��3���ٷ�Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ���ֵ������ǣ�
B��_________________________��D��________________________��
��ֹͣͨ����,�ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�ΪB��___________________��
D��______________________��
��4����һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶����ǿ�����ǽ��Ƶõ�SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ���������������������������������ԭ���û�ѧ����ʽ��ʾ��________________________��
�ο��𰸣���1����Һ©���IJ�����û��ȡ����
��2��3��6.02��1023
��3����Ʒ����ɫ��Ʒ����ɫ������ɫ��Ʒ���ָֻ��ɺ�ɫ������������
��4��Cl2+SO2+2H2O===2HCl+H2SO4
���������
�����Ѷȣ�һ��
4������� ��ˮ�Ȼ�����AlCl3���ǰ�ɫ���壬��178��������������ˮ�֣�װ����ˮ�Ȼ������Լ�ƿ���ó�ʪ�����У����Զ���ը���������������Ȼ�������Ϊ�л��ϳɺ�ʯ��ҵ�Ĵ�����ijѧϰС������ͼװ����ʵ�����Ʊ���ˮ�Ȼ���������һ������С��Ļ��
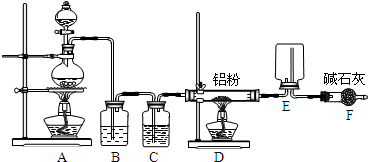
��1��д��װ��A�з�����Ӧ�����ӷ���ʽ��______��
��2��װ��B��C�е��Լ��ֱ�Ϊ��______��______��
��3��ʵ�鿪ʼʱ�ȵ�ȼ______���ƾ��ƣ�װ��E������Ϊ��______��
��4��װ��F������Ϊ��______��
�ο��𰸣���1��Ũ����Ͷ��������ڼ����������ܷ���������ԭ��Ӧ�����Ȼ��̡�������ˮ������ʽΪ��MnO2+4HCl��Ũ����.MnCl2+Cl2 ��+2H2O�����ӷ���ʽΪ��4H++2Cl-+MnO2�T����.Cl2��+2H2O+Mn2+��
�ʴ�Ϊ��4H++2Cl-+MnO2�T����.Cl2��+2H2O+Mn2+��
��2��Ũ������лӷ��ԣ����Ի�������к����Ȼ��⣬�Ȼ��⼫������ˮ�����������ڱ���ʳ��ˮ������ѡ����ʳ��ˮ��ȥ�Ȼ��⣻������Ҫ����ȡ��������ˮCuCl2������Ҫ��ȥ�����л��е�ˮ�������Ҳ������µ����ʡ�����Ҳ�����ʲ���Ӧ������ѡŨ���
�ʴ�Ϊ������ʳ��ˮ��Ũ���
��3����ͨ�������ſ�װ���еĿ�����Ȼ������������Ӧ��������178������������ʱ�������Ա��ռ�������װ��E������Ϊ�ռ��Ȼ�����
�ʴ�Ϊ��A���ռ��Ȼ�����
��4�������ж�����Ⱦ���������Բ����ſգ���ʯ�ҵijɷ��������ƺ��������ƣ������������ơ����������ܷ�Ӧ�ﵽ�����Կ��ü�ʯ�Ҵ���β������������ˮ��������ʯ�һ�������ˮ���������Կ����������
�ʴ�Ϊ�����ն������������ֹ��Ⱦ��������ֹ�����е�ˮ��������E�У�
���������
�����Ѷȣ�һ��
5��ʵ���� ��12�֣�ij�о���ѧϰС��Ϊ�ⶨ��13.7gijNa2CO3��Ʒ�Ĵ��ȣ�����ֻ��NaHCO3���ʣ���ѡ����ͼ��ʾ������װ�ý���ʵ�飨��װ��δ��ȫ�����Իش��й����⣺

��1����ѡ���ʵ�������������װ�õ���ȷ˳����_?��
��2������ʱNaHC03�ֽ�Ļ�ѧ����ʽΪ?��
��3����ɸ�ʵ����ȱ�IJ���������?�������ƣ������������װ�âܵ�?���룬��װ�âݵ�?���루��ӿ���ţ���
ʵ������ⶨ����ʵ����ɺ�ʣ����������ᷴӦ����CO2�������
��4�����Ⱥ�Ĺ������������ᷴӦ�����ӷ���ʽΪ?��
���ݷ��������ۣ�
��5���������������������ʱ������CO2����ڱ�״��ʱΪ2��24L����Na2CO3��Ʒ�Ĵ���Ϊ?��
��������
��6����ͬѧ��Ϊʵ��һ������ˮ��ʹ�����������������Ϊԭ�������?��
��7����ͬѧ������ʵ�顪��ȡCO2���ʱ������Һ���Һ����ڢ���Һ���Һ�棬��δ���κδ�������aֵ?���ƫ����ƫС������Ӱ�족����
�ο��𰸣�
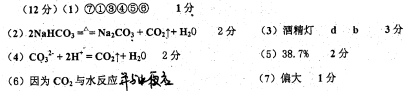
�����������
�����Ѷȣ���