1��ѡ���� Ϊ��ֹ���ִ���ĸ�ʴ��Ӧ�ڴ���ˮ������λ��Ƕ��һ�������ģ�������?
A��ͭ��
B��Ǧ��?
C���
D���ƿ�?
�ο��𰸣�̼�����ͺ�ˮ���ɵ�ԭ����У���ʧ���������������Ը����ϵ缫��ӦʽΪ��Fe-2e-=Fe2+��Ϊ��ֹ��������ʴ��������������������������������������������Ľ�����ԭ���������Ӧ��ѡȡ�������õĽ�����ԭ��ظ�����
A������ͭ������������ã���A����
B������Ǧ������������ã���B����
C������п�Ƚ��������ã���C��ȷ��
D�������ƿ��Ժ�ˮ���ҷ�����Ӧ��������ԭ��صĵ缫����D����
��ѡC��
���������
�����Ѷȣ���
2��ѡ���� ��������������н���ʱ�����Ʋ㲿�ֱ��ƻ�ʱ�������ױ���ʴ����
A.Sn
B.Zn
C.Cu
D.Ag
�ο��𰸣�B
����������Ʋ�ʹ������������������Ʋ��ܵ��ƻ�ʱ���������ý��������γ�ԭ��أ����ý��������������Ա��������ܵ���ʴ��
�����Ѷȣ�һ��
3��ѡ���� �����������ʴ�йص�˵����ȷ���ǣ�������
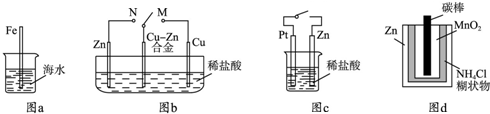
A��ͼa�У����뺣ˮ�е�������Խ�����˸�ʴԽ����
B��ͼb�У�������M������Nʱ��Cu-Zn�Ͻ�ĸ�ʴ���ʼ�С
C��ͼc�У���ͨ����ʱZn��ʴ��������Zn�Ϸų����������Ҳ����
D��ͼd�У�Zn-MnO2�ɵ���Էŵ縯ʴ��Ҫ����MnO2���������������
�ο��𰸣�A��ͼa�У�����������ѧ��ʴ�������˵IJ����������Ӵ��٣���ʴ�̶Ƚ��ᣬ��A����
Bͼb�п�����M����N��Cu-Zn����������ʴ���ʼ�С����B��ȷ��
C��ͼc�н�ͨ����ʱZn����������ʴ��������������Pt�Ϸų�����C����
D��ͼd�иɵ�طŵ�ʱMnO2������ԭ��Ӧ������п�Ļ�ԭ�ԣ���D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ��15�֣�
��6�֣�����������ɶ�����̼��ˮ�ϳ������ǣ�ͬʱ�ų����������뽫�÷�Ӧ������������Ƴ�һ��ԭ��أ����������������ͽ�̫����ת����˵��ܡ�
��1��д����ԭ��ص��ܷ�Ӧʽ��______________________________________
��2��д���õ�������Խ����зŵ�ĵ缫��Ӧʽ��
������_____________________________________________
������_____________________________________________
��6�֣����˼ά��ѧϰ��ѧ����Ҫ������������Ƿ���ȷ���뾭�ܼ��顣�ڽ������˼ά��ʱ���ܻ�е��ȣ�һ��Ҫע��һЩ���ʵ������ԣ��Է�ֹ��ȳ�����Ľ��ۡ�ƾ���еĻ�ѧ֪ʶ��������Ƚ����ȷ���ǣ��������ţ�?�������������д����ȷ�ġ�
������ͬ�����£�Na2CO3�ܽ�ȱ�NaHCO3��
��ȣ�����ͬ�����£�CaCO3�ܽ�ȱ�Ca��HCO3��2��
��ȷ��Ӧ��Ϊ���������ȷ���˴���д����ͬ������?��
������������Һ��ͨ����CO2��CO2 + ClO- + H2O = HCO3- + HClO
��ȣ������������Һ��ͨ����SO2��SO2 + ClO- +H2O = HSO3- + HClO
��ȷ��Ӧ��Ϊ��?��
�۸��ݻ��ϼ�Fe3O4�ɱ�ʾΪ��FeO��Fe2O3?��ȣ�Fe3I8Ҳ�ɱ�ʾΪFeI2��2FeI3
��ȷ��Ӧ��Ϊ��?��
��CaC2��ˮ�⣺CaC2+2H2O =Ca��OH��2 + C2H2��
��ȣ�Al4C3Ҳ��ˮ�⣺Al4C3 + 12H2O = 4Al��OH��3��+ 3CH4��
��ȷ��Ӧ��Ϊ��?��
�����֣������£�ijˮ��ҺM�д��ڵ������У�Na+ ��A-��H+��OH-��������ҺM�� pH=3��HA��Һ
��A-��H+��OH-��������ҺM�� pH=3��HA��Һ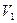 mL��pH=11��NaOH��Һ
mL��pH=11��NaOH��Һ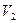 mL��Ϸ�Ӧ���ã�������˵������ȷ����?������ĸ����
mL��Ϸ�Ӧ���ã�������˵������ȷ����?������ĸ����
A������ҺM�����ԣ�����ҺM��C��H+��+C��OH-��=2��10-7mol��L-1
B����V1=V2������ҺM��pHһ������7
C������ҺM�����ԣ���V1һ������V2
D������ҺM�ʼ��ԣ���V1һ��С��V2
�ο��𰸣���15�֣�
��6�֣�
��1��C6H12O6��6O2 6CO2��6H2O�����֣�
6CO2��6H2O�����֣�
��2��C6H12O6��6H2O��24e��= 6CO2��24H�������֣� 6O2��24e����24H��= 12H2O�����֣�
��6�֣��ܣ�1�֣�
������ͬ�����£�CaCO3�ܽ�ȱ�Ca��HCO3��2С��1�֣�
�� ClO-?+ SO2 + H2O ==SO42- + Cl-?+ 2 H+��2�֣���3FeI2��I2��2�֣�
�����֣�AD
�����������
�����Ѷȣ�һ��
5��ѡ���� �����ڳ�ʪ�Ŀ����лᷢ��������ʴ������˵���У���ȷ����
A�����������ķ�ӦΪ��Fe��2e����Fe2��
B�����������ķ�ӦΪ��O2��4e��+4H+��2H2O
C����ʴ�����У����Ӵ���������
D��������ˮ�²��ֱ��ڿ�����ˮ���紦��������������ʴ
�ο��𰸣�A
���������
��ȷ�𰸣�A
A����ȷ��������ԭ����
B������ȷ�����������ķ�ӦΪ��O2��4e��+2H2O��4OH�D ;
C������ȷ����ʴ�����У����ӴӸ�����������
D������ȷ�������ڿ�����ˮ���紦��������������ʴ�������ϸ�ʴ�����������
�����Ѷȣ���