1、选择题 下列叙述与电化学腐蚀无关的是( )
A.切过咸菜的菜刀不及时清洗易生锈
B.线路连接时,有经验的电工从不把铝导线和铜导线接在一起
C.银质奖章久置后表面逐渐变暗
D.在轮船的尾部和船壳的水线以下,常装有一定数量的锌块
参考答案:A、铁和碳在盐溶液中形成原电池反应,铁做负极失电子生成亚铁离子,正极上氧气得到电子生成氢氧根离子,氢氧根离子和亚铁离子生成氢氧化亚铁被氧化为氢氧化铁,最后分解生成氧化铁铁锈,原电池反应加快反应速率,能够促进菜刀生锈,属于电化腐蚀,故A不符合;
B、铝和铜遇到电解质溶液会形成原电池反应,铝做负极被腐蚀,是原电池原理的应用,属于电化腐蚀,故B不符合;
C、银质奖章久置后表面逐渐变暗是阴和空气中的氧气反应生成氧化银的原因,和电化腐蚀无关,故符合;
D、锌和铁在海水电解质溶液中形成原电池反应,锌做负极,轮船中铁被保护,属于电化腐蚀,故D不符合;
故选C.
本题解析:
本题难度:一般
2、填空题 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁
年产量的1/4。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式。
正极:?;负极:?。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,其中焊接在铁闸门的固体材料R可以采用?。(请写出具体金属名称)
(3)下图中乙方案也可降低铁闸门腐蚀速率,其中铁闸门应该连接在直流电源
的?极。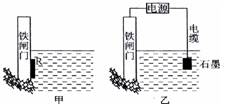
参考答案:(1)正极:O2+2H2O+4e-=4OH―;负极:Fe-2e-=Fe2+。(2) 锌 (3)负
本题解析:略
本题难度:简单
3、填空题 (12分) 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。
(1)肼―空气燃料电池是一种碱性燃料电池,电解质溶液是20%―30%的KOH溶液。该电池放电时,通入肼的一极为?极,该极的电极反应式是?,电池工作一段时间后,电解质溶液的pH将?(填“增大”、“减小”、“不变”)。
(2)肼用亚硝酸氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977。写出肼与亚硝酸反应的化学方程式?。
(3)肼和四氧化二氮作火箭推进剂,两者反应产物是氮气和水。当反应生成28.0kg还原产物时,计算参加反应的肼的质量 (写出计算过程) 。
参考答案:(12分)
(1)负极? N2H4 + 4OH--4e-= N2↑ + 4H2O?减小?(每空2分)
(2)N2H4 + HNO2 = HN3 + 2H2O?(2分)
(3)根据2N2H4+N2O4=3N2+4H2O找出参加反应的N2H4与还原产物N2之间的关系式为
2N2H4?~ N2
64? 28
m(N2H4)?28kg
m(N2H4)="64×28kg/28=64kg?" (找出关系式2分,结果正确2分)
本题解析:略
本题难度:一般
4、选择题 下列事实不能用电化学原理解释的是
[? ]
A.铝片不需要特殊的保护方法
B.炒过菜的铁锅未清洗易生锈
C.轮船水线下的船壳上镶有一定数量的锌
D.镀锌铁比镀锡铁耐腐蚀
参考答案:A
本题解析:
本题难度:简单
5、选择题 如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,则下列叙述中正确的是
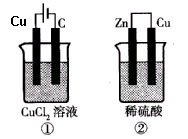
A.产生气体的体积:①>②
B.溶液的pH变化:①不变②增大
C.①和②中铜电极均失电子
D.电极反应式:①中阳极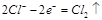 ②中负极
②中负极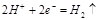
参考答案:B
本题解析:根据装置可判断,①是电解池,②是原电池。①中铜和电源的正极相连,作阳极失去电子。碳棒是阴极,溶液中的铜离子得到电子而析出。②中锌是负极,失去电子。铜是正极,溶液中的氢离子得到电子,生成氢气。所以A、C、D都是不正确的,选项B正确,答案选B。
本题难度:一般