1、简答题 如图是周期表的一部分,已知A、B、C、D都是短周期元素,四种元素原子核外共有56个电子,推断A、B、C、D各是什么元素,写出他们的元素符号:A______,B______,C______,D______.
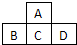
参考答案:A、B、C、D都是短周期元素,根据四种元素在周期表中的位置知,A位于第二周期,B、C、D位于第三周期,四种元素原子核外共有56个电子,即四种元素的原子序数为56,设C的原子序数为x,则B的原子序数是x-1,D的原子序数为x+1,A和C位于同一主族,A和C的原子序数相差8,则A的原子序数是x-8,四种元素的原子序数为56,所以得x-1+x+x+1+x-8=56,x=16,则C是S元素,B是P元素,D是Cl元素,A是O元素,
故答案为:O;P;S;Cl.
本题解析:
本题难度:一般
2、推断题 A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同主族元素。又知B、D两元素的原子核中质子数之和是A、C两元素的原子核中质子数之和的2倍。这四种元素的单质中常温下有两种是气体,其中一种气体易燃烧,另外两种为固体,其中一种是黄色晶体,质脆,易研成粉末。
(1)写出元素符号:A_______B_______C_______D_______。
(2)写出两种均含A、B、C、D四种元素的化合物相互反应放出气体的化学方程式:_________________________________。
(3)用电子式表示化合物C2D形成过程_________________________________。
(4)用A和B两元素的单质可以制成燃料电池,电池中装有浓KOH溶液。用多孔的惰性电极浸入浓KOH溶液中,两极均有特制的防止气体透过隔膜,在一极通入A的单质,另一极通入B的单质。写出通入B单质的一极电极反应式是:____________________________。
参考答案:(1)H;O;Na;S
(2)NaHSO4+NaHSO3==Na2SO4+SO2↑+H2O
(3)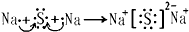
(4)O2+4e-+2H2O==4OH-
本题解析:
本题难度:一般
3、选择题 下列大小关系正确的是
A.熔点:NaI>NaBr
B.硬度:MgO>CaO
C.晶格能:NaClD.熔沸点:CO2>NaCl
参考答案:B
本题解析:选项ABC都是离子晶体,形成离子晶体的离子键越强,熔沸点的越高,硬度越大。形成离子键的离子半径越小,电荷数越多,离子键越强,所以选项AC不正确,B正确。D中CO2是分子晶体,熔沸点低于离子晶体氯化钠的,答案选B。
本题难度:困难
4、选择题 在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况,下列反应中属于这种情况的是
①过量的Zn与18 mo1/L硫酸溶液反应;
②过量的氢气与少量的氮气在催化剂存在一定条件下充分反应;
③过量的水与一定量氯气;
④过量的铜与浓硫酸;
⑤过量的铜与稀硝酸;
⑥过量的稀硫酸与块状石灰石;
⑦常温下过量浓硫酸与铝
A.②③⑤
B.②③④⑥⑦
C.①④⑤
D.①②③④⑤
参考答案:B
本题解析:①开始时是浓硫酸,发生反应:Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O。随着反应的进行,硫酸变稀,发生反应:Zn+H2SO4(稀)=ZnSO4+H2↑。硫酸溶液会完全反应; 错误。②N2+3H2 2NH3.由于该反应为可逆反应,所以无论二者以何种比例混合,反应都不可能完全进行。正确。③Cl2+H2O
2NH3.由于该反应为可逆反应,所以无论二者以何种比例混合,反应都不可能完全进行。正确。③Cl2+H2O HCl+HClO由于该反应为可逆反应,所以反应都不可能完全进行。正确。④Cu+2H2SO4(浓)
HCl+HClO由于该反应为可逆反应,所以反应都不可能完全进行。正确。④Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O随着反应的进行,硫酸变为稀硫酸,这时反应就不再进行。正确。⑤过量的铜与稀硝酸3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O直至硝酸反应完全。错误。⑥H2SO4+CaCO3= CaSO4+H2O+CO2↑。由于发生反应产生的CaSO4微溶解于水,覆盖在CaCO3的表面,使反应不能继续发生。正确。⑦常温下过量浓硫酸与铝接触。由于浓硫酸有强氧化性,在Al的表面产生一薄层致密的氧化物薄膜,对内层的金属起到了保护作用,而阻止了反应的继续进行。正确。因此符合题意的选项②③④⑥⑦。答案为B。
CuSO4+SO2↑+2H2O随着反应的进行,硫酸变为稀硫酸,这时反应就不再进行。正确。⑤过量的铜与稀硝酸3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O直至硝酸反应完全。错误。⑥H2SO4+CaCO3= CaSO4+H2O+CO2↑。由于发生反应产生的CaSO4微溶解于水,覆盖在CaCO3的表面,使反应不能继续发生。正确。⑦常温下过量浓硫酸与铝接触。由于浓硫酸有强氧化性,在Al的表面产生一薄层致密的氧化物薄膜,对内层的金属起到了保护作用,而阻止了反应的继续进行。正确。因此符合题意的选项②③④⑥⑦。答案为B。
本题难度:一般
5、选择题 下列各组物质中,互为同位素的是( )
A.红磷与白磷
B.正丁烷与异丁烷
C.11H与21H
D.金刚石与C60
参考答案:C
本题解析:
本题难度:简单