1、选择题 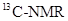 ?(核磁共振)可用于含碳化合物的结构分析
?(核磁共振)可用于含碳化合物的结构分析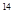 N―NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关。
N―NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关。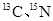 叙述正确的是
叙述正确的是
A.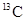 与砖
与砖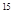 N具有相同的中子数
N具有相同的中子数
B. C与
C与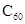 是同一种物质
是同一种物质
C.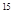 N与
N与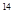 N互为同位素
N互为同位素
D.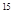 N的核外电子数与中子数相同
N的核外电子数与中子数相同
2、选择题 下列物质有固定熔、沸点的是
A.普通玻璃
B.漂白粉
C.消石灰
D.水玻璃
3、填空题 (6分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物。请回答:
(1)C和E两种元素相比较,原子得电子能力较强的是(填元素名称)?,以下三种说法中,可以验证该结论的是(填写编号)?;
A.比较这两种元素的常见单质的沸点
B.二者形成的化合物中,C元素的原子显负价
C.比较这两种元素的气态氢化物的稳定性
(2)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为?。
(3)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2LO2,消耗该化合物的质量为___________。
4、选择题 元素周期表中16号元素和4号元素原子的下列数据相比较,前者一定是后者4倍的是( )
A.中子数
B.最外层电子数
C.电子层数
D.次外层电子数
5、选择题 下列事实不能说明非金属性Cl>I的是(?)
A.Cl2+2I-==2Cl-+I2
B.稳定性:HCl>HI
C.酸性 HClO4>HIO4
D.酸性 HClO3>HIO3