1、填空题 硼的化学丰富多彩,也是材料化学研究的热点之一。
⑴ 最近美国Rice University的教授Boris Yakobson与其同事预测
了一种硼巴基球(Bn,如图所示)的存在,这种分子组成与C60相似,
但在它每个六边形的中心有一个额外的原子,显著提高了其稳定性。
则n="_______"
⑵ 硼是制造超硬材料的元素之一。提高材料的硬度有两种方法,一是制造具有类似金刚石结构的物质,如立方BM,若M为第三周期的元素,则 M为_______(填元素符号),二是寻找“不可压缩性的”的金属,这类金属具有高密度,低硬度的特点,它们和硼的化合物有异乎寻常的硬度,最近《Science》杂志报道合成了一种可与金刚石相媲美的超硬材料XB2,X是第VIIB族元素,则X为______(填元素名称)
⑶ 氮化硼纳米管是一种具有优异性能的材料,于1995年美国加州大学的教授首次合成。该材料可由高温热解法制得,用N2将由(NH4)2SO4与NaBH4反应生成的物质A带入含Co、Ni催化剂的硅晶基片上,加热到1000-1100℃反应生成,已知A为苯的等电子体,写出两步反应的方程式
参考答案:⑴80?(2分)
⑵P? , 铼?(2分,各1分)
⑶3(NH4)2SO4+ 6 NaBH4 ="=" 2B3N3H6 + 3Na2SO4 + 18 H2?
B3N3H6 ="=" 3BN + 3H2?(2分,各1分)
本题解析:⑴ C60是个32面体,其中有12个正五边形,20个正六边形。根据题意,硼巴基球与C60相似,但是在每个正六边形中存在一个B原子,所以铼共有80个 B原子,化学式为B80,即n=80。
⑵ M应为第三周期第ⅤA元素,根据等电子原理,M应为磷元素。X是ⅦB元素,该族元共有Mn、Tc、Re、Sg四种元素,其中Sg有放射性,不考虑。根据题意,该材料具有“高密度,低硬度”,根据同族元素性质递变规律,可以断定该金属元素是铼。
⑶ A是苯的等电子体,结合题意,可以推断出A为B3N3H6,该产物既不是氧化产物,也不是还原产物;根据NaBH4具有较强还原性的特点,产物中还有H2生成,它既是氧化产物,也是还原产物;另一种产物为Na2SO4。利用氧化还原反应配平方法,配平该化学反应方程式,如下:
3(NH4)2SO4+ 6 NaBH4 ="=" 2B3N3H6 + 3Na2SO4 + 18 H2
A分解形成BN,利用原子守恒关系,可以判断出产物中一定还有H2,然后配平化学反应方程式。
本题难度:一般
2、选择题 将1.92 g铜粉与一定量浓硝酸反应,当铜粉完全反应时收集到气体1.12 L(标准状况)。则所消耗硝酸的物质的量是(?)
A.0.12 mol
B.0.11 mol
C.0.09 mol
D.0.08 mol
参考答案:B
本题解析:1.92 g铜,即0.03 mol铜,与硝酸完全反应,失去电子的物质的量为2×0.03 mol,若HNO3的还原产物仅为NO2,根据电子得失相等,n(NO2)=2×0.03 mol,
V(NO2)=2×0.03 mol×22.4 L・mol-1="1.344" L>1.12 L
说明:HNO3的还原产物不仅为NO2,还有NO,因为随着反应的进行,硝酸的浓度不断降低,必然发生如下两个反应:
Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑+4H2O
消耗的硝酸的物质的量为:
n(HNO3)=2n〔Cu(NO3)2〕+n(NO2)+n(NO)=2×0.03 mol+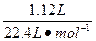 ="0.11" mol。
="0.11" mol。
本题难度:简单
3、填空题 磷单质及其化合物有广泛应用。
(1)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s) +21SiO2(s)+30C(s) ==3P4(g)+20CaSiO3(s)+30CO(g) +SiF4(g) △H
①上述反应中,副产物矿渣可用来__________________
②已知相同条件下:
4Ca5(PO4)3F(s) +3SiO2(s)=6Ca3(PO4)2(s) +2CaSiO3(s) +SiF4(g) △H
2Ca3(PO4)2(s)+10C(s) =P4(g) +6CaO(s) +l0CO(g) △H2
SiO2(s) +CaO(s)=CaSiO3(s) △H3
用△H1、△H2和△H3表示△H,△H=________________。
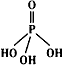
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式见下图)之间脱去两个水分子的产物,其结构式为
______________,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为___________
(3)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为_____________。
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)Ni2++_____H2PO2-+________→______Ni+____H2PO3-+_______
(b)6H2PO2-+2H+=2P+4H2PO3-+3H2↑
写出并配平反应式(a)。
③利用②中反应可在塑料镀件表面沉积镍-磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。方法上的不同点:___________________________;原理上的相同点:__________________________;化学镀的优点:_____________________________
参考答案:(1)①生产水泥等建筑材料;②△H1+3△H2+18△H3
(2)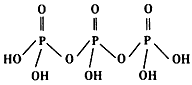 ;Na5P3O10
;Na5P3O10
(3)①+1;②Ni2++H2PO2-+H2O==Ni+H2PO3- +2H+;③化学镀无需通电,而电镀必须通电;都利用氧化还原反应;化学镀对镀件的导电性无特殊要求
本题解析:
本题难度:困难
4、填空题 氮可以形成多种离子,如N3-、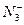 、
、 、
、 、
、 、
、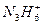 等,已知
等,已知 与
与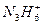 是由中性分子结合质子形成的,有类似于
是由中性分子结合质子形成的,有类似于 的性质,另外氮与氢也能形成NH3、N2H4、N3H5、N4H6、N5H7……
的性质,另外氮与氢也能形成NH3、N2H4、N3H5、N4H6、N5H7……
(1)一个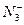 含有__________________________个电子,
含有__________________________个电子, 的电子式为____________。
的电子式为____________。
(2)形成 的中性分子的结构式是_____________________。
的中性分子的结构式是_____________________。
(3)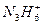 在强碱溶液中反应的离子方程式:_____________________________。
在强碱溶液中反应的离子方程式:_____________________________。
(4)NH3、N2H4、N3H5、N4H6、N5H7是否互为同系物,为什么?__________________________。
(5)写出N5H7可能的结构简式______________________________。
(6)这一系列化合物中N的质量分数最大值应小于____________%。
参考答案:(1)22? (各1分)
(各1分)
(2)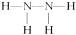 (2分)
(2分)
(3)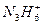 +OH-====N3H5+H2O(2分)
+OH-====N3H5+H2O(2分)
(4)互为同系物,因为它们的结构相似,组成上相差一个或若干个“NH”原子团(2分)
(5)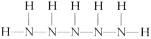 (2分)
(2分)
(6)93.3(2分)
本题解析:解答本题需要根据题目的条件对所学知识进行正向迁移,如果不能正确联系铵盐和同系物的知识,则必然会得出错误结论。因 与
与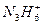 是由中性分子结合质子形成的,有类似于
是由中性分子结合质子形成的,有类似于 的性质,所以可以通过氨气和铵离子进行迁移分析
的性质,所以可以通过氨气和铵离子进行迁移分析 与
与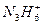 的性质。
的性质。
本题难度:简单
5、实验题 一无色气体,可能由CO2、HCl、NH3、NO2、NO、H2中的一种或几种组成。将此无色气体通过盛有浓H2SO4的洗气瓶,发现气体体积减少。继续通过装有固体Na2O2的干燥管,发现从出气管出来的气体颜色显红棕色,再将该气体全部通入盛满水倒立于水槽中的试管内,发现最后试管里仍然为一满试管液体。由此可推知:①原气体中一定含有_____________,一定不会有?____________;②最终结果可知原气体中____?__与____?___气体的体积比为____?___。
参考答案:①CO2 ?NH3?NO? ;?HCl? NO2? H2?(4分)
②NO ;? CO2 ;? 2:3?(3分)
本题解析:略
本题难度:简单