1、选择题 下列物质敞放在空气中,会因非氧化还原反应而变质的是( )
A.水玻璃
B.过氧化钠
C.亚硫酸溶液
D.硫酸亚铁溶 液
参考答案:A
本题解析:
本题难度:一般
2、选择题 已知:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;Cl2+2FeCl2═2FeCl3;2KI+2FeCl3═2KCl+I2+2FeCl2.则下列判断正确的是( )
A.氧化性:MnO>Cl2>I2>Fe3+
B.还原性:Fe2+>I->Cl-
C.Fe3+只有氧化性,Fe2+只有还原性
D.FeCl3能使湿润的淀粉碘化钾试纸变蓝
参考答案:已知:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,则氧化性KMnO4>Cl2,还原性HCl>Cl2,
在反应Cl2+2FeCl2═2FeCl3中,氧化性Cl2>Fe3+,还原性Fe2+>Fe3+,
反应2KI+2FeCl3═2KCl+I2+2FeCl2中,氧化性Fe3+>I2,还原性I->Fe2+,
则氧化性KMnO4>Cl2>Fe3+>I2,还原性I->Fe2+>Cl-,故A、B错误;
Fe3+只有氧化性,Fe2+化合价位于中间价态,既具有氧化性、又具有还原性,故C错误;
因氧化性Fe3+>I2,则FeCl3能使湿润的淀粉碘化钾试纸变蓝,故D正确.
故选:D.
本题解析:
本题难度:简单
3、选择题 宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2=2Ag2S+2H2O,其中H2S是( )
A.氧化剂
B.还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂又不是还原剂
参考答案:反应中Ag和O元素化合价发生变化,而S、H元素化合价在反应前后不变,H2S既不是氧化剂又不是还原剂.
故选D.
本题解析:
本题难度:一般
4、选择题 能正确表示四种基本类型反应与氧化还原反应关系的示意图是( )
A.
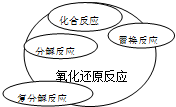
B.
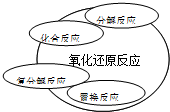
C.
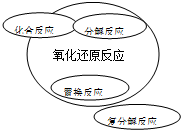
D.
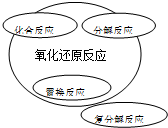
参考答案:D
本题解析:
本题难度:一般
5、简答题 将1.4g纯铁粉放入80ml?1mol/L的稀HNO3?中,反应停止后,生成的硝酸盐的成分是______其物质的量是______被还原的硝酸的质量是______.
参考答案:根据方程式:Fe+4HNO3 ═Fe(NO3)3+2H2O+NO↑,
? 0.025?0.08mol? 0.02mol
可知铁粉剩余0.025mol-0.02mol=0.005mol,生成0.02molFe(NO3)3?
再根据:Fe+2Fe(NO3)3 ═3Fe(NO3)2
? 0.005mol?0.02mol?0.015mol
可知:Fe(NO3)3?过量还剩?0.02mol-0.01mol=0.01mol,生成0.015mol硝酸亚铁.
所以生成的硝酸盐的成分为Fe(NO3)3?和?Fe(NO3)2,物质的量分别是0.01?mol、0.015?mol;?
根据Fe+4HNO3═Fe(NO3)3+2H2O+NO↑,可知被还原的硝酸是参加反应的硝酸的14,所以被还原的硝酸的物质的量为?0.08mol×14=0.02mol,其质量为?0.02mol×63g/mol=1.26g.
故答案为:Fe(NO3)3?和?Fe(NO3)2 ;0.01mol;0.015mol;1.26g.
本题解析:
本题难度:一般