1��ѡ���� ijMCFC��ȼ�ϵ�ؿ�ͬʱ��Ӧ���ˮ�������乤���¶�Ϊ600�桫700�棬����ȼ��Ϊ�����������Ϊ���ڵ�K2CO3���õ�ص��ܷ�ӦΪ��2H2+O2=2H2O�������缫��ӦʽΪ�� H2+CO32����2e�� H2O+CO2���������ж�����ȷ���� (? )?
H2O+CO2���������ж�����ȷ���� (? )?
A���ŵ�ʱCO32�����ƶ�
B���ŵ�ʱCO32���������ƶ�
C��������Ӧ�� 4OH����4e��=2H2O+O2��
D�������������1 molˮʱ��ת��4 mol����
�ο��𰸣�A
�����������������֪����ȼ�ϵ��ȼ��Ϊ�����������Ϊ���ڵ�K2CO3���ܷ�ӦΪ2H2+O2=2H2O��������ӦΪH2+CO32����2e�� H2O+CO2��������Ӧʽ��O2+2CO2+4e-
H2O+CO2��������Ӧʽ��O2+2CO2+4e- 2CO32-��A���ŵ�ʱCO32�����ƶ�����ȷ��B���ŵ�ʱCO32��Ӧ���ƶ�������C��������ӦʽΪ��O2+2CO2+4e-
2CO32-��A���ŵ�ʱCO32�����ƶ�����ȷ��B���ŵ�ʱCO32��Ӧ���ƶ�������C��������ӦʽΪ��O2+2CO2+4e- 2CO32-������D�������������1 molˮʱ��ת��2 mol���ӣ�����
2CO32-������D�������������1 molˮʱ��ת��2 mol���ӣ�����
�����Ѷȣ�һ��
2������� ��16�֣���1��ij����С��ͬѧ����ͼװ�ý���ʵ��
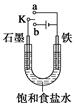
�Իش��������⣺
������ʼʱ����K��a���ӣ����������绯ѧ��ʴ�е� ��ʴ��
������ʼʱ����K��b���ӣ����ܷ�Ӧ�����ӷ���ʽΪ ��
��2��â����ѧʽΪNa2SO4��10H2O����ɫ���壬������ˮ����һ�ֲַ��ܹ㷺�������ο����С��ͬѧ���룬���ģ�ҵ�����ӽ���Ĥ�����ռ�ķ�����������ͼ��ʾװ�õ����������Һ����ȡ������������������������ƣ����۴ӽ�ʡ��Դ���Ǵ����ԭ�ϵ������ʶ��Զ����ӷ�����ɫ��ѧ���
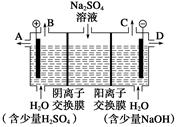
�ٸõ��۵�������ӦʽΪ ����ʱͨ�������ӽ���Ĥ�������� (����ڡ�����С�ڡ����ڡ�)ͨ�������ӽ���Ĥ����������
���Ƶõ�����������Һ�ӳ���(�A������B������C����D��) ������
��ͨ�翪ʼ������������ҺpH�����������ԭ�� ��
�������Ƶõ�����������������������Һ���Ϊ����ȼ�ϵ�أ����ظ����ĵ缫��ӦʽΪ ����֪H2��ȼ����Ϊ285.8 kJ��mol��1�����ȼ�ϵ�ع�������36 g H2Oʱ���������� kJ������ת��Ϊ���ܡ�
�ο��𰸣���16�֣�ÿ��2��(1)������ ��2Cl����2H2O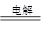 2OH����H2����Cl2��
2OH����H2����Cl2��
(2)��4OH����4e��===2H2O��O2�� С�� ��D ��H���ŵ�ٽ�ˮ�ĵ��룬ʹOH��Ũ������
��H2��2e����2OH��==2H2O 571.6
�����������1�����������K��a���ӣ���ԭ��ء�NaCl��ҺΪ���ԣ���˷���������ʴ�������������õ��ӷ�����ԭ��Ӧ��
�����K��b���ӣ��ɵ��ء������Դ�ĸ���������Fe����������Һ�е������ӷŵ硣ʯī����������Һ�е������ӷŵ磬��˵��������ӷ�ӦΪ2Cl����2H2O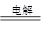 2OH����H2����Cl2����
2OH����H2����Cl2����
��2���ٵ��ʱ��������ʧ���ӷ���������Ӧ����Һ�е����������ӵķŵ�����������������ӵķŵ���������������������������ʧ���ӱ���������ˮ���������缫��ӦʽΪ4OH--4e-��2H2O+O2�����������������������ƶ����������������ƶ����������������������ƶ����������������ƶ�������ͨ����ͬ����ʱ��ͨ�������ӽ���Ĥ��������С��ͨ�������ӽ���Ĥ����������
�������������������ɣ�������D�ڵ�����
�۵��ʱ�����������ӷŵ�����������������������ˮ�ĵ��룬���Դٽ�ˮ�ĵ��룬������Һ�����������ӵ�Ũ�ȴ��������ӵ�Ũ�ȣ���Һ��pHֵ����
��ȼ��ԭ����У�ȼ���ڸ�����ʧ���ӷ���������Ӧ���������������ϵõ��ӷ�����ԭ��Ӧ����ȼ��ԭ����У��������������������ǻ�ԭ��������������Ϊ����ʣ���Һ�Լ��ԣ����缫��ӦʽΪH2��2e����2OH��==2H2O��36gˮ�����ʵ�����36g��18g/mol��2mol������2mol����������H2��ȼ����Ϊ285.8 kJ��mol��1������������285.8 kJ��mol��2��571.6kJ������ת��Ϊ���ܡ�
���㣺����ԭ��غ͵���ԭ��
�����Ѷȣ�����
3������� ������ͼ���ش��������⣺
��1�����պ�S1��װ������______��п����______��
��2�����պ�S2��װ������______��п���ϵķ�ӦΪ______��
��3�����պ�S3��װ������______���ܷ�ӦΪ______��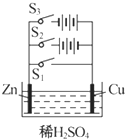
�ο��𰸣���1�����պ�S1������ԭ��صĹ����������л����Բ�ͬ�������缫п��ͭ���е������Һ���ᣬ�γ��˱պϻ�·�����л��ý���пΪ�������ʴ�Ϊ��ԭ��أ�������
��2�����պ�S2�����װ���Ǻ�����ӵ�Դ��װ�ã����ڵ��أ�����п���ý���������������ʧ���ӣ��缫��ӦΪ��Zn-2e-�TZn2+���ʴ�Ϊ�����أ�Zn-2e-�TZn2+��
��3�����պ�S3�����װ���Ǻ�����ӵ�Դ��װ�ã����ڵ��أ�����п������������ͭΪ�����������ܷ�ӦΪCu+H2SO4 ?ͨ��?.?CuSO4+H2�����ʴ�Ϊ��Cu+H2SO4 ?ͨ��?.?CuSO4+H2����
���������
�����Ѷȣ���
4��ѡ���� ���Ӽ��������õ�Ŧ��ʽ���Ϊ��п��أ���缫�ֱ�ΪAg2O��Zn���������ҺΪKOH��Һ���缫��ӦΪZn��2OH-��2e-=Zn(OH)2��Ag2O��H2O��2e-=2Ag��2OH-�����������У�����ȷ����
[? ]
A�����������������Ag2O
B��Zn����������������Ӧ��Ag2O�Ǹ���������ԭ��Ӧ
C��Zn�Ǹ���������������Ӧ��Ag2O��������������ԭ��Ӧ
D������ʱ������������Һ��pH��С������������Һ��pH����
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5��ѡ���� ����ȼ�ϵ�ؿ���ʹ���ں���ɻ��ϣ��䷴Ӧԭ��ʾ��ͼ����ͼ�������й�����ȼ�ϵ�ص�˵����ȷ����
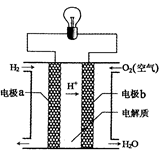
A���õ�ص��ܷ�Ӧ��2H2+O2=2H2O
B���õ���е缫b�Ǹ���
C�����·�е����ɵ缫bͨ����������缫a
D���õ�ع���ʱ����ת��Ϊ��ѧ��