| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ��������ԭ���ԭ������Ƶ����ǿ����ϰ��2019�����°棩(��)
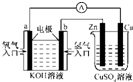 �ο��𰸣�A���ұ�װ���ǵ��أ�ͭ�缫����ԭ��ص�����������ͭ�缫�ǵ��ص���������A��ȷ�� ��������� �����Ѷȣ��� 2��ѡ���� ���б�װ���е������е���ͨ������ �ο��𰸣�B ���������A���缫����Zn�������γɵ���������B��Zn������ͭ��Һ�����û���Ӧ�����DZպϻ�·�����Կ����γ�ԭ��أ��е���ͨ������ȷ��C���ƾ��Ƿǵ������Һ�����ܵ��磬����û�е���ͨ��������D��δ�γɱպϻ�·�������γ�ԭ��أ�û�е���ͨ��������ѡB�� �����Ѷȣ�һ�� 3��ѡ���� ���ձ���ʢ�к�ˮ�����γ�ԭ�������Ϊ��������?��?�� �ο��𰸣�C ���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ��A��ֻ��1���缫�����ܹ���ԭ��أ�B�����Ľ�����ǿ��Sn�ģ����Ǹ�����C��п�Ľ�����ǿ�����ģ�����������D�����Ľ�����ǿ��ͭ�ģ����Ǹ�������ѡC�� �����Ѷȣ�һ�� 4��ѡ���� ԭ��صĵ缫���Ʋ�����缫���ϵ������йأ�Ҳ��������Һ�йأ�����˵���в���ȷ����(����) �ο��𰸣�D ���������A����Al��Cu��ϡH2SO4���ԭ��أ�Al��������Cu������������ͬ�ֵ����ų⣬���ֵ������������Էŵ�ʱSO42��������ɽ϶�ĸ���Al�缫�ƶ�����ȷ��B����Mg��Al��NaOH��Һ���ԭ��أ�Al���������为����ӦʽΪ��Al��3e����4OH��=AlO2����2H2O����ȷ��C����Al��Cu��Ũ�������ԭ��أ�����Al��Ũ�����лᷢ���ۻ�������Cu��������Al����������ԭ�������Դ����ʯī�缫�������������Һ����Ϊ�������պϻ�·�е���ת����Ŀ��ȡ�������1 mol Agʱ������ת��1mol,�����ĵ�Cu������Ϊ32 g����ȷ��D����Fe��Cu��FeCl3��Һ���ԭ��أ�Fe��Ա�Cuǿ����������Cu���������为����ӦʽΪ��Fe��2e��=Fe2��.���� �����Ѷȣ�һ�� 5������� ��4�֣���1����֪��һ����CH4��ȫȼ������CO2��Һ̬ˮʱ���ų�����QkJ������ȼ�ղ���ȫ��ͨ������ij���ʯ��ˮ���ɵõ�20g��������д��CH4ȼ�յ��Ȼ�ѧ����ʽ �ο��𰸣���1��CH4(g)+2O2(g)=CO2(g)+2H2O(l) ��H= -5QkJ/mol ��2�֣� �����������1��20g������̼��ƣ����ʵ�����0.2mol�����Ը���̼ԭ���غ��֪ȼ�����ɵ�CO2Ҳ��0.2mol����������1molCO2�ų���������5QkJ������Ȼ�ѧ����ʽΪ �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ����ɡ�����ʽ����.. | |
| �����Ŀ |