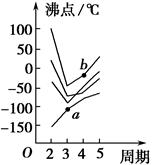
1、填空题 如图所示每条折线表示周期表ⅣA~ⅦA族中某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是____________,b点代表的是__________。
2、选择题 下列说法中,正确的是( )
A.NO2、BF3、NC13分子中没有一个分子中原子的最外层电子都满足8电子稳定结构
B.P4和CH4都是正四面体分子,两种分子中化学键之间的夹角相等且均为109°28′
C.(NH4)2SO4晶体中只有离子键
D.由原子间通过共价键而形成的晶体具有高熔、沸点及硬度
3、填空题 有H、C、O、Cl、Na五种元素。
(1)在由两种元素组成的化合物里,其中离子化合物有(写2种)______________________,共价化合物有(写2种)______________________。
(2)在由三种元素组成的化合物里,其中离子化合物有(写2种)______________________,共价化合物有(写2种)______________________。
4、选择题 .下列说法正确的是:
A.在化合物SiC中,Si显正价、C显负价是因为C的电负性大于Si的电负性
B.由于H与F的电负性差值为1.9大于1.7,所以HF是离子化合物
C.基态C原子有两个未成对电子,所以最多只能形成2个共价键
D.所有的原子轨道都具有一定的伸展方向,因此所有的共价键都具有方向性
5、计算题 物质结构理论有助于人们理解物质变化的本质,进行分子设计和研究反应规律。请回答下列问题:
(1)第三周期基态原子有2个未成对电子且电负性最大的元素是_____;
(2)金属晶体受到外力作用时易发生形变,而离子晶体容易破裂。试从结构的角度分析其中的主要原因____________;
(3)已知在水中存在平衡2H2O=H3O++OH-。下列分子中,中心原子采取的杂化方式与H3O+中氧原子的杂化方式相同的是_____
a.CH2=CH2中的碳原子? b.NH2-中的氮原子
c.ClO3-中的氯原子? d.NO2-中的氮原子
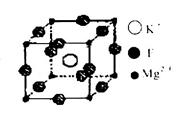
(4)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中Mg元素的质量分数为________。