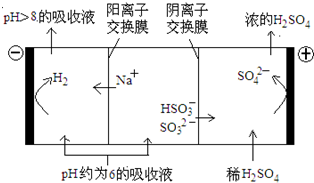
1、填空题 (12分)氯碱工业的原料饱和食盐水中含有一定量的铵根离子,在电解时会生成性质极不稳定的三氯化氮,容易引起爆炸。
(1)三氯化氮易水解,其水解的最初产物除生成氨气外,另一产物为 。
(2)为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为 ;该工艺选择氯气的优点是 。(答一点即可)
(3)过量氯气用Na2S2O3除去,反应中S2O32-被氧化为SO42-。若过量的氯气为1×10-3 mol,则理论上生成的SO42-为 mol。
(4)生产和实验中广泛采用甲醛法测定样品的含氮量。甲醛和铵根离子的反应如下:
4NH4+ + 6HCHO =(CH2)6N4H+(一元酸)+ 3H+ + 6H2O
实验步骤如下:
①已知甲醛溶液中常含有甲酸。取b mL甲醛溶液(过量)于锥形瓶,加入1滴酚酞,用浓度为c mol/L的NaOH溶液中和,滴定管的初始读数V1 mL,当溶液呈微红色时,滴定管的读数V2 mL。
②向其中加入饱和食盐水试样a mL,静置数分钟。
③再加1~2滴酚酞,再用上述NaOH溶液滴定至微红色,滴定管的读数V3 mL。
则饱和食盐水中的含氮量为 mg/L。
参考答案:(12分)
(1)HClO(2分)
(2)3Cl2 + 2NH4++ 8OH- = N2↑+ 6Cl- + 8H2O。(2分)
利用氯碱工业的产品氯气为原料,就近取材;不引入其他杂质离子。(2分)
(3)5×10-4(3分)
(4)14000C(V3―V2)/a mg/L (3分)
本题解析:(1)三氯化氮水解产生氨气,说明N原子与氢离子结合,所以Cl与氢氧根离子结合生成HclO;
(2)由题意可知,氯气与氨气反应,在碱性条件下生成氮气,则氯气被还原为氯离子,同时有水生成,离子方程式为3Cl2 + 2NH4++ 8OH- = N2↑+ 6Cl- + 8H2O;该过程选择氯气的原因是氯气本身是氯碱工业的产品,就近取材,同时氮气以气体放出,不会产生杂质离子;
(3)氯气被还原为氯离子,1×10-3 mol时转移电子的物质的量是2×10-3 mol,根据得失电子守恒,Na2S2O3在S的化合价是+2价,硫酸根中S的化合价是+6价,S的化合价升高4价,所以理论上生成的SO42-为2×10-3 mol/4=5×10-4mol;
(4)由题意可知,氢氧化钠滴定甲醛和铵根离子的反应产生的氢离子的物质的量是C(V3―V2) ×10-3 mol,由反应方程式得4NH4+~4 H+~4OH-,所以N的含量是C(V3―V2) ×10-3 mol×14g/mol/a×10-3 L=14000C(V3―V2)/a mg/L。
考点:考查反应在产物的判断,氧化还原反应规律的应用,滴定的计算
本题难度:困难
2、选择题 下列说法正确的是( )
A.pH=3的溶液中,Na+、Cl-、Fe2+、ClO-能大量共存
B.使石蕊变红的溶液中,Na+、I-、Cl-、NO3-、C6H5O-能大量共存
C.Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
D.室温下,向0.01mol/LNH4HSO4溶液中滴加NaOH溶液至中性,混合溶液中:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
参考答案:A、pH=3的溶液中存在大量的H+,H+、Fe2+、ClO-能发生氧化还原反应,则离子不能大量共存,故A错误;
B、使石蕊变红的溶液显酸性,H+、I-、NO3-能发生氧化还原反应,H+、C6H5O-能结合生成弱电解质,则离子不能大量共存,故B错误;
C、Na2CO3溶液中电荷守恒式为c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),物料守恒式为12c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-),
则c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3),故C正确;
D、NH4HSO4与NaOH的物质的量之比为1:1时溶液显酸性,NH4HSO4与NaOH的物质的量之比为1:2时溶液显碱性,则0.01mol/LNH4HSO4溶液中滴加NaOH溶液至中性,
NH4HSO4与NaOH的物质的量之比应大于1:1,小于1:2,此时溶液为硫酸钠、硫酸铵、氨水的混合溶液铵根离子的水解与氨水的电离程度相等,c(OH-)=c(H+),
由反应的物质的量可知c(Na+)>c(SO42-)>c(NH4+),故D正确;
故选CD.
本题解析:
本题难度:一般
3、选择题 下列事实不能用勒沙特列原理解释的是?(?)
A.浓度均为0.1 mol・L-1的新制氯水,加入少量NaHSO3晶体,片刻后,溶液中HClO
分子的浓度减小
B.室温下,将1 mL pH=3的醋酸溶液加水稀释至100 mL后,测得其pH<5
C.在硫化氢水溶液中加入碱有利于S2―的生成
D.500℃左右比室温更利于合成氨反应
参考答案:D
本题解析:D项,温度升高,化学反应速率增大,有利于合成氨反应,而与化学平衡的移动没有关系。ABC都涉及到化学平衡的移动。
本题难度:简单
4、选择题 能与铝反应放出氢气的溶液中,一定能够大量共存的离子组是 ( )
A.Ba2+、SO42-、Cl-、Na+
B.SO42-、K+、Cl-、CO32-
C.NH4+、Cl-、SO42-、K+
D.Na+、SO42-、Cl-、K+