1��ʵ���� ��12�֣����Ʊ��������о���ѧ�仯������Ҫ˼�뷽��������ϸ�۲��±���50mL
ϡ�����1g̼��Ʒ�Ӧ��ʵ�����ݣ�
ʵ��
���
| ̼���
״̬
| C(HCl)/ mol��l-1
| ��Һ�¶�/��
| ̼�����ʧ
ʱ��/s
|
��Ӧǰ
| ��Ӧ��
|
1
| ��״
| 0.5
| 20
| 39
| 400
|
2
| ��ĩ
| 0.5
| 20
| 40
| 60
|
3
| ��״
| 0.6
| 20
| 41
| 280
|
4
| ��ĩ
| 0.8
| 20
| 40
| 30
|
5
| ��״
| 1.0
| 20
| 40
| 120
|
6
| ��״
| 1.0
| 30
| 50
| 40
|
��1���÷�Ӧ���� ��Ӧ������ȡ����ȡ�����
��2��ʵ��5��6���� �Է�Ӧ���ʵ�Ӱ�졣
��3���ӱ�ʵ�������з�����Ӱ�컯ѧ��Ӧ���ʵ����ػ��� ���ܱ�����
һ���ɵ�ʵ������� ��
�ο��𰸣���1�� ���� ��2�� �¶� ��3�� ��Ӧ��Ӵ���� �٢�
�����������1����Ӧ����Һ�������ߣ�˵����Ӧ�Ƿ��ȷ�Ӧ��
��2��ʵ��5��6��ͬ�����¶ȣ����̽�������¶ȶԷ�Ӧ���ʵ�Ӱ�졣
��3�����ݷ�Ӧ�еı�����֪����ͬ�Ļ��з�Ӧ��ĽӴ���������Ӱ�컯ѧ��Ӧ���ʵ����ػ��з�Ӧ��Ӵ��������Ӧ��ʵ����1��2��
�����Ѷȣ�һ��
2������� �������з�Ӧ��2SO2+O2?
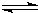
?2SO3�����2min��SO2��Ũ����6mol/L�½�Ϊ2mol/L����ô����SO2Ũ�ȱ仯����ʾ�Ļ�ѧ��Ӧ����Ϊ______����O2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ______�������ʼʱSO2Ũ��Ϊ4mol/L��2min��Ӧ��ƽ�⣬�����ʱ����v��O2��Ϊ0.5mol/��L?min������ô2minʱSO2��Ũ��Ϊ______��
�ο��𰸣���v��SO2��=��C��t=6mol/L-2mol/L2min=2mol/L��min��
?��ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ����������ķ�Ӧ����Ϊ���������һ�룬������1mol/L��min��
��ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ��������ķ�Ӧ����Ϊ0.5 mol/��L?min��ʱ����������ķ�Ӧ����Ϊ1mol/��L?min����
v��SO2��=��C��t=C��ʼ-C2min��t=4mol/L-C2min2min=1mol/��L?min����C2min=2mol/L
���������
�����Ѷȣ�һ��
3��ѡ���� ��N2+3H2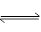 2NH3��Ӧ�У��Է�Ӧ��ʼ��2 sĩ������Ũ����0��Ϊ0.4 mol��L-1������������Ũ�ȱ仯��ʾ�÷�Ӧ��2s�ڵ�ƽ����Ӧ�����ǣ�?��
2NH3��Ӧ�У��Է�Ӧ��ʼ��2 sĩ������Ũ����0��Ϊ0.4 mol��L-1������������Ũ�ȱ仯��ʾ�÷�Ӧ��2s�ڵ�ƽ����Ӧ�����ǣ�?��
A��0.3 mol��L-1��s-1
B��0.4 mol��L-1��s-1
C��0.6 mol��L-1��s-1
D��0.8 mol��L-1��s-1
�ο��𰸣�A
�������������Ũ����0��Ϊ0.4 mol��L-1��������ʾ�ķ�Ӧ������0.4 mol��L-1��2s��0.2 mol��L-1��s-1������Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ����������ķ�Ӧ������0.3 mol��L-1��s-1����ѡA��
�����Ѷȣ���
4��ѡ���� ��Ӧ4NH3��g��+5O2��g��?4NO��g��+6H2O��g����5L�ܱ������н��У�����Ӻ�NO�����ʵ���������0.3mol�����ʾ�˷�Ӧ��������ȷ���ǣ�������
A��v��O2��=0.01mol?��L?s��-1
B��v��NO��=0.008mol?��L?s��-1
C��v��H2O��=0.003mol?��L?s��-1
D��v��NH3��=0.02mol?��L?s��-1
�ο��𰸣��ɰ���Ӻ�NO�����ʵ���������0.3mol������NO��ʾ�Ļ�ѧ��Ӧ����Ϊ
V��NO��=��C��t=��nV��t=0.3mol5L30s=0.002mol?��L?s�� -1
A���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��O2��=54V��NO��=54��0.002mol?��L?s��-1=0.0025 mol?��L?s��-1����A����
B����NO��ʾ�Ļ�ѧ��Ӧ����ΪV��NO��=0.002mol?��L?s��-1����B����
C���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���V��H2O��=64V��NO��=64��0.002mol?��L?s��-1=0.003 mol?��L?s��-1����C��ȷ��
D���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���V��NH3��=V��NO���T0.002mol?��L?s��-1����D��ȷ��
��ѡ��CD��
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪C��s��+ CO2��g��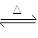 ?2CO��g������ӦΪ���ȷ�Ӧ�����д�ʩ��ʹ����Ӧ���ʼӿ���ǣ�?��
?2CO��g������ӦΪ���ȷ�Ӧ�����д�ʩ��ʹ����Ӧ���ʼӿ���ǣ�?��
����������C��s��?�������¶�?���������䣬��ͨ��CO2?����С�������ѹǿ
A���٢ڢ�
B���٢ڢۢ�
C���ڢ�
D���ڢۢ�
�ο��𰸣�D
���������������������Է�Ӧ���ʵ�Ӱ�졣����Ӧ��Ũ�Ȼ������¶Ȼ�����ѹǿ��ʹ�ô�������������Ӧ���ʡ�̼�ǹ��壬���������ٲ�Ӱ�췴Ӧ���ʡ����Դ���D��
�����Ѷȣ���