1��ʵ���� ijͬѧ������ԭ��ط�Ӧ���Zn��Cu�Ľ������˳���������ѡ�����˵IJ��Ϻ��Լ����һ��ԭ��أ����������ʵ�鱨�棺
ʵ��Ŀ�ģ�̽��Zn��Cu�Ľ������˳��
��1���缫 ���ϣ������� �������� ��
�������Һ�� ��
��2��д���缫��Ӧʽ��
������ �������� ��
��3��ʵ������
��4��ʵ����ۣ�
�ο��𰸣���1��ͭƬ��пƬ �� CuSO 4��Һ�����������𰸣�
��2��������Cu2+ + 2e�� �� Cu ������Zn
���������
�����Ѷȣ�һ��
2��ѡ���� һ���ɼ״���CH3OH���������Լ������������������Һ�����͵�أ��������ĵ缫��ӦʽΪ�� 2CH3 OH��16OH��
�ο��𰸣�
���������
�����Ѷȣ�����
3��ѡ���� ���з�Ӧ�У�����Ϊ��ƻ�ѧ��Դ�����ݵ��ǣ�������
A��HCl��NaOH��Ӧ
B��SO3��H2O��Ӧ
C��H2��O2��Ӧ
D��Ba��OH��2?8H2O��NH4Cl��Ӧ
�ο��𰸣�A��������������Ʒ�Ӧ��������кͷ�Ӧ����Ԫ�صĻ��ϼ۲��䣬���ڷ�������ԭ��Ӧ�����Բ�����Ƴɻ�ѧ��Դ����A����
B�����������ˮ��Ӧ�������ᣬ�÷�Ӧ���ڷ�������ԭ��Ӧ�����Բ�����Ƴɻ�ѧ��Դ����B����
C��������������Ӧ����ˮ�ҷų������ȣ��÷�Ӧ����������ԭ��Ӧ����������Ƴɻ�ѧ��Դ����C��ȷ��
D��Ba��OH��2?8H2O��NH4Cl��Ӧ���ڸ��ֽⷴӦ����Ԫ�ػ��ϼ۲��䣬�Ƿ�������ԭ��Ӧ���Ҹ÷�Ӧ���ȣ����Բ�����Ƴɻ�ѧ��Դ����D����
��ѡC��
���������
�����Ѷȣ���
4������� �Ķ��±��в��ֶ���������Ԫ�ص������Ϣ��

��ش�
��1��Ԫ��T��X��ԭ�Ӹ�����1:1�γɵĻ�����B�����Ļ�ѧ����____________ ���ѧ�����ƣ�����֪��ͨ�������£�39g B������CO2��Ӧ�ų�Q kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ ____________��
��2��д��YԪ������������Ӧˮ����ĵ��뷽��ʽ��__________________ ����Y��Z�γɵĻ������ˮ��Һ����μ��뵽T������������Ӧˮ�������Һ��ֱ���������ߵμӱ�����д���˹����з�����Ӧ�����ӷ���ʽ______________ ��______________ ��
��3����֪1mol������A��Na2SO3����Һ�з�����Ӧʱ��ת��2 mol���ӣ�д���÷�Ӧ�����ӷ���ʽ________________ ��
��4����һ�������£�X��Y���ֵ����Լ��п��Ե缫�ڻ�����TZ��ˮ��Һ�п��γ�ԭ��أ�Ϊ���ͺ�ˮ������ṩ��Դ��д����ԭ��������ĵ缫��Ӧʽ____________________ ��
�ο��𰸣���1�����Ӽ����Ǽ��Թ��ۼ�?��
2Na2O2��s��+ 2CO2��g�� �� 2Na2CO3��s��+ O2��g������H��-4Q kJ/mol?
��2��H++AlO2-+H2O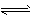 Al(OH)3
Al(OH)3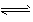 Al3++3OH-? ?��Al3++4OH-�� AlO2-+2H2O ��
Al3++3OH-? ?��Al3++4OH-�� AlO2-+2H2O ��
Al3+ + 3AlO2-+ 6H2O�� 4Al(OH)3��?
��3��SO32- + ClO- �� SO42- + Cl-?
��4��O2 + 4e- + 2H2O �� 4OH-
���������
�����Ѷȣ�һ��
5���ж��� ��10�֣��������վñ������ɫ�����������������������������ԭ���ԭ�����С���?�⡱ ��?�䴦������Ϊ����һ��Ũ�ȵ�ʳ����Һ����һ���������У��ٽ���ڵ�����������Һ�У�����һ��ʱ���ɫ����ȥ�����ָ������Ҳ�����ʧ���Իش�
��1��ʳ�ε�������?��
��2���ڴ�ԭ��ط�Ӧ�У����������ĵ缫��ӦΪ?�����������ĵ缫��ӦΪ?��
��3����Ӧ�����в�����������ζ�����壬��Һ�з����ķ�ӦΪ?��ԭ����ܷ�Ӧ����ʽΪ?��
��4��ʵ�ʲ����У�����ʳ��ˮʱ��ͨ��������һ������С�մ�����Ҫ������?����һ��Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���1���������������
��2��2Al-6e-�T�T2Al3+
3Ag2S+6e-�T�T6Ag+3S2-
��3��2Al3++3S2-+6H2O�T�T2Al��OH��3��+3H2S��
2Al+2Ag2S+6H2O�T�T6Ag+2Al��OH��3��+3H2S��
��4����ȥ���ɵ�H2S����ֹ��Ⱦ����
H2S+NaHCO3�T�TNaHS+H2O+CO2����
�����������1���γ�ԭ�����Ҫ����ʵ��磬���NaCl��������������á�
��2�����������Ϣ����ɫ��ȥ����������ʧ�������뷢��Ag2S Ag�仯��
Ag�仯��
���������ã�Ϊ������ʧ���ӱ��Al3+,��ӦΪ��Al-3e-�T�TAl3+��Ag2S��ΪAg��S2-���õ��ӣ���ԭ��ص���������ӦΪ��Ag2S+2e-�T�T2Ag+S2-��
��3����Һ��
2Al3++3S2-+6H2O�T�T2Al��OH��3��+3H2S����
��ˣ��ܷ�ӦΪ��2Al+3Ag2S+6H2O�T�T6Ag+2Al��OH��3��+3H2S����
��4�������ж������ȥ����ˣ�NaHCO3�������dz�ȥ���ɵ�H2S����ֹ��Ⱦ��������ӦΪ��
H2S+NaHCO3�T�TNaHS+H2O+CO2����
�����Ѷȣ���