1��ѡ���� ��ť�۵�����ִ��������й㷺Ӧ�ã���һ����п��أ���缫�ֱ���Ag2O��Zn���������ҺΪKOH���缫��ӦΪ��Zn+2OH--2e=ZnO+H2O��Ag2O+H2O+2e=2Ag+2OH-������������Ӧʽ���ж�������������ȷ���ǣ�������
A����ʹ�ù����У���ظ�������Һ��pH��С
B��ʹ�ù����У�������Ag20�������·����Zn��
C��Zn�Ǹ�����Ag2O������
D��Zn�缫������ԭ��Ӧ��Ag2O�缫����������Ӧ
�ο��𰸣�A����������Zn+2OH--2e=ZnO+H2O��c��OH-����С�����Ե�ظ�������Һ��pH��С����A��ȷ��
B��ZnΪ������Ag2OΪ��������ʹ�ù����У�������Zn�������·����Ag20������B����
C��Znʧȥ���ӣ�ZnΪ������Ag2O�õ���������������C��ȷ��
D��Zn�缫����������Ӧ��Ag2O�缫������ԭ��Ӧ����D����
��ѡAC��
���������
�����Ѷȣ���
2������� ��ͭ-пԭ����У�������Ӧ�۲쵽�������ǣ�ͭƬ�ϣ�______пƬ�ϣ�______����ʱԭ��صĵ缫��Ӧʽ�ǣ�������______������______������ʵ��ʵ���У�пƬ��Ҳ��______�������ڵ�������ԭ����______��
����ͬ�¶��£�ͬ����С�Ļ���̼�������ʵ�п�ȴ�п��ͬŨ��ͬ�����ϡ���ᷴӦ������______��ѡ�Ҫ�족����Ҫ����������ȡ�������ȷ�����������۽�����______��
�ο��𰸣���ԭ����У�ͭƬ�ϣ������ӵõ����������������Կ����������ǣ���������������ݣ�пƬ�ϣ�пʧȥ��������п���ӽ�����Һ��пƬ���ܽ⣬���Կ����������ǣ����������ݣ���пƬ���ܽ⣻ͭƬ��������пƬ�������������ϵĵ缫��ӦʽΪ��2H++2e-=H2���������ϵĵ缫��ӦʽΪ��Zn-2e-=Zn2+��
? ����ʵ��ʵ���У�����п����������̼�����ʣ�п��̼��ϡ���ṹ��С��ԭ��أ���п��̼����һ�����Կ���пƬ�������ݡ������ڵ�����
? ����ͬ�����£���п�ȴ�п��Ӧ���ʿ죬��������пƬ�ϵõ�����������������Ҫ�˷�п���Ӷ������ų���������ͭƬ�ϵõ�����������������ͨ��������������Խ�����Щ����������ͬ�����´�п�ȴ�п��Ӧ���ʿ죮
�ʴ�Ϊ����������������ݣ����������ݣ���пƬ���ܽ⣻2H++2e-=H2����Zn-2e-=Zn2+�����ݣ�п����������̼�����ʣ�������ϡ�������γ�������أ�Ҫ�죻�����Ӳ���Ҫ�˷�п���Ӷ������ų�����пƬ�ϵõ��ӣ�����ͨ������������ͭƬ�ϵõ��ӣ�
���������
�����Ѷȣ�һ��
3��ѡ���� ��ͼ��ij�ռ�վ����ת��ϵͳ�ľֲ�ʾ��ͼ������ ȼ�ϵ�ز���KOHΪ���Һ�������й�˵���в���ȷ����
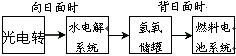
[? ]
A��������ת��ϵͳ�е�ˮҲ�ǿ���ѭ����
B��ȼ�ϵ��ϵͳ����������ʵ����������ˮ
C��ȼ�ϵ�طŵ�ʱ�������缫��Ӧʽ��2H2O+O2+4e-��4OH-
D��ȼ�ϵ�طŵ�ʱ�ĸ����缫��Ӧʽ��2H2+4OH--4e-��4H2O
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� �����������ؼ������ģ�飬�ǹ��ҡ�ʮ�塱863�ƻ��綯����ר����һ����Ҫ���⣮�ҹ������ؾ������Ƚ�ˮƽ����ž�DZͧ��װ�����������������أ����������ص�ij���Ǵ���Ͻ�LaNi5H6��LaNi5H6�и�Ԫ�ػ��ϼ۾�Ϊ�㣩����ط�Ӧͨ����ʾΪ��LaNi5H6+6NiO��OH��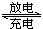 LaNi5+6Ni��OH��2
LaNi5+6Ni��OH��2
�����й������ص�˵��������ȷ���ǣ� ? ��
A����ع���ʱ������Ͻ�������
B����س��ʱ����������������Ӧ
C����طŵ�ʱ������������ͨ�����·����
D����ع���ʱ��������Ӧʽ��LaNi5H6+6OH--6e-�TLaNi5+6H2O
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5�������
Li-SOCl2��ؿ����������������õ�صĵ缫���Ϸֱ�Ϊ﮺�̼�����Һ��
LiAlCl4-SOCl2����ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2=4LiCl+S+SO2�� ?
��ش��������⣺ ?
(1)��صĸ�������Ϊ__________�������ĵ缫��ӦΪ____________�� ?
(2)������������ĵ缫��ӦΪ________��
(3)SOCl2�ӷ���ʵ�����г���NaOH��Һ����SOCl2����Na2SO3��NaCl���ɡ����������ˮ�ε�SOCl2�У�ʵ��������____________����Ӧ�Ļ�ѧ����ʽΪ________________��?
(4)��װ�õ�ر�������ˮ�������������½��У�ԭ����____________________��
�ο��𰸣�(1)Li��Li-e-=Li+?
(2)2SOCl2+4e-= 4Cl-+S+SO2��?
(3)���ְ������д̼�����ζ���������ɣ�SOCl2+H2O=SO2��+2HCl��?
(4)��Ϊ���ɵ�ص���Ҫ�ɷ�Li�ܺ�������ˮ��Ӧ��SOCl2��Ҳ��ˮ��Ӧ
���������
�����Ѷȣ�һ��