1、填空题 12.4?g?Na2R含Na+0.4?mol,则Na2R的摩尔质量为________,R的相对原子质量为________。含R的质量为1.6?g的Na2R,其物质的量为________。
参考答案:62 g・mol-1;16;0.1 mol
本题解析:
本题难度:一般
2、简答题 实验室需要500ml?0.4mol?L-1的NaOH溶液,配制时:
(1)需称量______g的烧碱固体,固体应放在______中置于天平的左盘称量.
(2)配制过程中,下列仪器中肯定不需要使用的是______.
(3)根据实验的实际需要和(2)中列出的仪器判断,完成实验还缺少的仪器是(填仪器名称)______.
(4)若实验时遇到下列情况,所配溶液的浓度偏大的是______.
A.加水定容时超过刻度线,又吸出少量水至刻度线
B.忘记将洗涤液转入容量瓶
C.容量瓶洗涤后内壁有水珠而未作干燥处理
D.溶液未冷却即转入容量瓶
E.定容时俯视刻度线.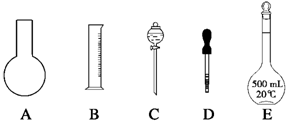
参考答案:(1)需氢氧化钠的质量为m=0.5L×0.4mol?L-1×40g/mol=8.0g.
氢氧化钠有腐蚀性,易潮解,应放在小烧杯内迅速称量.
故答案为:8.0;小烧杯.
(2)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
所以需要的仪器有天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙.
根据给出的仪器可知肯定不需要使用的是圆底烧瓶、分液漏斗.
故选:AC.
(3)由(2)可知还需要的仪器为天平、烧杯、玻璃棒、药匙.
故答案为:天平、烧杯、玻璃棒、药匙
(4)A.定容时,加水超过刻度线,使溶液的体积偏大,所配溶液浓度偏低,溶液是均匀的,再用胶头滴管吸出多余的部分,剩余溶液与所配溶液浓度相同,溶液浓度偏低;
B.未将洗涤液转入容量瓶,移入容量瓶中氢氧化钠的实际质量减小,溶液浓度偏低;
C.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
D.液体具有热胀冷缩的性质,氢氧化钠溶解放热,未冷却到室温,趁热将溶液到入容量瓶,并配成溶液,会导致溶液体积偏小,溶液浓度偏大;
E.定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓度偏大.
故选:DE
本题解析:
本题难度:一般
3、选择题 下列说法正确的是
A.2mol的盐酸
B.0.1mol氢
C.0.3molHCl
D.4mol的氧元素
参考答案:C
本题解析:用摩尔表示物质的量的单位时必须要用化学式指明粒子的种类,否则造成表达不清楚,所以
A错,盐酸为混合物,是物质不是微观粒子;B错,0.1mol氢指代不明,是氢离子还是氢原子或氢分子;C正确;D错,通常用化学式指明,不是元素符号;
本题难度:简单
4、选择题 某学生配制氯化钠溶液时,用天平称取氯化钠固体20.6 g,(1g以下由游码提供),因砝码与氯化钠的位置放反了,天平恰好平衡,用称量的该氯化钠配制溶液,则所配溶液浓度
[? ]
A.偏高
B.偏低
C.无影响
D.无法确定
参考答案:B
本题解析:
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数,下列说法正确的是?(?)
①18g D2O含有的电子数为10NA;②1mol Na2O2与水完全反应时转移电子数为2NA;③三硫化四磷分子中没有不饱和键,且各原子的最外层均已达到了八个电子的结构。在1mol三硫化四磷分子中含有的共价键数是9NA ?;④在标准状况下,22.4LSO3的物质的量为1mol;⑤6.2g氧化钠和7.8g过氧化钠混合物中所含有的离子数约为0.6×6.02×1023
A.②④? B.③⑤? C?①②③? D.①④⑤
参考答案:B
本题解析:略
本题难度:一般