1������� �����������ʢ�NaCl��Һ�ڸɱ�����̬�Ķ�����̼���۱����ᣨ�����Ĵ��ᣩ��ͭ��BaSO4��������Ǣ߾ƾ������ڵ�KNO3���������ڵ���ʵ��ǣ�______�����ڷǵ���ʵ���______���ܵ������______������д��ţ�
�ο��𰸣���1���������ˮ��Һ���ۻ�״̬���ܹ�����Ļ����������ˮ��Һ�ܹ����磬���������ڵ���ʣ����ᱵ��ˮ��Һ���ܵ��磬����Ϊ���ᱵ���ܽ��̫С�����ᱵ���ڵ���ʣ�����״̬������������������Ӻ���������Ӷ����磬�����������ڵ���ʣ���ˣ����ڵ���ʵ��Ǣۢݢ࣮
��2���ǵ������ָ��ˮ��Һ����ۻ�״̬�¶����ܵ���Ļ�������ǡ��ƾ�ˮ��Һ�����磬���ڷǵ���ʣ��ɱ���������̼��ˮ��Һ�ܵ��磬����Ϊ������̼��ˮ��Ӧ�����˵����̼�ᣬ���Ƕ�����̼������Ե�ʣ���˸ɱ����ڷǵ���ʣ������ڷǵ���ʵ�ֻ�Тڢޢߣ�
��3���������ˮ��Һ���ۻ�״̬���ܹ����磬NaCl��Һ�ǵ�����Ȼ��Ƶ�ˮ��Һ�����ܹ����磻���ڵ�������д������ɵļ����Ӻ���������ӣ��ܹ����磻ͭ���ڽ������ܹ����磮���ܹ�������Т٢ܢ࣮
�ʴ�Ϊ���ۢݢࣻ�ڢޢߣ��٢ܢ�
���������
�����Ѷȣ�һ��
2��ѡ���� ����������������Һ����ʹ��Һ���������������������ٵ���
A��Cl-
B��Ba2��
C��CO32-
D��Na+
�ο��𰸣�BC
�����������
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ��д��ȷ����
A.��������Һ�м��������ˮ��Al3++4NH3?H2O�TAlO2-+4NH4++2H2O
B.�����������Һ��ͨ������SO2���壺ClO-+SO2+H2O�THClO+HSO3-
C.��Ͷ��CuSO4��Һ�У�2Na+Cu2++2H2O�T2Na++Cu��OH��2��+H2��
D.����ϡHNO3��Ӧ����ҺpH=2��3Fe+8H++2NO3-�T3Fe2++2NO��+4H2O
�ο��𰸣�C
���������������A����Ӧ������������������泥�
B������������ԭ��Ӧ���������ƣ�
C����Ӧ���������ơ�������ͭ��������
D����ҺpH=2�������������Ӧ������������NO��ˮ��
���A����������Һ�м��������ˮ�����ӷ�ӦΪAl3++3NH3?H2O�TAl��OH��3��+4NH4+����A����
B�������������Һ��ͨ������SO2��������ӷ�ӦΪClO-+SO2+H2O�T2H++Cl-+SO42-����B����
C����Ͷ��CuSO4��Һ�е����ӷ�ӦΪ2Na+Cu2++2H2O�T2Na++Cu��OH��2��+H2������C��ȷ��
D������ϡHNO3��Ӧ����ҺpH=2�������ӷ�ӦΪFe+4H++NO3-�TFe3++NO��+2H2O����D����
��ѡC��
���������⿼�����ӷ�Ӧ����д����ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ���ע�ⷢ����������ԭ��ӦΪ�����ѵ㣬��Ŀ�Ѷ��еȣ�
�����Ѷȣ���
4��ѡ���� �������ӷ�Ӧ����ʽ��ȷ����
A.������ͭ�缫���ʳ��ˮ��2Cl-+2H2O?2OH-+H2��+Cl2��
B.��ʴ������ӡˢ��·�壺Fe3++Cu�TFe2++Cu2+
C.��ͭ���缫�������ͭ��Һ��2Cu2++2H2O2Cu+O2��+4H+
D.AlCl3��Һ�����Ե�ԭ��Al3++3H2O?Al��OH��3+3H+
�ο��𰸣�D
������������������ӷ���ʽ��ָ��ʵ�ʲμӷ�Ӧ�����ӷ��ű�ʾ���ӷ�Ӧ��ʽ�ӣ����ӷ���ʽ����д����һ��Ϊ��
�١�д����д���йط�Ӧ�Ļ�ѧ����ʽ���ڡ��𡱣������Եĵ���������ӷ��ű�ʾ���������ܵ����ʡ����塢ˮ�����û�ѧʽ��ʾ���ۡ�ɾ����ɾȥ����ʽ���߲��μӷ�Ӧ�����ӣ� �ܡ��顱�����ʽ�����ߵĸ���ԭ�ӵĸ�����������Ƿ���ȣ�
A�������У�����ͭ������ʱ��ͭ�缫����ʧȥ���ӣ�
B������ʽ���ҵ�ɲ��غ㣻
C����ͭ���缫�������ͭ��Һ����ͭ��������ͭ�缫����ʧȥ���ӣ�
D��AlCl3��Һ�����������������ӵ�ˮ�⣬����ʽ�����غ㣻
���A������ͭ������ʱ��ͭ�缫����ʧȥ���ӣ�������ӦΪCu-2e-=Cu2+��������ˮ�е������ӷŵ磬�ʵ��ԭ������ʽΪCu+2H2O Cu��OH��2��+H2������A����
Cu��OH��2��+H2������A����
B������ʽ��ߴ�3����λ�ĸ���ɣ��ұߴ�4����λ������ɣ���ȷ��Ϊ��2Fe3++Cu�T2Fe2++Cu2+����B����
C����ͭ���缫�������ͭ��Һ������ͭ�缫����ʧȥ���ӷ�ӦΪCu-2e-=Cu2+������ΪCu2++2e-=Cu����C����
D����AlCl3Ϊǿ�������Σ�������ˮ����Һ�����ԣ�ˮ���ǿ����Al3++3H2O?Al��OH��3+3H+������ʽ���Ҹ���ԭ�ӵĸ������������ȣ���D��ȷ��
��ѡD��
���������⿼�����ӷ���ʽ����д����ȷ�����ķ�Ӧ����Ϥ���ӷ�Ӧ����ʽ����д�����ǽ����Ĺؼ�����Ŀ�ѶȲ���
�����Ѷȣ�����
5��ѡ���� �����Ƿ���ȷ
A.������Һ��̼������Һ��ӦCO2��C6H5OH+CO32-��C6H5O-+CO2��+H2O
B.CH3CHBrCOOHCH2=CHCOONa+NaBr+2H2O
C.̼����ˮ�⣺CO32-+H2O?HCO3-+OH-
D.̼��������Һ��̼�����Ƶ�ˮ�⣺HCO3-+OH-?CO32-+H2O
E.�ڱ�״���£�H2O2��ˮ����������ܣ����Ʋ�H2S��ˮ�����������
F.�ýṹΪ�����ʷ��ӵ������ṹ��һ���ṹΪ�������������ṹΪ�����ṹ�������ṹΪ�����۵�����ά�ṹ
�ο��𰸣�C
���������������A����Ӧ���ɱ����ƺ�̼�����ƣ�
B��NaOHˮ��Һ�У�����ˮ�ⷴӦ����������ȥ��Ӧ��
C��ˮ��ֲ����У��Ե�һ��Ϊ����
D��ˮ������̼������������ӣ�
E�����ⲻ����ˮ������������ܣ�
F���ļ��ṹ�вų�����ά�ṹ��
���A��������Һ��̼������Һ��Ӧ�����ӷ�ӦΪC6H5OH+CO32-��C6H5O-+HCO3-����A����
B��NaOHˮ��Һ�з���CH3CHBrCOOH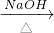 CH3CH��OH��COONa+NaBr+H2O����B����
CH3CH��OH��COONa+NaBr+H2O����B����
C��̼����ˮ������ӷ�ӦΪCO32-+H2O?HCO3-+OH-����C��ȷ��
D��̼��������Һ��̼�����Ƶ�ˮ������ӷ�ӦΪHCO3-+H2O?H2CO3+OH-����D����
E��H2O2��ˮ���γ��������������������ܣ���H2S��ˮ�����γ����������������������ܣ���E����
F����ͼ��֪���ڵ������е��ļ��ṹ�г�����ά�ṹ����F����
��ѡC��
���������⿼��֪ʶ��϶࣬ע�����ӷ�Ӧ�Ŀ��飬��Ϥˮ������ӷ�Ӧ��������л���ѧ��Ӧ�������Ĺ�ϵ���ɽ����Ŀ�ѶȲ���
�����Ѷȣ���