1、填空题 (10分)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2与水反应生成乙炔的化学方程式?;
CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为?_________________________。
(2)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是?;分子中处于同一直线上的原子数目最多为?。
(3)金刚石的晶胞如图所示,已知六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,立方氮化硼晶体密度为ag/cm3, 表示阿伏加德罗常数,则立方氮化硼晶胞体积为?cm3。
表示阿伏加德罗常数,则立方氮化硼晶胞体积为?cm3。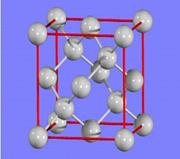
2、选择题 金属晶体的下列性质中,不能用金属晶体结构加以解释的是
A.易导电
B.易导热
C.有延展性
D.易锈蚀
3、选择题 某物质熔融状态可导电,固态可导电,将其投入水中水溶液也可导电,则可推测该物质可能是?(?)
A.金属晶体
B.分子晶体
C.原子晶体
D.离子晶体
4、选择题 下列说法正确的是(?)
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.H2O比H2S稳定,是因为H2O分子间能形成氢键而H2S不能
C.晶体中含阳离子就一定含阴离子
D.基态24Cr原子的电子排布式为:〔Ar〕3d44s2
5、选择题 钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是
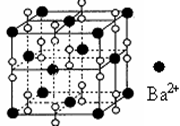
A.该晶体属于离子晶体
B.晶体的化学式为Ba2O2
C.该晶体晶胞结构与NaCl相似
D.与每个Ba2+距离相等且最近的Ba2+共有12个