1������� ��10�֣���Ȳ���л��ϳɹ�ҵ��һ��ԭ�ϡ���ҵ������CaC2��ˮ��Ӧ������Ȳ��
��1��CaC2��ˮ��Ӧ������Ȳ�Ļ�ѧ����ʽ?��
CaC2��C22-��O22+��Ϊ�ȵ����壬O22+�ĵ���ʽ�ɱ�ʾΪ?_________________________��
��2����Ȳ�������ᷴӦ�ɵñ�ϩ�棨H2C��CH��C��N������ϩ�������̼ԭ�ӹ���ӻ�������?�������д���ͬһֱ���ϵ�ԭ����Ŀ���Ϊ?��
��3�����ʯ�ľ�����ͼ��ʾ����֪�����������ڸ��¸�ѹ�£�����ת��Ϊ������������ṹ����ʯ���ƣ�Ӳ������ʯ�൱���������������ܶ�Ϊag/cm3�� ��ʾ�����ӵ����������������������Ϊ?cm3��
��ʾ�����ӵ����������������������Ϊ?cm3��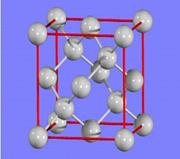
�ο��𰸣���1��CaC2+2H2O��Ca(OH)2+C2H2����2�֣�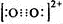 ?��2�֣�?
?��2�֣�?
��2��sp�ӻ�?sp2�ӻ���2�֣�? 3��1�֣�?��3��100/aNA?��3�֣�
�����������1��������Ȳ��ʵ������ȡ��C22-����14�����ӣ�����O22+�ĵ���ʽ�ɱ�ʾΪ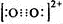 ��
��
��2����ϩ������к���̼̼˫����̼̼����������̼̼������̼ԭ����sp�ӻ���̼̼˫����̼ԭ����sp2�ӻ�������̼̼������ֱ���ͽṹ����̼̼˫����ֱ���ͽṹ�����Է����д���ͬһֱ���ϵ�ԭ����Ŀ���Ϊ3����
��3���ṹ����ʯ���ƣ����Ծ����к��еĵ�ԭ�Ӻ���ԭ�ӵĸ�������4�������Ըþ�����������4��25/NA����������100/aNA��
�����Ѷȣ���
2��ѡ���� ������������������У������ý�������ṹ���Խ��͵���
A������
B������
C������չ��
D������ʴ
�ο��𰸣�D
���������������ʴ��Ҫ�����ԭ�ӵĻ������й�ϵ��������Խ���ã�Խ�ױ���ʴ�������硢���Ⱥ���չ�����������Ľṹ�й�ϵ����������������н������й�ϵ����ѡD��
�����������dz�ʶ��֪ʶ�Ŀ��飬���ڼ�����֪ʶ�Ŀ��顣��������������ѧ����ѧϰ�����ģ��ѶȲ���
�����Ѷȣ���
3��ѡ���� ij��������״̬�ɵ���,��̬�ɵ���,����Ͷ��ˮ��ˮ��ҺҲ�ɵ���,����Ʋ�����ʿ�����?��?��
A����������
B�����Ӿ���
C��ԭ�Ӿ���
D�����Ӿ���
�ο��𰸣�A
�������������״̬�ܵ�����������ѡ����ֻ�н������壬������ˮ��Һ��Ҳ�ܵ��磬�п����ǽ�����ˮ��Ӧ�����ɵĵ������Һ���硣���Դ�ѡA��
�����Ѷȣ���
4��ѡ���� ����˵����ȷ���ǣ�?��
A�����Ӿ�����һ�����ڷ��Ӽ�����������һ�����ڹ��ۼ�
B��H2O��H2S�ȶ�������ΪH2O���Ӽ����γ������H2S����
C�������к������Ӿ�һ����������
D����̬24Crԭ�ӵĵ����Ų�ʽΪ����Ar��3d44s2
�ο��𰸣�A
���������A��ȷ������ϡ����������в����ڻ�ѧ�������Ӱ��������ʵ��������ʣ����ӵ��ȶ��Ժͻ�ѧ���й�ϵ��B����ȷ��C����ȷ���������������ֻ��������û�������ӡ����Ӵ���ȫ�������������ȶ��ģ�����D����ȷ���й��ǡ�Ar��3d54s1��������ȷ�Ĵ���A��
�����Ѷȣ�һ��
5��ѡ���� ����������ȼ��ʱ�õ�һ�ֱ��������ᄃ�壬�ṹ��ͼ��ʾ���й�˵������ȷ����
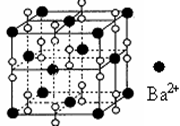
A���þ����������Ӿ���
B������Ļ�ѧʽΪBa2O2
C���þ��徧���ṹ��NaCl����
D����ÿ��Ba2+��������������Ba2+����12��
�ο��𰸣�B
���������
�𰸣�B
������Ba2��Ϊ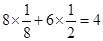 ��O22�DΪ
��O22�DΪ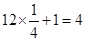 ��������ΪBaO2��A���þ�����Ba2����O22�D���ɣ��������Ӿ��壻 B������Ļ�ѧʽΪBaO2��C����ȷ���þ��徧���ṹ��NaCl���ƣ� D����ȷ����ÿ��Ba2+��������������Ba2+����12����
��������ΪBaO2��A���þ�����Ba2����O22�D���ɣ��������Ӿ��壻 B������Ļ�ѧʽΪBaO2��C����ȷ���þ��徧���ṹ��NaCl���ƣ� D����ȷ����ÿ��Ba2+��������������Ba2+����12����
�����Ѷȣ�һ��