| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《影响化学反应速率的因素》考点预测(2019年强化版)(十)
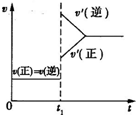 参考答案:向一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g)△H<0,当达到平衡后,t1时刻改变反应的某一条件,造成容器内压强增大,且混合气体总物质的量不变,故改变的条件为升高温度,升高温度正、逆反应速率均增大,但是逆反应速率大于正反应速率,反应逆向移动, 本题解析: 本题难度:一般 3、选择题 下列图示与对应叙述相符的是( ) 参考答案:A.由图象可知,反应物总能量大于生成物总能量,反应放热,升高温度平衡向逆反应方向移动,平衡向平衡常数K值减小,故A错误; 本题解析: 本题难度:简单 4、简答题 教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(2)若实验①在2min末收集了4.48mL?CO2(标准状况下),则在2min末,c(MnO4-)=______mol/L. (3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定______来比较化学反应速率. (4)小组同学发现反应速率总是如图二,其中t1~t2时间内速?率变快的主要原因可能是:①该反应放热、②______.  参考答案:(1)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大,故答案为:浓度;②;①; 本题解析: 本题难度:一般 5、选择题 在一密闭容器中发生反应:2X(g)+Y(g) | ||||||||||||||||||||||||||||||||||||||||||||||||
参考答案: D
本题解析: A项,图甲,在同一温度下(T1),p1压强下先达到平衡,说明p1>p2,由图可知压强大时Z的体积分数反而小,说明增大压强平衡逆向移动,则a>3;B项,图甲,在同一压强下(p2),T2温度下先达到平衡,说明T2>T1,由图可知温度高时Z的体积分数反而小,说明升高温度平衡逆向移动,则Q<0;D项,图乙,t2时正、逆反应速率同等倍数增大,则可能是使用了催化剂或a=3时增大压强。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《盐类水解的原理》.. | |