|
高考化学试题《氧化性和还原性强弱的比较》试题巩固(2019年最新版)(十)
2019-07-03 23:40:05
【 大 中 小】
|
1、选择题 已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性是顺序为SO2 > I- > Fe2+ > H2O2> Cl-,则下列反应不可能发生的是( )
A.2Fe2++Cl2=2Fe3++2Cl-
B.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
C.H2O2+H2SO4=SO2↑+O2↑+2H2O
D.SO2+I2+2H2O=H2SO4+2HI
|
参考答案:C
本题解析:在反应中氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。A.由于还原性:Fe2+ > Cl-,所以2Fe2++Cl2=2Fe3++2Cl-能发生,正确;B.由于还原性:SO2 > Fe2+;所以反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+能发生,正确;C.由于还原性:SO2 > H2O2,所以H2O2+H2SO4=SO2↑+O2↑+2H2O不可能发生,错误;D.由于还原性:SO2 > I- ,所以反应SO2+I2+2H2O=H2SO4+2HI能发生,正确。
考点:考查物质的还原性大小的比较及应用的知识。
本题难度:一般
2、选择题 Cl2的氧化性比S的氧化性强,最主要的事实是( )
A.通常情况下硫为浅黄色固体,而氯气为黄绿色气体
B.硫不溶于水,而氯气能溶于水
C.与金属反应时,硫被还原为-2价而氯被还原成-1价
D.与同一种金属反应时,金属被硫氧化成低价态,被氯气氧化成高价态
参考答案:A.物质的颜色为物理性质,与化学性质无关,不能用来比较氧化性强弱,故A错误;
B.物质的溶解性属于物理性质,不能用来比较化学性质,故B错误;
C.与金属反应时,非金属元素的化合价取决于最外层电子数目的多少,与氧化性强弱无关,故C错误;
D.与同一种金属反应时,金属被硫氧化成低价态,被氯气氧化成高价态,说明Cl得电子能力较强,氯气的氧化性强,故D正确.
故选D.
本题解析:
本题难度:一般
3、选择题 已知常温下,在溶液中发生如下反应:①16H++10Z-+2XO4-=2X2++5Z2+8 H2O;②2A2++B2=2A3-+2B-; ③2B-+Z2=B2+2Z-由此推断下列说法错误的是( )
A.反应Z2+2A2+=2A3++2Z-可以进行
B.Z元素在①③反应中均被还原
C.氧化性由强到弱的顺序是XO4-,Z2,B2,A3+
D.还原性由强到弱的顺序是Z-,B-,A2+,X2+
参考答案:A、根据反应2A2++B2=2A3-+2B-,可得氧化性是B2>A3+,2B-+Z2=B2+2Z-,可得氧化性是Z2>B2>A3+,反应Z2+2A2+=2A3++2Z-可以进行,故A正确;
B、Z元素在①中化合价升高,在反应中被氧化,在③中化合价降低,在反应中被还原,故B错误;
C、氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,:反应①16H++10Z-+2XO4-=2X2++5Z2+8H2O中,氧化性XO4->Z2;反应②2A2++B2=2A3-+2B-中,氧化性B2>A3+;
反应③2B-+Z2=B2+2Z-中,氧化性Z2>B2,所以氧化性由强到弱的顺序是XO4->Z2>B2>A3+,故C正确;
D、氧化还原反应中,还原剂的还原性强于还原产物的还原性,反应①16H++10Z-+2XO4-=2X2++5Z2+8H2O中,还原性Z->X2+;反应②2A2++B2=2A3-+2B-中,还原性A2+>B-;反应③2B-+Z2=B2+2Z-中,还原性B->Z-,所以还原性由强到弱的顺序是A2+>B->Z->X2+,故D错误.
故选BD.
本题解析:
本题难度:简单
4、选择题 下列实验能够达到实验目的是( )
A.
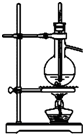
分离沸点相差较大的互溶液体混合物
B.
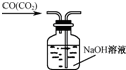
除去CO气体中得CO2气体
C.

电解饱和食盐水制氯气和氢气
D.
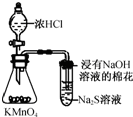
比较KMnO4、Cl2和S氧化性
参考答案:A.蒸馏操作时,温度计应位于蒸馏烧瓶支管口附近,用于测量馏分的温度,故A错误;
B.除去CO气体中得CO2气体,导管应长进短出,否则会导致洗气瓶内压强过大而将瓶塞顶开,故B错误;
C.电解饱和食盐水,阳极应为惰性电极,如用铜作阳极,在阳极上生成铜离子,不能得到氯气,故C错误;
D.高锰酸钾与浓盐酸反应生成氯气,氯气可与硫化钠反应生成单质S,可证明氧化性强弱,故D正确.
故选D.
本题解析:
本题难度:简单
5、选择题 将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
下列有关说法不正确的是(? )
A.氧化性Cr2O72->Fe3+>SO2
B.Cr2O72-能将Na2SO3氧化成Na2SO4
C.若33.6 L SO2(标准状况)参加反应,则最终消耗K2Cr2O7 0.5 mol
D.反应中Fe2(SO4)3既是氧化剂,又是还原剂
参考答案:D
本题解析:反应①Fe3+能氧化SO2,反应②说明Cr2O72-氧化性比Fe3+强,A项正确。Cr2O72-比Fe3+氧化性强,能氧化Na2SO3,B项正确。标准状况33.6 L SO2为1.5 mol,失电子3 mol,而K2Cr2O7中Cr为+6价,得电子变为+3价,0.5 mol K2Cr2O7得电子为3 mol,C项正确。反应①Fe2(SO4)3是氧化剂,而化合价没有升高没做还原剂,D项不正确。
本题难度:一般
|