| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《常见的化学电源》高频考点预测(2019年最新版)(二)
参考答案:D 本题解析:略 本题难度:一般 2、选择题 锂镉电池在现代生活中有广泛应用,它的充放电反应按下式进行: 参考答案:C 本题解析: 本题难度:简单 3、填空题 聚合氯化铝是一种新型净水剂,其中铝的总浓度(用AlT表示)包括三类‘“主要为Al3+的单体形态铝总浓度(用Ala表示);主要为[AlO4Al12(OH)24(H2O)12]7+的中等聚合形态铝总浓度(用Alb表示)和Al(OH)3胶体形态铝总浓度(用A1c表示)。
②如将AlT =" 2.520" mol・L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式: 。 ③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图1。当T>80℃时,AlT显著下降的原因是 。 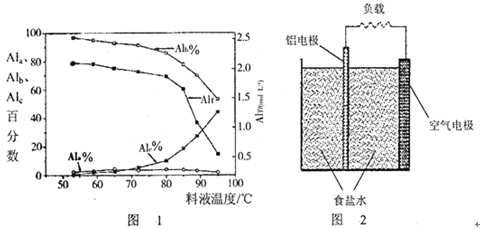 (3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下: ①Al2O3(s)+AlCl3(g)+3C(s) = 3AlCl(g)+3CO(g) △H1 =" a" kJ・mol-1 ②3AlCl(g) =" 2Al(l)+" AlCl3(g) △H2 =" b" kJ・mol-1 则反应Al2O3(s)+ 3C(s) =" 2Al(l)+" +3CO(g) △H = kJ・mol-1(用含a、b的代数式表示)。反应①常压下在1900℃的高温下才能进行,说明△H 0(填“>”“=”或“<”)。 (4)一种铝空气电池结构如图2所示,写出该电池正极的电极反应式 。 参考答案:(1)13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+;(2)①减小;②Al3++3H2O=Al(OH)3(胶体)+3H+;③温度升高,水解程度加大,产生氢氧化铝沉淀;(3)a+b;>;(4)O2+2H2O+4e-=4OH-。 本题解析:(1)根据题意结合原子守恒、电荷守恒可得生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+;(2)①在一定温度下,AlT越大,Ala%越大,Alc%越小,所以pH减小;②如将AlT =" 2.520" mol・L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O=Al(OH)3(胶体)+3H+;③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图所示。当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀;(3)①+②整理可得Al2O3(s)+ 3C(s) =" 2Al(l)+" +3CO(g) △H =△H1+△H2 =-(a+b)kJ/mol;反应①常压下在1900℃的高温下才能进行,说明该反应是吸热反应,△H>0;(4)在该铝空气电池中活动性强的Al作负极,活动性弱的C作正极。由于是在中性介质中,所以发生的是吸氧腐蚀。该电池正极的电极反应式是O2+2H2O+4e-=4OH-。 本题难度:困难 4、选择题 银锌电池的充电和放电过程可表示为: 2Ag+Zn(OH)2 参考答案:D 本题解析:根据原电池工作原理,负极上发生氧化反应.元素化合价会升高,所以在放电过程中被氧化的是Zn,即Zn为负极. 本题难度:一般 5、填空题 (8分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为: 参考答案:PbO2+2e-+4H++SO42-=PbSO4+2H2O;小;48;1 本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。又因为放电相当于是原电池,所以根据反应式可知,二氧化铅是正极,电极反应式是PbO2+2e-+4H++SO42-=PbSO4+2H2O。放电消耗硫酸,所以电解液中H2SO4的浓度将变小。负极是铅失去电子,1mol铅失去2mol电子,所以当外电路通过1 mol电子时,负极生成0.5mol硫酸铅,则理论上负极板的质量增加0.5mol×96g/mol=48g。根据总的反应式可知消耗H2SO4物质的量1mol。 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《铝》高频考点预测.. | |