1、填空题 23.已知:铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
负极反应为:Cd+2OH--2e-=Cd(OH)2
铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用。镍镉碱性充电电池使用(放电)到后期,当电压明显下降时,其内阻却几乎不变,此时充电后也能继续使用。回答下列问题:
⑴铅蓄电池在放电时的负极反应为?,其在充电时阳极反应为?;
⑵镍镉碱性充电电池在充电时的总反应的化学方程式为?;
⑶上述两种电池使用一段时间后,一个内阻明显增大,而另一个内阻却几乎不变的主要原因可能是?;
⑷如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO4?mol。
参考答案:(1)Pb+SO42―-2e―=PbSO4? PbSO4+2H2O-2e―=PbO2+SO42―+4H+
(2)Cd(OH)2+2Ni(OH)2=Cd+2NiO(OH)+2H2O
(3)铅蓄电池放电时离子浓度减小,而镍镉电池放电时离子浓度不变
(4)2
本题解析:略
本题难度:一般
2、选择题 (08广州综合测试,17)甲醇(CH3OH)燃料电池可用于笔记本电脑、汽车等,一极通入甲醇,另一极通入氧气,电池工作时,H+由负极移向正极。下列叙述正确的是(?)
A.氧气为负极
B.甲醇为负极
C.正极反应为:O2+4H++4e-="=" 2H2O
D.负极反应为:CH3OH+H2O+6e- ="=" CO2↑+ 6H+
参考答案:BC
本题解析:本题考查原电池原理,中等题。该燃料电池中甲醇为负极,电极反应为:CH3OH+H2O-6e-=CO2↑+6H+,B对,D错;氧气为正极,电极反应为:O2+4H++4e-=2H2O,A错,C对。
本题难度:一般
3、填空题 (15分)I.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
a、2NO(g)+Cl2(g)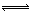 2ClNO(g) ?H1<0 其平衡常数为K1
2ClNO(g) ?H1<0 其平衡常数为K1
b、2NO2(g)+NaCl(s)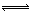 NaNO3(s)+ClNO(g) ?H2<0 其平衡常数为K2
NaNO3(s)+ClNO(g) ?H2<0 其平衡常数为K2
(1)4NO2(g)+2NaCl(s)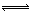 2NaNO3(s)+2NO(g)+Cl2(g) ?H3的平衡常数K= (用K1、K2表示)。?H3= (用?H1、?H2表示)。
2NaNO3(s)+2NO(g)+Cl2(g) ?H3的平衡常数K= (用K1、K2表示)。?H3= (用?H1、?H2表示)。
(2)为研究不同条件对反应a的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应a达到平衡。测得10min内υ(ClNO)=7.5×10-3mol?L-1?min-1,则平衡后n(Cl2)= mol,NO的转化率α1= 。其它条件保持不变,反应(1)在恒压条件下进行,平衡时NO的转化率为α2,α1 α2(填“>”“<”或“=”),平衡常数K1 (填“增大”“减小”或“不变”)。若要使K1减小,可采用的措施是 。
II.第三代混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液.镍氢电池充放电原理示意如图:
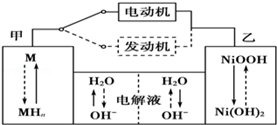
其总反应式为H2+2NiOOH 2Ni(OH)2 。根据所给信息判断,混合动力车上坡或加速时,甲电极周围溶液的pH (填“增大”“减小”或“不变”), 乙电极的电极反应式 。
2Ni(OH)2 。根据所给信息判断,混合动力车上坡或加速时,甲电极周围溶液的pH (填“增大”“减小”或“不变”), 乙电极的电极反应式 。
参考答案:I(1)K22/ K1, 2?H2-?H1 (每空2分)
(2)0.025; 75%; <(每空2分); 不变(1分); 升高温度(1分)
Ⅱ增大(1分), NiOOH+H2O+e
本题解析:
本题难度:困难
4、填空题 (14分)二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放。
1.在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),△H=-akJ・mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),△H=-akJ・mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

①能说明该反应已达平衡状态的是________。
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O
D.反应中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②下列措施中能使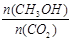 增大的是________(选填编号)。
增大的是________(选填编号)。
A.升高温度
B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离
D.恒温恒容再充入2 mol CO2和3 mol H2
③计算该温度下此反应的平衡常数K=_________。若改变条件 (填选项),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度 D.升高温度 E.加入催化剂
(2)某甲醇燃料电池原理如图1所示。
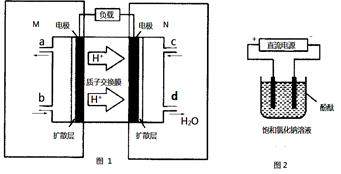
①M区发生反应的电极反应式为______________________ _________。
②用上述电池做电源,用图2装置电解饱和食盐水(电极均为惰性电极),则该电解反应的总反应的离子方程式为: 。假设溶液体积为300mL,当溶液的pH值变为13时(在常温下测定),理论上消耗甲醇的质量为______________(忽略溶液体积变化)。
(3)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-a kJ・mol-1;
CH3OH(g)+H2O(g) △H=-a kJ・mol-1;
CH3OH(g)=CH3OH(l) △H=-b kJ・mol-1;
2H2(g)+O2(g)=2H2O(g) △H=-c kJ・mol-1;
H2O(g)=H2O(l) △H=-d kJ・mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:________________________ _________。
参考答案:(1)①AB ②CD ③0.20或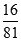 C (2)①CH3OH-6e-+H2O=CO2+6H+
C (2)①CH3OH-6e-+H2O=CO2+6H+
②2Cl-+2H2O H2↑+Cl2↑+2 OH- 0.16g
H2↑+Cl2↑+2 OH- 0.16g
CH3OH(l) + O2(g) =CO2(g) +2H2O(l) ΔH=-(
O2(g) =CO2(g) +2H2O(l) ΔH=-( c+2d-a-b)kJ・mol-1
c+2d-a-b)kJ・mol-1
本题解析:
试题解析:(1)①未平衡CO2的体积分数是个变化的量,现在混合气体CO2的体积分数保持不变,说明已经平衡了,故A正确;未平衡时混合气体的平均相对分子质量是个变化的量,现在不随时间的变化而变化,说明已经达平衡状态,故B正确;单位时间内每消耗1.2mol H2,向正方向,同时生成0.4mol H2O,也向正方向,不能反映正逆反应之间的关系,故C错误;反应中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变,不能说明各自的量不再随时间的变化而变化,故C错误;②升高温度,平衡逆向移动,故比值减小,故A错误;恒温恒容下充入He(g),平衡不移动,故比值不变,故B错误;将H2O(g)从体系中分离,平衡正向移动,故比值变大,故C正确;恒温恒容再充入2mol CO2和3mol H2,相当于增大压强,平衡正向移动,故比值变大,故D正确;
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
初始(mol/L) 1 1.5 0 0
变化(mol/L) 0.25 0.75 0.25 0.25
平衡(mol/L) 0.75 0.75 0.25 0.25
所以: K= =0.20,而平衡常数是温度的函数,只有通过改变温度,来改变平衡常数,正反应量放热反应,降低温度,K值变大;(2)①M区是质子流出的一极,应是原电池的负极,发生氧化反应,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;②用惰性电极,电解饱和食盐水总的电极反应式为2Cl-+2H2O
=0.20,而平衡常数是温度的函数,只有通过改变温度,来改变平衡常数,正反应量放热反应,降低温度,K值变大;(2)①M区是质子流出的一极,应是原电池的负极,发生氧化反应,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;②用惰性电极,电解饱和食盐水总的电极反应式为2Cl-+2H2O H2↑+Cl2↑+2OH-,pH值变为13时,pOH=1,C(OH-)=10-1mol/L,n(OH-)=10-1mol/L×300mL×10-3L/mL=0.03mol,由CH3OH-6e-+H2O=CO2+6H+,2Cl-+2H2O
H2↑+Cl2↑+2OH-,pH值变为13时,pOH=1,C(OH-)=10-1mol/L,n(OH-)=10-1mol/L×300mL×10-3L/mL=0.03mol,由CH3OH-6e-+H2O=CO2+6H+,2Cl-+2H2O H2↑+Cl2↑+2OH-可知:
H2↑+Cl2↑+2OH-可知:
CH3OH ~ 6e- ~ 6OH-
32g 6mol
m(CH3OH) 0.03mol
则m(CH3OH)=32g×0.03mol÷6mol=0.16g;
(3)应用盖斯定律解题,△H=-△H1-△H2+ △H3+2△H4=-(
△H3+2△H4=-( c+2d-a-b)kJ?mol-1,所以CH3OH(l)燃烧热的热化学方程式为CH3OH(l)+
c+2d-a-b)kJ?mol-1,所以CH3OH(l)燃烧热的热化学方程式为CH3OH(l)+ O2(g)=CO2(g)+2H2O(l)△H=-(
O2(g)=CO2(g)+2H2O(l)△H=-( c+2d-a-b)kJ?mol-1。
c+2d-a-b)kJ?mol-1。
考点:化学反应中的能量变化、化学平衡、电化学
本题难度:一般
5、选择题 一种新型燃料电池,它是用两根惰性金属做电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,发生的电极反应为:X极:CH4+10OH--8e-=CO32-+7H2O?Y极:4H2O+2O2+8e-=8OH-关于此燃料电池的下列说法中正确的是( )
A.X极为正极,Y极为负极
B.工作一段时间后,KOH的物质的量不变
C.在标准状况下通入5.6LO2完全反应,则有1.0mol电子发生转移
D.该电池工作时甲烷一极附近溶液的pH升高
参考答案:A、碱性甲烷燃料电池,具有还原性的甲烷为原电池的负极,发生氧化反应,所以X极是负极,通入氧气的一极为原电池的正极,发生还原反应,Y极为正极,故A错误;
B、根据总反应:CH4+2O2+2OH-=CO32-+3H2O,则氢氧化钾被消耗,物质的量减小,故B错误;
C、在标准状况下通入5.6L即0.25molO2完全反应,根据电极反应式:O2+2H2O+4e-=4OH-,转移电子是1.0mol,故C正确;
D、该电池工作时甲烷电极发生的电极反应为:CH4+10OH--8e-=CO32-+7H2O,该极氢氧根被消耗,所以该极附近溶液的pH降低,故D错误.
故选C.
本题解析:
本题难度:简单