1、选择题 下列有关实验操作、现象和解释或结论都正确的是
[? ]
实验操作?
现象
解释或结论
A.
在试管中的无色溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口?
试纸不变蓝
原溶液中无
NH4+
B.
向AgI沉淀中滴入稀KCl溶液?
有白色沉淀出现
Ksp(AgCl)?>Ksp(AgI)
C.
向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热
无红色沉淀生成
淀粉没有水解成葡萄糖
D.
pH均为1的盐酸、醋酸溶液分别用蒸馏水稀释m倍、n倍后测pH值
pH相同
m<n
2、选择题
| 化学式 | 电离常数
(25℃)
HCN
4.9×l0-10
H2CO3
K1=4.3×l0-7
K2=5.6×l0-11
|
根据表中提供的数据,判断下列说法正确的是( )
A.等浓度的NaCN、NaHCO3、Na2CO3溶液中,pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)
B.a?mol/L?HCN溶液与b?mol/L?NaOH溶液等体积混合后,所得溶液中c(Na+)=c(CN-),则a一定大于b
C.等浓度的NaCN、NaHCO3混合溶液中,c(Na+)+c(H+)=c(CN-)+c(HCO3-)+c(OH-)
D.NaCN溶液中通入少量CO2,发生的反应可表示为2NaCN+H2O+CO2→2HCN+Na2CO3
3、选择题 下面关于电解质的叙述正确的是?(?)
A.NaCl溶液能导电,所以NaCl溶液是电解质
B.若某种电解质溶液中含有未电离的分子,则该电解质一定是弱电解质
C.氯气和氨气的水溶液导电性都很好,所以它们是电解质
D.CaCO3在水中溶解度很小,但溶解的 CaCO3全部电离,所以 CaCO3是强电解质
4、选择题 常温下,有关下列4种溶液的说法正确的是
①
| ②
| ③
| ④
|
0.1 mol・L-1氨水
| pH=11氨水
| 0.1 mol・L-1盐酸
| ?pH=3盐酸
|
?
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍,pH与②相同
C.①与③混合,若溶液pH=7,则溶液中c(NH4+)>c(Cl-)
D.②与④等体积混合,混合液pH>7
5、选择题 与纯水的电离相似,液氨中也存在着微弱的电离: 2NH3 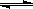 ?NH4++NH2-,据此判断以下叙述中错误的是:
?NH4++NH2-,据此判断以下叙述中错误的是:
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)・C(NH2-)是一个常数
C.液氨的电离到达平衡时C(NH3)=C(NH4+)=C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+)=C(NH2-)