1������� ��֪�����������ת��

�Իش𣺣�1��д��B�Ļ�ѧʽ______��D�Ļ�ѧʽ______��
��2��д����Eת���F�Ļ�ѧ����ʽ______��
��3��д����KSCN����G��Һ�����ӷ���ʽ______��
�ο��𰸣���ɫ����EΪFe��OH��2�����ɫ����FΪFe��OH��3��D��Һ���������ữ�����������ɰ�ɫ����HΪAgCl�����ɵ���Һ�к��м����ӣ�֤��D��ҺΪKCl������ת����ϵ�õ���CΪKOH��BΪFeCl2��F�ܽ������ᣬ˵���������ܽ����ɵ�GΪFeCl3���ж�AΪFe��
��1�������ƶ�B�Ļ�ѧʽΪ��FeCl2��D�Ļ�ѧʽΪ��KCl���ʴ�Ϊ��FeCl2��KCl��
��2��E��Fe��OH��2��ת���F��Fe��OH��3���ķ�Ӧ������������������Ϊ������������Ӧ�Ļ�ѧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3
��3��д����KSCN����G��FeCl3����Һ�����õ������������Ӻ�������������γ�Ѫ��ɫ��Һ����Ӧ�����ӷ���ʽΪ��Fe3++3SCN-=Fe��SCN��3��
�ʴ�Ϊ��Fe3++3SCN-=Fe��SCN��3��
���������
�����Ѷȣ�һ��
2������� A��B��C��DΪ��ѧ��ѧ���������ʣ����Ǽ�ķ�Ӧ��ϵ��ͼ��ʾ��
��1����A�ǿ�����ǿ�B�����Σ�D������ϡ���ᣬ��B�Ļ�ѧʽ______���йط�Ӧ�Ļ�ѧ����ʽΪ______��
��2����B�����Σ�D�ȿ����������ֿ�����NaOH��Һ����A��NaHCO3ʱ���÷�Ӧ�����ӷ���ʽΪ______��
��3����A��̼���ƣ�CaC2����A��B����Һ��Ӧʱֻ��������C��CaCO3��ˮ��C��ȼ����Ϊ1300kJ?mol-1����B�Ļ�ѧʽΪ______��Cȼ�յ��Ȼ�ѧ����ʽΪ______��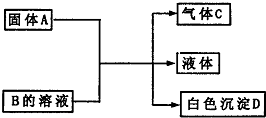
�ο��𰸣���1��ǿ������ι��ȷŰ�������AΪǿ�����BΪ��Σ�����D������ϡ���ᣬ����DΪ���ᱵ����BΪ����泥�AΪ�������������߷�Ӧ����ʽΪ��
Ba��OH��2+��NH4��SO4�TBaSO4+2NH3��+2H2O��
�ʴ�Ϊ����NH4��SO4��Ba��OH��2+��NH4��SO4�TBaSO4+2NH3��+2H2O��
��2��D�ȿ����������ֿ�����NaOH��Һ������֪DΪ����������������A��NaHCO3ʱ��BӦ��Al3+�����߷���˫ˮ�ⷴӦ��
Al3++3HCO3-�TAl��OH��3��+3CO2����
�ʴ�Ϊ��Al3++3HCO3-�TAl��OH��3��+3CO2����
��3����A��̼���ƣ�CaC2����̼���ƣ�CaC2����ˮ��Ӧ�����������ƺ���Ȳ���壨C�����������ƺ�B��Ӧ����̼��ƺ�ˮ�����������غ��֪BΪ̼����ƣ���ѧʽΪ��Ca��HCO3��2��������Ȳ��ȼ���ȿ�д����Ȳȼ�յ��Ȼ�ѧ����ʽ��
C2H2��g��+5/2O2?��g���T2CO2��g��+H2O��l����H=-1300?KJ/mol��
�ʴ�Ϊ��Ca��HCO3��2��C2H2��g��+5/2O2?��g���T2CO2��g��+H2O��l����H=-1300?KJ/mol��
���������
�����Ѷȣ�һ��
3������� ������ѧ��ѧ�г������ʵ�ת����ϵͼ�У���Ӧ���������ַ�Ӧ��Ͳ���δȫ��ע������֪A��DΪ�������ʣ�����Ϊ���������CΪ������������ƶϣ���������ʾ������Al���ڸ����½�һЩ�����������������û�������

��1��д�����ʵĻ�ѧʽ��
A��______?B��______?C��______
��2��д�����з�Ӧ�ķ���ʽ��
C��F�����ӷ�Ӧ����ʽ______H��I�Ļ�ѧ��Ӧ����ʽ______����Ӧ��ʵ������Ϊ______��D�������ϡ���ᷴӦ�����ӷ�Ӧ����ʽ______��
�ο��𰸣�CΪ���������ӦΪAl2O3������ɫ��ĩBΪFe2O3����A��B�ķ�ӦӦΪ���ȷ�Ӧ��AΪAl��DΪFe�������ᷴӦ����Fe2+��������Ӧ����Fe��OH��2�����Լ���Ϊ�ᣬ�Լ���Ϊ���IΪFe��OH��3��EΪ���Σ�FΪƫ�����Σ�
��1�������Ϸ�����֪AΪAl��BΪFe2O3��CΪAl2O3���ʴ�Ϊ��Al��Fe2O3��Al2O3��
��2��C��F�ķ�ӦΪAl2O3+2OH-=2AlO2-+H2O��H��I�Ļ�ѧ��Ӧ����ʽΪ4Fe��OH��2+O2+2H2O=4Fe��OH��3����Ӧ��ʵ������Ϊ��ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��D�������ϡ���ᷴӦ�����ӷ�Ӧ����ʽFe+4H++NO3-=Fe3++NO��+2H2O��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��4Fe��OH��2+O2+2H2O=4Fe��OH��3����ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��Fe+4H++NO3-=Fe3++NO��+2H2O��
���������
�����Ѷȣ�һ��
4������� ͼ��B��FΪ���ʣ�����Ϊ���������֮���������ת����ϵ�����ַ�Ӧ������P��Ӧ��������ȥ�������У�A��C�ǹ�ҵ����;�ܹ��������Ҫ����ԭ�ϣ�C����ɫ��ӦΪ��ɫ��BΪ�ճ������г����Ľ�����H��G���Ӿ�������������ṹ��H��һ����Ҫ����Դ��J��һ�ֽϺõ��ͻ���ϣ�K�Ǽ�������ˮ�ļ������壬��ش��������⣺
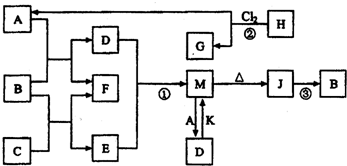
��1��C�д��ڵĻ�ѧ������Ϊ______��G�ĵ���ʽΪ______��
��2����Ӧ�ڽ��е�����______��
��3����Ӧ�ٵ����ӷ���ʽΪ______��
��Ӧ�۵Ļ�ѧ����ʽΪΪ______��
��4����D��Һ��ͨ��K������M����һ������X��д������X�������ӵ�ʵ�鷽��������Ϊ______��
��5������ȵ�ԭ������֮��Ϊ36��������131��ԭ�Ӻ���������Ϊ______������Ԫ�����ڱ��е�λ��Ϊ______��
��6���ҹ��״��ĺ�������B����Ϊ����������Ϊ��������ˮΪ�������Һ�������е�������B��Ӧ�����������õ�ص�������ӦʽΪ______��
�ο��𰸣�H��G���Ӿ�������������ṹ��H��һ����Ҫ����Դ����H�Ǽ��飬G��CCl4��AΪHCl��BΪ�ճ������г����Ľ����������B��Ӧ�����κ�������F�ǵ��ʣ�����F��������A��C�ǹ�ҵ����;�ܹ��������Ҫ����ԭ�ϣ�C����ɫ��ӦΪ��ɫ������C�к�����Ԫ�أ�����B�ܺ����ᷴӦҲ�ܺ��ƵĻ����ﷴӦ������������B������C���������ƣ�D���Ȼ�����E��ƫ�����ƣ��Ȼ�����ƫ�����Ʒ�Ӧ���������������Ȼ��ƣ�M�ܼ�������J������M������������J��һ�ֽϺõ��ͻ���ϣ�J����������K�Ǽ�������ˮ�ļ������壬��K�ǰ�����
��1��C���������ƣ������Ӻ�����������֮��������Ӽ�����ԭ�Ӻ���ԭ��֮����ڹ��ۼ���G��CCl4�������ʽΪ��

���ʴ�Ϊ�����Ӽ������ۼ���

��
��2��������������ڹ��������·���ȡ����Ӧ�������Ȼ�̼���ʴ�Ϊ�����ա�����Cl2��
��3���Ȼ�����ƫ�����Ʒ�Ӧ���������������Ȼ��ƣ����ӷ���ʽΪ��Al3++3AlO2-+6H2O=4Al��OH��3�����������̬����������ұ������ͬʱ������������Ӧ����ʽΪ��2Al2O3�����ڣ�?���?.����ʯ4Al+3O2����
�ʴ�Ϊ��Al3++3AlO2-+6H2O=4Al��OH��3����2Al2O3�����ڣ�?���?.����ʯ4Al+3O2����
��4���Ȼ����Ͱ�ˮ��Ӧ���������������Ȼ�泥�Ҫ����笠����ӣ�����笠����ӵ���Һ�м�������Լͬʱ���ȣ�����ɫʯ����ֽ���鰱���Ĵ��ڣ�������ʹ��ɫʯ����ֽ��죬
�ʴ�Ϊ��ȡ����X��Һ���Թ��У��ý�ͷ�ιܵ���NaOH��Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿڣ������Թܣ��ɹ۲쵽��ɫʯ����ֽ������
��5������ȵ�ԭ������֮��Ϊ36������ԭ������=17+36=63��������131��ԭ�Ӻ���������=131-53=78����λ�ڵ������ڵڢ�A�壬�ʴ�Ϊ��78����5���ڵڢ�A�壻
��6�������������õ��ӷ�����ԭ��Ӧ��ͬʱ�������������ӣ��缫��ӦʽΪ��O2+2H2O+4e-=4OH-����3O2+6H2O+12e-=12OH-�����ʴ�Ϊ��O2+2H2O+4e-=4OH-����3O2+6H2O+12e-=12OH-����
���������
�����Ѷȣ�һ��
5���ƶ��� ��A���ܱ������м��ȵ����ʵ�����ȵ�B��C��D��E�������壬����ȴ������һ���¶�ʱ�������о�������X���ɣ���ʱԭ4��������ֻ��Bû�вμӷ�Ӧ��������ͬ������B������������ܶ�Ϊ14�����ж����塣�й����ʵ�ת����ϵ����ͼ������E�ڳ�����Ϊ��ɫҺ�壬GΪ����ɫ���壬X��F��һ�ֳ����ĵ��ʡ���Ӧ����n(C):n(D)=2 :1����Ӧ�٢ڢۢ��ڹ�ҵ�����о�����ҪӦ�ã�ͼ�в��ַ�Ӧ����������δע�����Իش���������
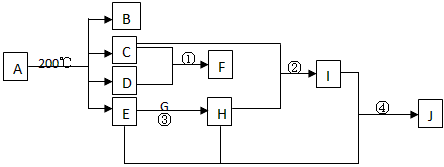
(1)A�Ļ�ѧʽ__________�� C�ĵ���ʽ__________��D�Ľṹʽ__________��
(2)д����ѧ��Ӧ����ʽ��____________________��
(3)д��J��ϡ��Һ�����ͭ�����ӷ�Ӧ����ʽ____________________��
�ο��𰸣�(1)NH4HC2O4��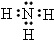 ��
��
(2)4NH3+5O2 4NO+6H2O
4NO+6H2O
(3)3Cu+8H++2NO3-�T�T3Cu2++2NO��+4H2O
���������
�����Ѷȣ�һ��