1、选择题 下列表示正确的是?
A.CO2的比例模型:
B. H2O2的电子式: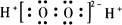
C.NH4+ 的结构式: 
D.14C的原子结构示意图: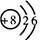
参考答案:A
本题解析:H2O2是共价化合物,电子式为共用电子,不带电荷,B错;NH4+带一个单位正电荷,其结构式应标出,并加一中括号,C错;14C的原子核由6个质子和8个中子构成,原子结构示意图为 ,D错误。
,D错误。
点评:对化学用语的考查是高考必考知识点,难度不大,考生在平时的学习过程中应注意化学用语的规范使用。
本题难度:一般
2、选择题 下列化学用语表达正确的是(? )
A.一氯甲烷的结构式CH3Cl
B.丁烷的结构简式CH3(CH2)2CH3
C.四氯化碳的电子式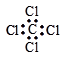
D.苯的分子式
参考答案:B
本题解析:A不正确,一氯甲烷的结构式应该是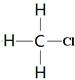 ;C不正确,四氯化碳的电子式是
;C不正确,四氯化碳的电子式是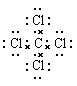 ;苯的分子式是C6H6,答案选B。
;苯的分子式是C6H6,答案选B。
点评:该题是中等难度的试题,也是高考中的常见题型与重要的考点。该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度。该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等,需要学生熟练记住,并能灵活运用。
本题难度:简单
3、填空题 硫酸工厂的烟气中含有SO2,有多种方法可实现烟气脱硫。
(1)工业制硫酸的过程中,SO2被氧气氧化的化学方程式为?。
(2)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。
已知:25℃时,H2SO3  ?HSO3 -+H+?K=1.5×10-2
?HSO3 -+H+?K=1.5×10-2
H2CO3 HCO3 -+H+?K=4.4×10-7
HCO3 -+H+?K=4.4×10-7
下列试剂中适合用作该法吸收剂的是?(填字母序号)。
a.石灰乳?b. Na2SO3溶液?c. Na2CO3溶液?
②“钠碱法”用NaOH溶液作吸收剂,向100 mL 0.2 mol・L-1的NaOH溶液中通入标准状况下0.448 L SO2气体,反应后测得溶液pH<7,则溶液中下列各离子浓度关系正确的是?(填字母序号)。
a.c(HSO3-)> c(SO32-)> c(H2SO3)
b.c(Na+)>c(HSO3-)> c(H+)> c(SO32-)
c.c(Na+)+c(H+)= c(HSO3-)+c(SO32-)+c(OH-)
(3)某硫酸厂拟用烟气处理含Cr2O72-的酸性废水,在脱硫的同时制备Cr2O3产品。具体流程如下:
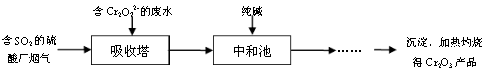
①吸收塔中反应后的铬元素以Cr3+形式存在,则其中发生反应的离子方程式为?。?
②中和池中的反应除生成Cr(OH)3沉淀外,还会产生某种气体,该气体的化学式为?。
参考答案:(1)2SO2+O2 2SO3(2分,写“高温”不扣分,既不写条件也不写可逆号的只扣1分)
2SO3(2分,写“高温”不扣分,既不写条件也不写可逆号的只扣1分)
(2)①a、b、c(2分,只选一个为0分,选两个给1分)
②a、b(2分,只选对一个为1分,选对一个选错一个为0分)
(3)①Cr2O72-+2H++3SO2=2Cr3++3SO42-+H2O(2分)?②CO2(1分)
本题解析:(1)SO2被氧气氧化生成SO3,化学方程式为:2SO2+O2 2SO3
2SO3
(2)①SO2可以分别与Ca(OH)2、Na2SO3、Na2CO3反应,所以a、b、c项都可以用来吸收SO2。
②NaOH为0.02mol,SO2为0.02mol,二者恰好生成NaHSO3,因为HSO3?的电离程度大于水解程度,所以 c(HSO3-)> c(SO32-)> c(H2SO3),a项正确;HSO3?和H2O电离都可生成H+,所以 c(Na+)>c(HSO3-)> c(H+)> c(SO32-),故b项正确;根据电荷守恒可知: c(Na+)+c(H+)= c(HSO3-) +2 c(SO32-)+c(OH-),故c项错误。
(3)①Cr2O72?具有强氧化性,能氧化SO2,离子方程式为:Cr2O72-+2H++3SO2=2Cr3++3SO42-+H2O
②CO32?与Cr3+发生水解反应,除了生成Cr(OH)3,另外生成的气体为CO2。
本题难度:困难
4、推断题 硫酸的工业制备是一个重要的化工生产过程,但在生产过程中会产生大量污染,需要在生产工艺中考虑到绿色工艺。
I尾气的吸收和综合利用。
以工业制硫酸的尾气、氨水、石灰石、焦炭、碳酸氯铵和KCI为原料可以合成硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
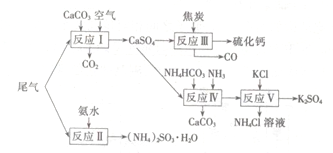
(1)反应III中氧化剂与还原剂的物质的量之比为 。
(2)反应Ⅳ的化学方程式为 。
(3)反应V在25℃、40%的乙二醇溶液中进行,该反应能顺利进行的原因为 。
Ⅱ催化剂的回收利用。
SO2的催化氧化所使用的催化剂为V2O5,实际生产中,催化剂在使用一段时间后,会含有V2O5、VOSO4和SiO2等,其中VOSO4。能溶于水。回收V2O5,的主要流程如下:

(4)若反萃取使用的硫酸用量过大,进一步处理时会增加____ 的用量。
(5)浸取还原过程的产物之一是VOSO4,反应的化学方程式为 。
氧化过程的化学方程式为KClO3+6VOSO4+3H2SO4= 2(VO)2(SO4)3+KCl+3H2O;若两步所用试剂Na2SO3与KC1O3的物质的量之比为12:7,则该催化剂中V2O5、VOSO4的物质的量之比为 。
参考答案:(1)1
本题解析:
本题难度:一般
5、选择题 加热下列各物质,发生氧化还原反应的是
A.NH4Cl
B.NH4HCO3
C.浓盐酸
D.浓硝酸
参考答案:D
本题解析:略
本题难度:简单