1、选择题 标准状况下,VL氨气溶解在1L水中(水的密度近似为1g/mL)所得溶液的密度为ρg/mL质量分数为ω,物质的量浓度为cmol/L,则下列关系中不正确的是
A.c=
B.ω=
C.ω=
D.c=
参考答案:D
本题解析:分析:A.根据c=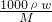 计算判断;
计算判断;
B.根据c=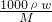 的公式变形计算ω;
的公式变形计算ω;
C.根据n=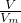 计算VL氨气的物质的量,根据m=nM计算氨气的质量,根据m=ρV计算水的质量,进而计算溶液的质量,溶液质量分数=
计算VL氨气的物质的量,根据m=nM计算氨气的质量,根据m=ρV计算水的质量,进而计算溶液的质量,溶液质量分数=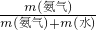 ×100%;
×100%;
D.根据n=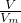 计算VL氨气的物质的量,根据m=nM计算氨气的质量,根据m=ρV计算水的质量,进而计算溶液的质量,根据V=
计算VL氨气的物质的量,根据m=nM计算氨气的质量,根据m=ρV计算水的质量,进而计算溶液的质量,根据V=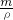 计算溶液的体积,再利用c=
计算溶液的体积,再利用c= 计算.
计算.
解答:A、ρg/mL质量分数为ω氨水,其物质的量浓度c=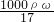 mol/L,故A正确;
mol/L,故A正确;
B、根据c=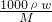 可知,该氨水质量分数w=
可知,该氨水质量分数w=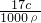 ,故B正确;
,故B正确;
C.VL氨气的物质的量为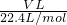 =
=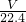 mol,氨气质量为
mol,氨气质量为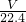 mol×17g/mol=
mol×17g/mol=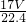 g,1L水的质量为1000mL×1g/mL=1000g,故溶液质量为(
g,1L水的质量为1000mL×1g/mL=1000g,故溶液质量为(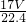 +1000)g,所以溶液的质量分数w=
+1000)g,所以溶液的质量分数w=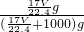 ×100%=
×100%=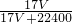 ×100%,故C正确;
×100%,故C正确;
D.VL氨气的物质的量为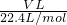 =
=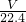 mol,氨气质量为
mol,氨气质量为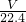 mol×17g/mol=
mol×17g/mol=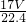 g,1L水的质量为1000mL×1g/mL=1000g,故溶液质量为(
g,1L水的质量为1000mL×1g/mL=1000g,故溶液质量为(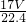 +1000)g,溶液体积为
+1000)g,溶液体积为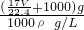 =
=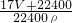 L,所以物质的量浓度c=
L,所以物质的量浓度c=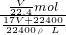 =
=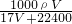 mol/L,故D错误;
mol/L,故D错误;
故选D.
点评:本题考查物质的量浓度、质量分数的有关计算及二者的关系,难度中等,注意对概念的理解与公式的灵活运用.
本题难度:一般
2、选择题 2mol?Cl2与足量的元素A单质完全反应生成1mol?AClX,则x值为
A.1
B.2
C.3
D.4
参考答案:D
本题解析:分析:根据Cl原子守恒计算AClX中x的值,据此判断.
解答:2mol?Cl2与足量的元素A单质完全反应生成1mol?AClX,氯气完全反应,氯元素全部转移到AClX,中,所以由Cl原子守恒可知:2mol×2=1mol×x,
解得x=4,
故选D.
点评:本题考查质量守恒定律的微观意义,难度较小,关键在于氯气完全反应,理解质量守恒定律的宏观意义与微观意义.
本题难度:一般
3、选择题 下列物质不能用氯气与单质直接化合制取的是
A.AlCl3
B.FeCl2
C.HCl
D.CuCl2
参考答案:B
本题解析:分析:根据Cl2有强氧化性,当与变价金属反应时将金属氧化成高价态来回答.
解答:A、因Cl2有强氧化性,与金属反应化合生成相应的盐(氯化物),当与金属铝反应时将金属氧化成氯化铝,能用氯气与单质直接化合制取,故A错误;
B、当氯气与变价金属Fe反应会生成FeCl3,不能用氯气与单质直接化合制取,故B正确;
C、氢气可以在氯气中燃烧生成氯化氢,能用氯气与单质直接化合制取,故C错误;
D、因Cl2有强氧化性,与金属反应化合生成相应的盐(氯化物),当与金属Cu反应时将金属氧化成氯化成高价Cu即氯化铜,能用氯气与单质直接化合制取,故D错误.
故选:B.
点评:Cl2是卤族元素的代表,有强氧化性,当与变价金属反应时将金属氧化成高价态.
本题难度:困难
4、选择题 1molN2和44gCO2的气体体积,前者和后者的关系是
A.大于
B.等于
C.小于
D.不能确定
参考答案:D
本题解析:分析:气体的体积和气体的物质的量的多少以及所处的温度压强有关.
解答:根据物质的量和气体体积的关系公式V=nVm可知,要计算1molN2和44gCO2的气体体积,还须知道二者的Vm的大小,而Vm的大小和气体所处的温度压强有关,故不能确定体积的大小.
故选D.
点评:本题考查学生对公式V=nVm的理解和掌握,考查学生分析和解决问题的能力,难度不大.
本题难度:简单
5、选择题 氟氯烃对大气臭氧层有破坏作用。据报道南极上空的臭氧空洞已有三个中国的面积!科学家们呼吁人类要保护臭氧层。大气层中,臭氧的作用是
A.吸收CO2
B.补充O2
C.吸收红外线
D.吸收紫外线
参考答案:D
本题解析:试题分析:本题主要考查大气层中臭氧的作用:吸收紫外线。臭氧层的主要作用是吸收紫外线,防止紫外线的直接照射,对人体以及地球上的各种生物造成威胁。因为紫外线具有强烈的辐射作用。
考点:考查臭氧的作用。
点评:本题从氟氯烃对臭氧层的破坏出发,旨在引导学生加强环保意识,同时也体现了化学与生活息息相关。
本题难度:一般