1、选择题 在标准状况下,称量一个充满氯气的容器质量为74.6克,若改充氮气,其质量为66克,则容器的容积为
A.11.2L
B.5.6L
C.4.48L
D.2.24L
参考答案:C
本题解析:分析:氯气的体积与氮气体积相等,等于容器的容积.相同条件下,体积之比等于物质的量之比,所以氯气与氮气的物质的量相等.
假设气体的物质的量为n,容器的质量为m,根据不同气体的质量,列方程进行相关计算n值,再根据v=nVm计算.
解答:假设气体的物质的量为nmol,容器的质量为mg,则:
mg+nmol×71g/mol=74.6g
mg+nmol×28g/mol=66g
联立方程,解得n=0.2mol
气体的体积为V=0.2mol×22.4L/mol=4.48L.
所以容器的容积为4.48L.
故选C.
点评:本题考查阿伏伽德罗定律及推论,难度不大,氯气的体积等于氮气体积等于容器的体积,是解题的关键.
本题难度:简单
2、选择题 今有0.1mol.L-1 Na2SO4溶液300ml, 0.1mol.L-1 MgSO4溶液200ml和0.1mol.L-1 Al2(SO4)3溶液100ml,这三种溶液中硫酸根离子的浓度之比是
A.1:1:1
B.3:2:2
C.3:2:3
D.1:1:3
参考答案:D
本题解析:试题分析:0.1mol.L-1 Na2SO4溶液中硫酸根离子的浓度为0.1mol.L-1; 0.1mol.L-1 MgSO4溶液中硫酸根离子的浓度为0.1mol.L-1;0.1mol.L-1 Al2(SO4)3溶液中硫酸根离子的浓度为0.3mol.L-1;因此这三种溶液中硫酸根离子的浓度之比为1:1:3,答案选D。
考点:物质的量浓度的计算
点评:本题是对“物质的量浓度的计算”的简单考查,在对物质中离子浓度的计算时,要特别注意构成物质的离子数目。
本题难度:简单
3、选择题 p克某结晶水合物A?nH2O,受热失去全部结晶水后,质量变为q克,由此可以得知该结晶水合物的相对分子质量为
A.
B.
C.
D.
参考答案:A
本题解析:分析:据物质的化学式,利用组成中整体与部分组成的相对分子质量之比等于质量之比来解答.
解答:设结晶水合物A?nH20的相对分子质量为x,
结晶水合物的质量为P克,受热失去全部结晶水后,质量为q克,
则水的质量为(P-q)克,
则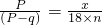 ,解得x=
,解得x=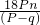 ,
,
故选A.
点评:本题考查学生利用物质的化学式及物质中的组成来计算物质的相对分子质量,明确组成中质量的关系是解答的关键.
本题难度:困难
4、选择题 在一密闭容器中,盛放A、B、C三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下:
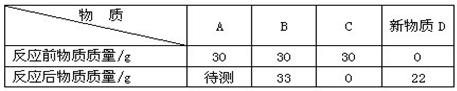
关于此反应,下列认识不正确的是
A.C物质中所含有的元素种类是A、B、D三种物质中所有元素种类之和
B.变化后待测的A质量为5g
C.变化后生成B物质3g
D.C物质一定是化合物
参考答案:B
本题解析:分析:生成物的质量增加,反应物的质量减少,由表中各物质的质量变化可知C为反应物,B、D为生成物.
参加反应的C的质量为30g,生成的D的质量为22g,生成的B的质量为33g-30g=3g.
根据质量守恒定律可知,A为生成物,生成的A的质量为30g-22g-3g=5g.
所以反应为分解反应,该反应可表示为C→A+B+D.
解答:由物质的质量变化可知C为反应物,B、D为生成物,参加反应的C的质量为30g,生成的D的质量为22g,生成的B的质量为33g-30g=3g.根据质量守恒定律可知,A为生成物,生成的A的质量为30g-22g-3g=5g.所以反应为分解反应,该反应可表示为C→A+B+D.
A、该反应为分解反应,根据化学变化前后元素的种类不变,可判断分解反应的反应物C中所含元素应是生成物A、B、D三种物质中所有元素种类之和,故A正确;
B、A为生成物,生成的A的质量为30g-22g-3g=5g,所以变化后待测的A质量为30g+5g=35g,故B错误;
C、由表中数据可知,生成的B的质量为33g-30g=3g,故C正确;
D、物质C由A、B、D三种物质化合生成,则C物质一定是化合物,故D正确.
故选:B.
点评:考查质量守恒定律,难度不大,根据物质的质量变化判断反应物与生成物,根据质量守恒判断A是生成物是解题的关键.
本题难度:一般
5、选择题 把4.6g钠投入到95.6g水中,不考虑水的蒸发,所得溶液中溶质的质量分数是
A.4.6%
B.7.7%
C.8.0%
D.10%
参考答案:C
本题解析:试题分析:4.6g钠的物质的量是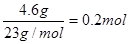 ,根据方程式2Na+2H2O=2NaOH+H2↑可知,生成的氢氧化钠是0.2mol,氢气是0.1mol。所以根据质量守恒定律可知反应后溶液的质量是4.6g+95.6g-0.1mol×2g/mol=100g,因此所得溶液中溶质的质量分数是
,根据方程式2Na+2H2O=2NaOH+H2↑可知,生成的氢氧化钠是0.2mol,氢气是0.1mol。所以根据质量守恒定律可知反应后溶液的质量是4.6g+95.6g-0.1mol×2g/mol=100g,因此所得溶液中溶质的质量分数是 ,答案选C。
,答案选C。
考点:考查溶液质量分数的有关计算
点评:该题属于基础性试题,难度不大。解题的关键是准确溶液中的溶质以及溶液的质量。
本题难度:一般