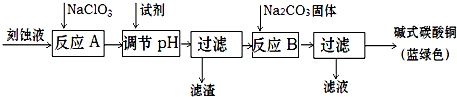
1������� ��ʽ̼��ͭ��һ����;�㷺�Ļ���ԭ�ϣ���ҵ�Ͽ������Կ�ʴ��Һ����Ҫ����Cu2+��Fe2+��Fe3+��H+��Cl-���Ʊ������Ʊ��������£�
Cu2+��Fe2+��Fe3+���ɳ�����pH���£�
| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3
��ʼ����pH
4.2
5.8
1.2
��ȫ����pH
6.7
8.3
3.2
|
��1����������Ҫ�ɷ���______��д��ѧʽ����
��2�����ڷ�ӦA����Һ��pH��ΧӦΪ______��ѡ����Լ�����ʵ���______������ţ���
a����ˮb��ϡ����c����������d��̼��ͭ
��3����ӦB���¶�����ߣ�����������ɫ��Ʒ�п��ܻ���ֵ�������______��
��4����Na2CO3��Һ���뵽һ����CuCl2��Һ�еõ�����������Ӧ�����ӷ���ʽ��ʾ��
�ٳ���ֻ��CuCO3��______��
�ڳ���ֻ��Cu��OH��2�ҷų����ݣ�______��
��5����ʽ̼��ͭ����ɿɱ�ʾΪ��aCuCO3?bCu��OH��2?cH2O��Ҫ�ⶨ����ɣ���ͬѧ��Ƶ�ʵ�鷽������Ҫ����������裺�ٳ�����Ʒ���������ڸ��·ֽ⣻�۲��CO2���������ܲ��ˮ�������������ݳ���CuO������������ͬѧ��Ϊ��������⣬ʵ��ֻ��ⶨ�ĸ����е��������ɣ�����������Ϊ______������ţ�дһ�鼴�ɣ���
�ο��𰸣�������ͼ��֪����ʴ��Һ����NaClO3��Fe2+����ΪFe3+������pH���������ӣ�����ΪFe��OH��3����CuCl2��Һ�м���̼���ƹ��壬���˵õ���ʽ̼��ͭ��
��1������Ϊ��������ȫ�����õ������������������ʴ�Ϊ��Fe��OH��3��
��2������pHʹ�������ӳ�����ȫ����ͭ���Ӳ��ܿ�ʼ���������ڷ�ӦA����Һ��pH��ΧӦΪ3.2-4.2����ˮ�������ƾ������������ӣ����������ʹpH���ߣ�Ϊ�˲��������ʣ�����ʵļ���������̼��ͭ��
�ʴ�Ϊ��3.2-4.2��d��
��3����ӦB���¶�����ߣ�̼��ͭ������ͭ�������ȷֽ���������ͭ���ʴ�Ϊ��CuO��
��4����Na2CO3��Һ���뵽һ����CuCl2��Һ�еõ�������Cu2+��CO32-����CuCO3���������ӷ���ʽΪ��Cu2++CO32-=CuCO3����Cu2+��CO32-��ˮ��Ӧ����Cu��OH��2�����Ͷ�����̼�����ӷ���ʽΪ��Cu2++CO32-+H2O=Cu��OH��2��+CO2����
�ʴ�Ϊ����Cu2++CO32-=CuCO3������Cu2++CO32-+H2O=Cu��OH��2��+CO2����
��5����ʽ̼��ͭ����ɿɱ�ʾΪ��aCuCO3?bCu��OH��2?cH2O���ֽ��������������ɣ�������̼��CuO��ˮ��Ҫ�ⶨ����ɣ�����ٳ�����Ʒ����������֪��������۲��CO2�������ܲ��ˮ�����������ݳ���CuO��������������֪�����е������������ɣ���һ���ֵ����ݿ�����Ʒ����������֪�����ֵ�������ã�
�ʴ�Ϊ���٢ۢܣ���٢ۢݡ��٢ܢݣ���
���������
�����Ѷȣ�һ��
2��ѡ���� ϡ�����м���ͭƬ���������ټ�������ij���ʺ�ͭƬ���ܽ⣬������Ϊ��������
A��KNO3
B��NaCl
C��FeCl3
D��Cu��OH��2
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
3��ѡ���� �ֱ��������ʣ�������?��Na2O2?��NaCl?��Ca(HCO3)2?��FeCl3Ͷ��ˮ�У�������Һ�������ɣ����ܵõ�ԭ���ʵ���
[? ]
A���٢ڢ�
B���٢�
C���ۢ�
D����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ijͭ��ʯ������ͭ��������ͭ�������������ʹ�����ʯ��SiO2�����ֲ���������ӿ�ʯ����ȡͭ��������ͼ���£�

��֪���ٵ���ʯ����������������̫��ʱ������������������Ļ��Һ����ͭ���ڷ���ȡ���ˮ��������ͭ��Һ��Cu2+Ũ��ԼΪ50g/L���ش��������⣺
��1����ʯ��ϡ�������������������ͭ�����ķ�ӦΪ��Cu2O+2H+�TCu2++Cu+H2O����д���ù����з�������һ��������ԭ��Ӧ�����ӷ���ʽ��______��
��2����ȡ��A��һ�����Ϊ�����л��������N-510��N-530�ȣ�ij������A�ķ��ӽṹ�н���n1��-CH3��n2��-OH?��n3��
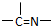
���ֻ��ţ���״�ṹ�����ֻ��ŵ���Ŀ��ϵΪn3=______����A����Է�������Ϊ116�����ӽṹ��̼ԭ�Ӹ�̼ԭ�������ӣ���A�Ľṹ��ʽ��______��
��3��д�������������������Ե缫��������Ӧ�ĵ缫��Ӧʽ��______��
��4��ѭ���з���ȡ��B����Ҫ�ɷ���______��
��5��ijͭ��ʯ��Ʒ�У�������������ͭ����������������ʯ�������ʣ�ȡ�ÿ�ʯ��Ʒ200.0g����100mL1.0mol?L-1H2SO4��Һ��ȡ�������10mL?1.0mol?L-1?Fe2��SO4��3��Һ����ʹͭȫ����������ȡҺ����ֵ���ɵõ�?6.4gCu����ͭ��ʯ��Ʒ��������ͭ��������������������
�ο��𰸣���1����ʯ��ϡ�������������������ͭ�����ķ�ӦΪ��Cu2O+2H+�TCu2++Cu+H2O������ͭ��������֮�䷢��������ԭ��Ӧ����Ӧ�����ӷ���ʽΪ��Cu+2Fe3+�T2Fe2++Cu2+��
�ʴ�Ϊ����Cu+2Fe3+�T2Fe2++Cu2+��
��2��-CH3��-OH�Ƕ�ͷ����
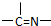
? �Ƿ��ӵĹǼܣ�һ��
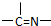
�����һ����ͷ������������β��������ͷ���������ͷ��n3+2����n3+2=n1+n2��n3=n1+n2-2��?
���ݷ����жϳ���ȡ��������A����Է�������Ϊ116�����ӽṹ��̼ԭ�Ӹ�̼ԭ�������ӣ��õ��ṹ��ʽΪ��CH3-C��=N-OH��-C��=N-OH��-CH3��
�ʴ�Ϊ��n1+n2-2��CH3-C��=N-OH��-C��=N-OH��-CH3��
��3�������������������Ե缫���ŵ��������������ʧ��������������������Ӧ�ĵ缫��Ӧʽ��4OH--4e-�TO2��+2H2O��
�ʴ�Ϊ��4OH--4e-�TO2��+2H2O��
��4������ȡ���ˮ��������ͭ��Һ���ɵ��֪�������ᣬ����ѭ���з���ȡ��B�����
�ʴ�Ϊ��H2SO4��
��5��ȡ�ÿ�ʯ��Ʒ200.0g����100mL1.0mol?L-1H2SO4��Һ��ȡ�������10mL?1.0mol?L-1?Fe2��SO4��3��Һ����ʹͭȫ����������ȡҺ����ֵ���ɵõ�?6.4gCu��
����ͭԪ���غ�������ͭ�е�ͭԪ���������ͭ��ͭCu���ʵ���=6.4g64g/mol=0.1mol��������ͭ���ʵ���Ϊ0.05mol������Ϊ0.05mol��144g/mol=7.2g��
Cu2O%=7.2g200g��100%=3.6%������������ԭ��Ӧ�����غ�Fe3+��Cu+��Cu����õ���n��Fe3+��=0.1mol��ԭ��Ʒ����Ԫ�����ʵ���Ϊ=0.1mol-0.02mol=0.08mol��
����Fe2O3���ʵ���Ϊ��0.04mol����������=0.04mol��160g/mol200g��100%=3.2%��
�ʴ�Ϊ��Cu2O��3.6%��?Fe2O3��3.2%��
���������
�����Ѷȣ�һ��
5������� 1.�������м�����������ʵķ��뷽����������ں����ϡ� A������ B������ C���ᾧ D����Һ
��1������ˮ�����Ȼ�̼�Ļ���____________��
��2������ɳ���뱥��ʳ��ˮ�Ļ���________��
��3��������غ��Ȼ��صĻ��Һ�л������أ�_________��
��4���������Ȼ�̼���е�76.75�棩�ͼױ����е�110.6�棩�Ļ����____________��
2.������Fe��Cu��FeCl3��FeCl2��CuCl2��Һһ��Ž�ij�����ڣ�����������ͬ�������д������������ӣ�
��1����ַ�Ӧ�����Fe��ʣ�࣬�������ڲ������У�_____________________��
��2����ַ�Ӧ������������н϶�Cu2+��Cu���������ڲ�������___________��
�ο��𰸣�1.��1��D ����2��A����3��C����4��B��
2.��1����������Cu2+��Fe3+����2����������Fe��Fe3+��
���������
�����Ѷȣ�һ��