1、计算题 A、B两种金属元素的相对原子质量之比是8∶9,将两种金属单质按物质的量之比3∶2组成混合物1.26 g,跟足量稀硫酸反应,放出氢气1.344 L(标准状况),这两种金属单质在反应中生成氢气的体积相等,则A的摩尔质量和B的摩尔质量各是多少?
参考答案:24 g・mol-1 27 g・mol-1
本题解析: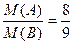 ,
,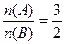 ,提示:A、B与酸反应放出H2。n(H2)=
,提示:A、B与酸反应放出H2。n(H2)=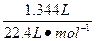 =?0.06 mol,可知A、B各放出0.03 mol H2。
=?0.06 mol,可知A、B各放出0.03 mol H2。
则A为+2价,B为+3价,
n(A)="0.03" mol n(B)="0.02" mol,
所以M(A)・0.03 mol+M(B)・0.02 mol="1.26" g
故M(A)="24" g・mol-1,M(B)="27" g・mol-1。
本题难度:简单
2、选择题 用NA表示阿伏加德罗常数的值,下列叙述正确的是(?)
A.64g SO2含有氧原子数为NA
B.0.5mol/L MgCl2溶液,含有Cl-离子数为NA
C.标准状况下,22.4L H2O的分子数为NA
D.常温常压下,14g N2含有分子数为0.5NA
参考答案:D
本题解析:A、64g SO2含有氧原子数为2NA,错误;B、溶液的体积不确定,因此不能确定其物质的量,错误;C、标况下,水是液体,错误;D、正确。
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的值,下列叙述不正确的(?)
A.10g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA
B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA
C.50 mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA
D.常温常压下,46g NO2 与N2O4的混合气体中含有的原子总数为3NA
参考答案:C
本题解析:A.乙醇溶液中含有乙醇分子的质量为10g×46%=4.6g,n(C2H6O)=4.6g÷46g/mol=0.1mol.所以含氢原子数是0.1mol×6NA=0.6 NA。正确。B.5.6 g铁与0.1 mol氯气充分反应,氯气不足量,转移电子数为 0.2NA。正确。C.二氧化锰只与浓盐酸发生反应,随着反应的进行,盐酸溶液变稀,反应就不再进行。转移电子数小于0.3 NA,错误。D.46g NO2含有的原子数是46g÷46g/mol×3=3NA; 46g N2O4含有的原子数是46g÷92g/mol×6=3NA。正确。
本题难度:一般
4、选择题 在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比8:1:2,则溶液中Na2SO4、NaCl、NaOH个数比为(?)
A.1:1:1
B.1:4:2
C.1:2:4
D.1:3:2
参考答案:B
本题解析:设Na+、SO42-、OH-物质的量分别为8mol、1mol、2mol,由电荷守恒得Cl-物质的量为4mol。所以硫酸钠、氯化钠、氢氧化钠物质的量分别为1mol、4mol、2mol。
点评:本题关键是理解溶液中含有四种离子:Na+、SO42-、Cl-、OH-,根据电荷守恒可快速计算出Cl-物质的量。
本题难度:一般
5、选择题 下列四个图中,白球代表氢原子,黑球代表氦原子,表示等质量的氢气与氦气混合的是
[? ]
A. 
B. 
C. 
D. 
参考答案:B
本题解析:
本题难度:简单