1、选择题 实现下列反应需加入氧化剂的是( )
A.NaOH→NaCl
B.H2SO4→H2
C.HCl→Cl2
D.CaCO3→CO2
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列叙述错误的是( )
A.元素的单质可由氧化或还原含该元素的化合物来制得
B.失电子越多的还原剂,其还原性就越强
C.阳离子只能得到电子被还原,只能作氧化剂
D.含有最高价元素的化合物不一定具有强的氧化性
参考答案:A、化合态元素形成单质,元素化合价即可能降低也可能升高,物质可能发生氧化反应或还原反应,故A正确;
B、还原性强弱与失电子能力有关,与失电子数目多少无关,如钠比铝活泼,但钠失电子少,故B错误;
C、中间价态的离子,即具有氧化性也具有还原性,如亚铁离子,故C错误;
D、元素表现氧化性主要是看得电子能力,最高价只能有氧化性,但不一定有强氧化性,如NaCl中的钠元素,故D正确.
故选:BC.
本题解析:
本题难度:一般
3、选择题 为了实现下列各变化,需还原剂物质的是( )
A.KClO3→O2
B.NH4+→NH3
C.Fe→FeCl3
D.CO2→CO
参考答案:D
本题解析:
本题难度:简单
4、简答题 稀硝酸和足量的铁反应的化学方程式如下:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
(1)该氧化还原反应的氧化剂是______,氧化产物是______.用双线桥法在化学方程式中表示出电子转移的方向和数目为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
(2)此反应的离子方程为______.
(3)若生成标准状况下11.2LNO气体,计算参加反应的铁的质量以及反应中被还原的HNO3的物质的量.
参考答案:(1)该反应中,硝酸得电子作氧化剂,铁失电子作还原剂,铁对应的产物硝酸亚铁是氧化产物,该反应中铁失去电子数=3(2-0)=6,硝酸得电子数=2(5-2)=6,所以用双线桥法在化学方程式中表示出电子转移的方向和数目为
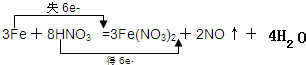
,
故答案为:HNO3;Fe(NO3)2;
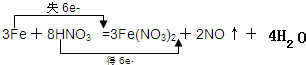
;
(2)该反应的离子方程式为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故答案为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
(3)设参加反应的铁的质量为m,
被还原的HNO3的物质的量为n
由?3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O
? 3×56g?2mol(被还原)?2×22.4L
? m?n?11.2L
得?m=11.2L×3×56g2×22.4L=42?g
n=11.2L×2mol2×22.4L=0.5?mol
答:参加反应铁的质量是42g,被还原的硝酸的物质的量是0.5mol.
本题解析:
本题难度:一般
5、填空题 (1)在反应5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,氧化剂是______,还原剂是______;氧化剂具有______性;被氧化和被还原的原子数之比是______.
(2)某溶液有Cl-、CO32-、SO42-等,今要求在一次样液中先后检验出这三种离子,请完成下列实验设计:先加足量______溶液,生成气泡,确定CO32-存在;再加足量______溶液,现象是______,确定SO42-存在;过滤后向滤液中加______溶液,现象是生成白色沉淀,确定Cl-存在.
参考答案:(1)由5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O可知,KCl中Cl元素的化合价由-1价升高为0,则KCl为还原剂,KClO3中Cl元素的化合价由+5价降低为0,KClO3为氧化剂,氧化剂具有氧化性,由电子守恒可知,被氧化和被还原的原子数之比是5:1,
故答案为:KClO3;KCl;氧化;5:1;
(2)先后检验出这三种离子,应排除离子之间的干扰,先加足量硝酸液,生成气泡,确定CO32-存在;再加足量硝酸钡溶液,观察到白色沉淀,则确定SO42-存在;过滤后向滤液中加 硝酸银溶液,现象是生成白色沉淀,确定Cl-存在,
故答案为:硝酸;硝酸钡;白色沉淀;硝酸银.
本题解析:
本题难度:一般