1、选择题 如果菜籽油中混有 水,最好采用下列何种方法分
水,最好采用下列何种方法分 离
离
A.过滤
B.蒸馏
C.分液
D.萃取
参考答案:C
本题解析:略
本题难度:简单
2、选择题 下列实验装置或操作正确的是
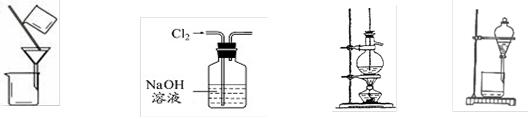
A.分离NaCl溶液中CaCO3
B.除去Cl2中含有的HCl
C.石油分馏
D.分离乙醇和水
参考答案:A
本题解析:A.碳酸钙不溶于水,可用过滤的方法分离,故A正确;B.氯气和NaOH反应,应通过饱和食盐水除杂,故B错误;C.蒸馏时,温度计应位于蒸馏烧瓶支管口附近,故C错误;D.乙醇和水混溶,不能用分液的方法分离,应用蒸馏的方法分离,故D错误.故选A.
本题难度:一般
3、实验题 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
2NH3(g)+CO2(g) NH2COONH4(s) + Q? (Q > 0 )
NH2COONH4(s) + Q? (Q > 0 )
(1)如用如图装置制取氨气,你所选择的试剂是?。

制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。
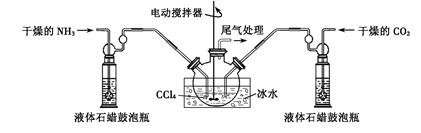
注:四氯化碳与液体石蜡均为惰性介质。
(2)发生器用冰水冷却的原因是___________ __?_。
(3)液体石蜡鼓泡瓶的作用是_______。
(4)从反应后的混合物中分离出产品的实验方法是_______(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a. 常压加热烘干? b. 高压加热烘干? c. 真空40 ℃以下烘干
(5)尾气处理装置如图所示。双通玻璃管的作用:________?;浓硫酸的作用:?、______________?_。
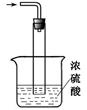
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为
___________。(精确到2位小数)
参考答案:(1) 浓氨水与生石灰(氢氧化钠固体等) (2分,合理即给分)
(2)降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解)(2分)
(3) 通过观察气泡,调节NH3与CO2通入比例 (1分)
(4)过滤? c(各1分,共2分)
(5)防止倒吸;吸收多余氨气、防止空气中水蒸气进入反应器使氨基甲酸铵水解(各1分,共3分)
(6)0.80或80%(有效数字没有考虑扣1分)?(2分)
本题解析:(1)由于氨水中存在平衡关系NH3+H2O NH3・H2O
NH3・H2O NH4++OH-,所以要利用浓氨水制备氨气,可以把浓氨水滴入到固体氧化钙或氢氧化钠,在溶解过程中放热且溶液中c(OH-)增大,使浓氨水分解生成氨气。
NH4++OH-,所以要利用浓氨水制备氨气,可以把浓氨水滴入到固体氧化钙或氢氧化钠,在溶解过程中放热且溶液中c(OH-)增大,使浓氨水分解生成氨气。
(2)反应2NH3(g)+CO2(g) NH2COONH4(s)+Q是放热反应,降低温度平衡向正反应方向进行,有利于氨基甲酸铵上网生成。且氨基甲酸铵受热易分解,所以反应过程中需要用冰水冷却。
NH2COONH4(s)+Q是放热反应,降低温度平衡向正反应方向进行,有利于氨基甲酸铵上网生成。且氨基甲酸铵受热易分解,所以反应过程中需要用冰水冷却。
(3)因为气体参与反应的不易控制反应速率和用量,所以液体石蜡鼓泡瓶的作用是控制反应进行程度,控制气体流速和原料气体的配比,即通过观察气泡,调节NH3与CO2通入比例。
(4)制备氨基甲酸铵的装置如图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小,其晶体悬浮在四氯化碳中,分离产品的实验方法利用过滤得到,氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、不能加热烘干,应在真空40℃以下烘干,所以答案选c。
(5)氨气易溶于水,所以需要有防倒吸装置,双通玻璃管的作用是防止液体倒吸;氨气是碱性气体,浓硫酸是强酸,且具有吸水性,所以浓硫酸起到吸收多余的氨气,同时防止空气中水蒸气进入反应器使氨基甲酸铵水解。
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g。该物质是碳酸钙,其物质的量为1.000g÷100g/mol=0.010mol。设样品中氨基甲酸铵物质的量为x,碳酸氢铵物质的量为y,依据碳原子守恒得到;x+y=0.01,又因为78x+79y=0.7820,解得x=0.008mol、y=0.002mol,则样品中氨基甲酸铵的物质的量分数= ×100%=80%。
×100%=80%。
本题难度:困难
4、选择题 把镁粉中混入的少量铝粉除去,应选用的试剂是
[? ]
A.盐酸
B.氯水
C.烧碱溶液
D.纯碱溶液
参考答案:C
本题解析:
本题难度:一般
5、填空题 (4分)海带中含有碘元素,碘缺乏者宜多食海带,为检测海带中是否含有碘元素,实验人员将海带在坩埚中烧成灰渣后加水搅拌,使海带中的碘离子溶于水,然后在所得澄清溶液中通入适量氯气,将碘离子转变成单质碘,为进一步检验溶液中单质碘的存在,人们利用碘易溶于四氯化碳溶剂且呈紫红色的特殊性进行确认,最终发现海带中含碘。在上述实验中未提到的两步常见分离操作的名称是:?、?。
参考答案:过滤;萃取
本题解析:海带灰加水搅拌后应过滤;向滤液中通入氯气生成I2,I2在水中溶解度不大,在有机溶液中溶解度较大,加四氯化碳萃取出碘水中碘。
点评:混合物分离常见方法:过滤、蒸发、蒸馏(分馏)、萃取分液、加热分解、洗气、升华等。
本题难度:简单