分液
参考答案:C
本题解析:略
本题难度:一般
2、填空题 (4分)某无色溶液可能是由Na2CO3、 NaOH 、MgCl2、AlCl3、BaCl2 、Fe2(SO4)3 、(NH4)2SO4溶液中的两种或两种以上混合而成。取该溶液少许于试管,向其中加入H2SO4,有白色沉淀生成,继续加入H2SO4时沉淀又完全消失,整个实验过程中无气体产生,则原溶液是由??和??混合而成。实验过程中有关的离子反应方程式是?
参考答案:AlCl3溶液和NaOH溶液(2分);Al3++4OH―=AlO2―+2H2O、AlO2―+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3 H2O(共2分)。
本题解析:略
本题难度:简单
3、填空题 多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它对环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成分为BaCO3,且含有钙、铁、镁等离子)制备BaCl2・2H2O,工艺流程如图所示。已知常温下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4。
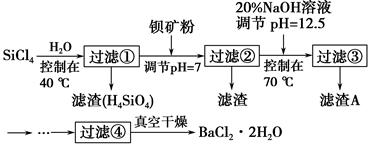
(1)SiCl4水解控制在40 ℃的原因是___________________________________。
已知:SiCl4(s)+H2(g)=SiHCl3(s)+HCl(g)?ΔH1=+47 kJ・mol-1
Si(s)+3HCl(g)=SiHCl3(s)+H2(g)?ΔH2=-189 kJ・mol-1
则由SiCl4制备硅的热化学方程式为__________________________________。
(2)加钡矿粉时生成BaCl2的离子反应方程式是_________________________。
(3)加20% NaOH溶液调节pH=12.5,得到滤渣A的主要成分是________,控制温度70 ℃的目的是____________________________________________。
(4)BaCl2滤液经蒸发浓缩、降温结晶、过滤,再经真空干燥后得到BaCl2・2H2O。实验室中蒸发浓缩,用到的含硅酸盐的仪器有__________种。
(5)为体现该工艺的绿色化学思想,该工艺中能循环利用的物质是____________。
参考答案:(1)防止HCl挥发污染环境或控制SiCl4的水解速率,防止反应过于剧烈 SiCl4(s)+2H2(g)=Si(s)+4HCl(g) ΔH=+236 kJ・mol-1
(2)BaCO3+2H+=Ba2++CO2↑+H2O
(3)Mg(OH)2、Ca(OH)2 确保钙离子完全除去[或温度越高,Ca(OH)2溶解度越小]
(4)3 (5)BaCl2
本题解析:根据题中信息SiCl4与水反应时,强烈水解并放出大量的热,控制温度较低,可以降低反应速率,减少HCl的挥发。将题给的两个热化学方程式相减,便得到制硅的热化学方程式。(2)过滤后溶液为盐酸,与碳酸钡发生反应,碳酸钡难溶,写离子方程式时,应保留化学式。(3)根据题中的信息,常温下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4,因此调节pH=7时滤渣的主要成分是Fe(OH)3,pH=12.5时滤渣的主要成分是Mg(OH)2,同时控制温度较高时,Ca(OH)2溶解度减小,有Ca(OH)2生成。(4)蒸发浓缩时,需要用到酒精灯、蒸发皿、玻璃棒。(5)过滤④的滤液中含有大量的氯化钡,可以循环利用。
本题难度:一般
4、选择题 (辽宁省大连市八中2007―2008学年度高三上学期期中考试,化学,9)下列每组各有三对物质,它们都能用分液漏斗分离的是
①乙酸乙酯和水,酒精和水,苯酚和水
②二溴乙烷和水,溴苯和水,硝基苯和水
③甘油和水,乙醛和水,乙酸和乙醇
④油酸和水,甲苯和水,乙烷和水
A.①②
B.②④
C.③④
D.①②④
参考答案:B
本题解析:①中酒精和水、③中的三组物质均相互溶解,不能用分液漏斗分离。故②④中的各组均互相部溶,可用分液漏斗分离。
本题难度:简单
5、选择题 有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可以将它们鉴别出来,这种试剂是
A.NaOH
B.H2SO4
C.BaCl2
D.KSCN
参考答案:A
本题解析:分析:这五种物质的阴离子相同阳离子不同,钠离子可以用焰色反应检验,亚铁离子可以用酸性高锰酸钾或氢氧根离子检验,反应现象分别是酸性高锰酸钾溶液褪色和先生成白色沉淀后生成灰绿色沉淀最终生成红褐色沉淀,铁离子可以用氢氧根离子检验也可以用硫氰化钾溶液检验,分别生成红褐色沉淀和溶液呈血红色,镁离子用氢氧根离子检验,生成白色沉淀,铝离子用氢氧根离子检验,先生成白色沉淀,当氢氧根离子过量时氢氧化铝转化为可溶性的偏铝酸盐,沉淀消失,注意氢氧化铝不溶于弱碱,所以向以上五种溶液中加入氢氧化钠溶液后反应现象为:无现象,先生成白色沉淀后生成灰绿色沉淀最终生成红褐色沉淀,红褐色沉淀,白色沉淀,先生成白色沉淀后沉淀消失.
解答:A、向以上五种溶液中加入氢氧化钠溶液后反应现象为:无现象,先生成白色沉淀后生成灰绿色沉淀最终生成红褐色沉淀,红褐色沉淀,白色沉淀,先生成白色沉淀后沉淀消失,反应现象不同,所以可以用氢氧化钠溶液区别,故A正确;
B、硫酸和以上五种物质不反应,现象相同,所以无法区别,故B错误;
C、氯化钡和以上五种物质不反应,现象相同,所以无法区别,故C错误;
D、硫氰化钾溶液和NaCl、FeCl2、MgCl2、AlCl3四种溶液不反应,现象相同,所以无法区别,故D错误.
故选A.
点评:本题考查物质的鉴别,注意物质的鉴别要有典型的不同现象才可以,尤其注意铁离子和氯离子的检验,为高考的热点,该种题型涉及元素化合物知识,要注意总结和积累.
本题难度:一般
|