1、选择题 下列装置或操作能达到实验目的是( )
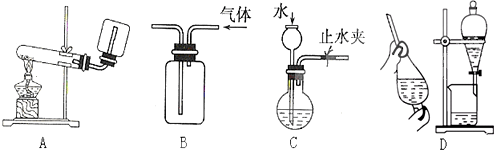
A.A是实验室制氧气装置
B.B是收集CO2气体的装置
C.C是检查装置的气密性
D.D是分离酒精和水的装置
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列有关物质的性质和该性质的应用均正确的是( )
A.NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体
B.碳酸钠溶液显碱性,用热的碳酸钠溶液可去除金属表面的油污
C.次氯酸钠具有强还原性,可用于配制“84”消毒液
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
参考答案:B
本题解析:
本题难度:一般
3、简答题 实验室有一瓶密封不严的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究.
试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水.
(1)[提出假设]假设一:该漂白粉未变质,含______;
假设二:该漂白粉全部变质,含______;
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3.
(2)[进行实验]在答题卡上完成下表写实验步骤、预期现象与结论(不必检验Ca2+、Cl-):
| 实验步骤 | 预期现象和结论
1
用试管取少量澄清石灰水备用,用另一试管取少量样品,再______
若无气体放出且澄清石灰水未见浑浊,则假设一成立;
2
______
______
③
______
______
参考答案:(1)漂白粉的主要成分为CaCl2、Ca(ClO)2,Ca(ClO)2易与空气中二氧化碳和水反应生成HClO,HClO不稳定,见光分解生成HCl和水,最终生成CaCl2、CaCO3,如果漂白粉部分变质,则成分为CaCl2、Ca(ClO)2、CaCO3,
故答案为:CaCl2、Ca(ClO)2;CaCl2、CaCO3;
(2)如漂白粉没有变质,则漂白粉中无CaCO3,加入盐酸后无气体放出且澄清石灰水未见浑浊;
如漂白粉全部变质,则产物为CaCl2、CaCO3,取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水,则品红不褪色,而石灰水变浑浊;
如漂白粉部分变质,漂白粉中含有CaCl2、Ca(ClO)2、CaCO3,取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水,品红溶液褪色,澄清石灰水变浑浊.
故答案为:?实验步骤预期现象和结论①再向试管加入1mol/L的稀盐酸?②取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水品红不褪色,而石灰水变浑浊,假设二成立 ③取少量样品于试管中,加入足量的稀盐酸,并将所得气体依次通入品红溶液和澄清石灰水品红溶液褪色,澄清石灰水变浑浊,假设三成立
本题解析:
本题难度:一般
4、实验题 某校化学小组学生利用下图所示装置进行“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中有CO2和CO(图中夹持装置已略去)。
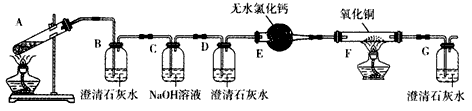
(1)装置C的作用是____________ 装置E的作用是________________
(2)乙二酸受热分解的化学方程式是_____________________
(3)①证明分解产物中有CO2的现象是_________________
②证明分解产物中有CO的现象是___________________
(4)该装置有一个不足之处,请写出弥补这个不足之处的理由和具体方法:____________________
参考答案:(1)吸收乙二酸晶体受热分解生成的二氧化碳干燥CO
(2)HOOC-COOH CO↑+CO2↑+H2O CO↑+CO2↑+H2O
(3)装置B中澄清石灰水变浑浊;装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊
(4)在G装置后加燃着的酒精灯处理尾气中的CO,以防止其污染空气
本题解析:
本题难度:一般
5、实验题 实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取wg该种氨基酸放在纯氧中充分燃烧,生成
CO2、H2O和N2。现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出),请回答有关问题
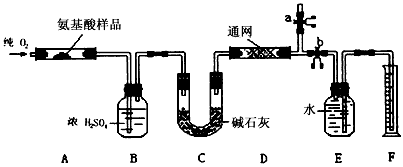
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通一段时间的纯氧,这样做的目的是__________;之后则需关闭止水夹________,打开止水夹__________。
(2)以上装置中需要加热的有(填装置代号)________。操作时应先点燃________处的酒精灯。
(3)装置A中发生反应的化学方程式为_____________________________;
(4)装置D的作用是______________________________;
(5)为将N2所排水的体积测准,反应前应将连接E和F装置的玻璃导管中充满________(水、空气或氧气),简述理由________________________。
(6)读取N2所排水的体积时,要注意:①________________________;②________________________。
(7)实验中测得N2的体积为VmL(已换算成标准状况)。为确定此氨基酸的分子式,还需得到的数据有(填字母)________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通入氧气的体积
D.该氨基酸的摩尔质量
(8)如果将装置中B、C的连接顺序变为C、B,该实验的目的能否达到?简述理由________________________________________。
参考答案:(1)将装置中的N2排净;a;b
(2)AD;D
(3)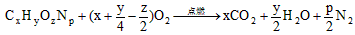
(4)吸收未反应的O2,保证最终收集到的气体是反应生成的N2
(5)水;这段玻璃管中如充满气体,将不能被收集和测量,导致较大的实验误差,而充满水时将保证进入装置E的气体体积与排出水的体积基本相等
(6)①量筒中的液面应与广口瓶中的液面相持平;②视线应与刻度线和凹液面最低点相切
(7)ABD
(8)不能达到该实验的目的,因为碱石灰是碱性干燥剂,将同时吸收H2O和CO2两种气体,使实验结果缺少必要的数据,无法确定该氨基酸的分子组成
本题解析:
本题难度:困难
|