1������� ��һ����ɫ�����ĩ�����ܺ���Na2SO4��CaCO3��KCl��BaCl2��CuSO4�е�һ�ֻ��֣������²������ʵ�飺
��1���������ĩ����ˮ�õ���ɫ��Һ�Ͱ�ɫ������
��2������������ϡ���ᣬ���������ܽ��������ݲ�����
��������ʵ������������ж��������һ������______���ʣ�һ��û��
______���ʣ����ܺ��е�����______��
д����1���ķ�Ӧ����ʽ______
д����2���ķ�Ӧ����ʽ______��
�ο��𰸣���Na2SO4��CaCO3��KCl��BaCl2��CuSO4����ˮ�õ���ɫ��Һ�Ͱ�ɫ��������һ������������ͭ����ɫ������̼��ƣ������������ƺ��Ȼ�����Ӧ���ɵ����ᱵ��Na2SO4+BaCl2�TBaSO4��+2NaCl������Ϊ����������ϡ���ᣬ���������ܽ��������ݲ���������һ���ǼȺ���̼�ᱵ�������������ƺ��Ȼ������ڣ��Ȼ��ش��������ȷ����̼������������У�CaCO3+2HCl�TCaCl2+H2O+CO2�������ᱵ�������Ӧ��
�ʴ�Ϊ��Na2SO4��CaCO3��BaCl2��CuSO4��KCl��Na2SO4+BaCl2�TBaSO4��+2NaCl��CaCO3+2HCl�TCaCl2+H2O+CO2����
���������
�����Ѷȣ���
2������� ʳ�����ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ�
��1����ʳ�γ���������K+��Ca2+��Mg2+��Fe3+��SO42-���������ӣ�ʵ�����ᴿNaCl���������£�
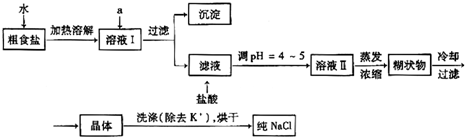
�ṩ���Լ�������Na2CO3��Һ?����K2CO3��Һ?NaOH��Һ?BaCl2��ҺBa��NO3��2��Һ?75%�Ҵ������Ȼ�̼
������ȥ��ҺI�е�Ca2+��Mg2+��Fe3+��SO42-���ӣ�ѡ��a���������Լ������μ�˳������Ϊ______��ֻ�ѧʽ����
��ϴ�ӳ�ȥNaCl������渽��������KCl��ѡ�õ��Լ�Ϊ______��
��2�����ᴿ��NaCl����500mL4.00mol?L-1NaCl��Һ������������ҩ�ס����������______�����������ƣ���
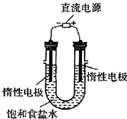
��3����ⱥ��ʳ��ˮ��װ����ͼ��ʾ�����ռ���H2Ϊ2L����ͬ���������ռ���Cl2______�����������=��������2L��ԭ����______��װ�øĽ��������Ʊ�NaOH��Һ�����ⶨ��Һ��NaOH��Ũ�ȣ����õķ�����______��
��4��ʵ�����Ʊ�H2��Cl2ͨ���������з�Ӧ��
Zn+H2SO4?ZnSO4+H2����MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O
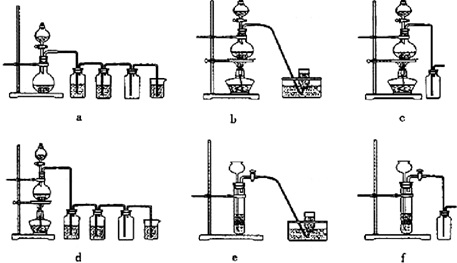
�ݴˣ���������������װ����ѡ���Ʊ����ռ�H2��װ��______������ţ����Ʊ����ռ��������Cl2��װ��______������ţ�����ѡ���Ʊ������װ�ã�
�ο��𰸣���1����Ҫ��ȥSO42-��ֻ��ѡBaCl2��Һ����ѡ��Ba��NO3��2���������µ�����NO3-����ѡ��NaOH��Һ��ȥMg2+��Fe3+��Һ�����ѡ��Na2CO3��Һ��ȥCa2+���˴�����ѡ��K2CO3��Һ������������µ�K+������HCl��ȥ������CO32-��Na2CO3��Һ���ܼ���BaCl2��Һǰ�����������Ba2+���ʴ�Ϊ��BaCl2��NaOH��Na2CO3��
�ڳ�ȥNaCl��������������KCl��Ӧѡ��75%���Ҵ�����ΪCCl4�ж���ͬʱKClҲ�����ܽ���CCl4�У�
�ʴ�Ϊ��75%�Ҵ���
��2������һ�����ʵ���Ũ�ȵ���Һ������������У�ҩ�ס�����������ƽ���ձ���500mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ����ƽ���ձ���500mL����ƿ����ͷ�ιܣ�
��3����ⱥ��ʳ��ˮ�ķ�Ӧ��2NaCl+2H2O?���?.?2NaOH+Cl2��+H2�������������ڲ�����Cl2����������ɵ�NaOH��ӦNaCl��NaClO��H2O��ʹ�ò��ֵ�Cl2�����ģ�����ͬ���������ռ�����Cl2С��2L�����ⶨ��Һ��NaOH��Ũ�ȣ������к͵ζ��ķ�����
�ʴ�Ϊ������������ɵ������������ɵ�NaOH�����˷�Ӧ���к͵ζ���
��4��ʵ�����в��ý���п������ȷ�Ӧ�������������ѡ��װ��e�����ö������̺�Ũ���������������������е������Ȼ�����Լӱ���ʳ��ˮ����������ˮ���Բ���Ũ��������ȥ������ѡ��װ��d���ʴ�Ϊ��e��d��
���������
�����Ѷȣ�һ��
3������� �ó������ⶨNaHCO3��K2CO3��������ɣ�ʵ�������ÿ�γ�ȡһ����������Ʒ����ˮ�Ƴ���Һ�������еμ���ͬŨ�ȵ�
Ba��OH��2��Һ��ÿ��ʵ�����ַ�Ӧ��ʵ���¼���±���
| ʵ����� | ��ȡ��Ʒ������/g | ����Ba��OH��2��Һ�����/L | ������ɳ�������/g
1
0.858
0.5
1.379
2
1.716
0.5
______
3
2.574
0.5
4.137
4
3.432
0.5
5.516
5
4.290
0.5
5.516
6
5.148
0.5
5.516
|
�ش��������⣺
��1����2��ʵ���в���������������______��
��2��Ba��OH��2��Һ���ʵ���Ũ����______��
��3��ͨ������ȷ����Ʒ��NaHCO3��K2CO3�����ʵ���֮����______��
�ο��𰸣���1����3�Ρ���4�����ɳ���̼�ᱵ��������Ϊ5.516g��˵����Ʒ����Ϊ3.342gʱ�����������Ѿ���ȫ��Ӧ����1�Ρ���3����Ʒ�������ֱ�Ϊ0.858g��2.574g����1�Ρ���3�����ɳ���̼�ᱵ�����ֱ�Ϊ1.379g��4.137g����Ʒ������֮�ȵ������ɵij�������֮��Ϊ1��2��˵����3��ǡ����ȫ��Ӧ����2��ʵ������Ʒ��ȫ��Ӧ���������������Ϊmg����
1.716g��2.574g=mg��4.137g�����m=2.758���ʴ�Ϊ��2.758g��
��2��ʵ����ÿ�εμ���ͬŨ�ȵ�Ba��OH��2��Һ50.5L����5�Ρ���5�����ɳ���̼�ᱵ������Ϊ5.516g��˵����Ʒ����Ϊ3.342gʱ�����������Ѿ���ȫ��Ӧ��̼�ᱵ�����ʵ���Ϊ5.516g197g/mol=0.028mol�����ݱ������غ��֪���������������ʵ���Ϊ0.028mol������Ba��OH��2��Һ�����ʵ����ʵ���Ũ����0.028mol0.5L=0.056mol/L���ʴ�Ϊ��0.056mol/L��
��3����3��ʵ������Ʒ��ȫ��Ӧ����̼��������̼��ص����ʵ����ֱ�Ϊxmol��ymol����
���������
�����Ѷȣ�һ��
4��ʵ���� ��ͼ��ʾΪʵ������ȡ����ˮ��װ��ʾ��ͼ������ͼʾ�ش��������⡣
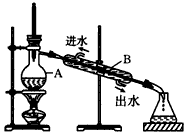
(1)ͼ�����������ԵĴ����ǣ� ��________________�� ��_______________��
(2)A������������_________��B������������_________��
(3)ʵ��ʱA�г�������������ˮ�⣬����Ҫ����������__________����������_______________��
�ο��𰸣�(1)���¶ȼ�ˮ�������̫���ˣ�����ȴˮ���ڡ����ڷ���귴��
(2)������ƿ��������
(3)��ʯ�������Ƭ������ֹҺ�屩��
���������
�����Ѷȣ�һ��
5������� ��һ��ɫ�����ĩ������̼���ơ��������ơ��������е�һ�ֻ���֣�ij��ȤС����Ը���Ʒ����̽����
��1��ȡ������Ʒ�ܽ���ˮ���ⶨ��Һ��pH���������Һ��pH=7������Ʒ��һ������______��һ������______��
��2�����Ҫ�������Ʒ�Ƿ��������ƣ����Ҫ˵������ķ���������ͽ��ۣ�______��
��3��ȡ����������Ʒ������������У�������ų�����Ҫ����ų��������ɣ����������Լ���ѡ����ʵ��Լ����һ�����ʵ������û���������ɣ���Ҫд��ʵ�鷽��������ͽ��ۣ�
���Լ���Ʒ����Һ������ʯ��ˮ������KMnO4��Һ����������Ũ��Һ������NaHCO3��Һ��
| ʵ�鷽�� | ���ܵ��������Ӧ�Ľ���
�������������ͨ��ʢ��______��______��______��ϴ��ƿ��
�ο��𰸣���1��̼���ƺ����������Һ�У���Ϊ������ˮ�����Һ��ʾ���ԣ�ֻ���������Dz�ˮ����Σ������ԣ��ʴ�Ϊ�������ƣ�̼���ơ��������ƣ�
��2��Ҫ�������Ʒ�Ƿ��������ƣ�ֻ��������е���������Ӽ��ɣ�������������ӵ��������ӷ�Ӧ���ܺͱ����ӷ�Ӧ���ɲ���������İ�ɫ���������У�ע�ⲻ�������ᣬ������������ԣ��ܽ������������������
�ʴ�Ϊ��ȡ����������Ʒ������������У�Ȼ�����BaCl2��Һ�����г�������˵����Ʒ����Na2SO4������������˵��˵����Ʒ��û��Na2SO4��
��3��ȡ����������Ʒ������������У�������ų����������Ƕ�����̼�Ͷ��������е�����һ�֣���������Ͷ�����̼����ʹ����ʯ��ˮ����ǣ��ڼ��������̼֮ǰ�ȼ����������Ĵ��ڲ��������������������ó���ʯ��ˮ�����������̼����������ļ���ʹ��Ʒ�죬��ȥ������������ø�����أ�������̼�ļ����ó���ʯ��ˮ���ʴ�Ϊ��ʵ�鷽�����ܵ��������Ӧ�Ľ���Ʒ����Һ��
������������KMnO4��Һ��������������ʯ��ˮ��Ʒ����ɫ��������KMnO4��Һ����ȫ��ɫ��������ʯ��ˮ����ǣ���������SO2��CO2�Ļ��������Ʒ����ɫ��������KMnO4��Һ����ȫ��ɫ��������ʯ��ˮ������ǣ���������SO2��Ʒ�첻��ɫ��������KMnO4��Һ����ɫ��������ʯ��ˮ����ǣ���������CO2
���������
�����Ѷȣ�һ��
|