1、填空题 有一包白色固体粉末,可能含有Na2SO4,CaCO3,KCl,BaCl2,CuSO4中的一种或几种,按以下步骤进行实验:
(1)将固体粉末溶于水得到无色溶液和白色沉淀;
(2)加以足量的稀盐酸,沉淀部分溶解且有气泡产生.
根据以上实验产生的现象,判断这混合物里,一定含有______物质.一定没有
______物质,可能含有的物质______.
写出(1)的反应方程式______
写出(2)的反应方程式______.
2、简答题 食盐是日常生活的必需品,也是重要的化工原料.
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
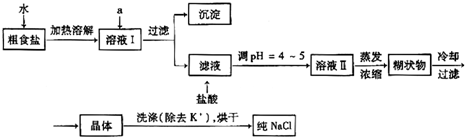
提供的试剂:饱和Na2CO3溶液?饱和K2CO3溶液?NaOH溶液?BaCl2溶液Ba(NO3)2溶液?75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为______(只填化学式).
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为______.
(2)用提纯的NaCl配制500mL4.00mol?L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有______(填仪器名称).
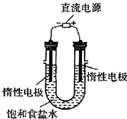
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2______(填“>”、“=”或“<”)2L,原因是______.装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法是__ ____.
(4)实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4?ZnSO4+H2↑;MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
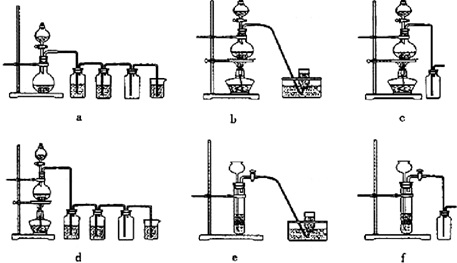
据此,从下列所给仪器装置中选择制备并收集H2的装置______(填代号)和制备并收集干燥、纯净Cl2的装置______(填代号).可选用制备气体的装置:
3、简答题 用沉淀法测定NaHCO3和K2CO3混合物的组成.实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的
Ba(OH)2溶液,每次实验均充分反应.实验记录见下表:
| 实验次数 | 称取样品的质量/g | 所加Ba(OH)2溶液的体积/L | 测得生成沉淀质量/g
1
0.858
0.5
1.379
2
1.716
0.5
______
3
2.574
0.5
4.137
4
3.432
0.5
5.516
5
4.290
0.5
5.516
6
5.148
0.5
5.516
|
回答下列问题:
(1)第2次实验中产生沉淀的质量是______;
(2)Ba(OH)2溶液物质的量浓度是______;
(3)通过计算确定样品中NaHCO3和K2CO3的物质的量之比是______.
4、实验题 如图所示为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
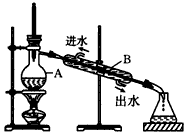
(1)图中有两处明显的错误是: ①________________, ②_______________。
(2)A仪器的名称是_________,B仪器的名称是_________。
(3)实验时A中除加入适量自来水外,还需要加入少量的__________,其作用是_______________。
5、简答题 有一白色固体粉末可能是碳酸钠、亚硫酸钠、硫酸钠中的一种或二种,某兴趣小组拟对该样品进行探究.
(1)取少量样品溶解于水,测定溶液的pH,若测得溶液的pH=7,则样品中一定含有______,一定不含______;
(2)如果要检验该样品是否含有硫酸钠,请简要说明检验的方法、现象和结论:______;
(3)取适量固体样品加入过量盐酸中,有气体放出.若要检验放出气体的组成,从以下限定试剂中选择合适的试剂设计一个组合实验分析该混合气体的组成,简要写出实验方案、现象和结论.
限定试剂:品红溶液、澄清石灰水、酸性KMnO4溶液、氢氧化钠浓溶液、饱和NaHCO3溶液.
| 实验方案 | 可能的现象和相应的结论
将混合气体依次通过盛有______、______、______的洗气瓶.
|