1、选择题 已知短周期主族元素A、B在周期表中的相对位置如右图(稀有气体除外),则下列说法不正确的是
?
A.A一定是第2周期元素? B.B的原子半径一定比A大?
C.B的金属性一定比A强? D.A的熔沸点一定比B高
参考答案:D
本题解析:根据A、B在周期表中的相对位置知,A是第2周期、B为第三周期,根据原子半径和元素金属性变化规律,A、B、C均正确;A的熔沸点不一定比B高,如A为F、B为S,溶沸点后者高,D错误。
本题难度:一般
2、选择题 下列基态原子或离子的电子排布式错误的是 ?
A.Ca: 1s22s22p63s23p64s2
B.Mg2+: 1s22s22p6
C.F―: 1s22s22p5
D.Br: 1s22s22p63s23p63d104s24p5
参考答案:C
本题解析:根据构造原理可知 ,选项C是错误的,应该是1s22s22p6,其余选项都是正确的,答案选C。
点评:该题是高考中的常见考点和题型,属于基础性试题的考查,试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力。该题的关键是记住构造原理,然后灵活运用即可。
本题难度:一般
3、填空题 (12分)下表为元素周期表的一部分,按要求完成各小题。

| IA
| IIA
| IIIA
| IVA
| VA
| VIA
| VIIA
| 0
|
2
| ?
| ?
| ?
| ⑥
| ?
| ⑦
| ⑾
| ?
|
3
| ①
| ③
| ⑤
| ?
| ?
| ?
| ⑧
| ⑩
|
4
| ②
| ④
| ?
| ?
| ?
| ?
| ⑨
| ?
|
小题1:化学性质最不活泼的元素 ??(填元编号,下同),非金属性最强的元素是?金属性最强的单质与水反应的离子方程式为 ?
小题2:①③⑤三种元素的最高价氧化物水化物中,碱性最强的 ?
小题3:①③⑤三种元素的原子半径由大到小的顺序为??
小题4:某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素为 ??在两种盐中该元素的化合价为??,该元素的最高价氧化物和盐酸反应的化学方程式为 ?向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为?
参考答案:
小题1:⑩? ⑾? 2K + 2H2O ==2K + ?+ 2OH― + H2?
小题2: ①?
小题3:①③⑤
小题4:⑤? +3? AI2O3+6HCI==2AICI3+3H2O?随着氢氧化钠的滴入,白色沉淀逐渐增加,当达到最多后又逐渐减少,最后完全消失,得到澄清溶液
本题解析:考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断,①~⑾分别为Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar、F。
(1)稀有气体元素的性质最不活泼,非金属性最强的是F,金属性最强的K。
(2)金属性越强,最高价氧化物的水化物的碱性就越强。同周期元素自左向右原子半径逐渐减小,金属性逐渐减弱。所以氢氧化钠的碱性最强。
(3)①③⑤属于同一周期,所以原子半径大小顺序为①③⑤
(4)氢氧化铝既和酸反应,也和强碱反应生成盐和水。铝属于第ⅢA,化合价是+3价。
本题难度:一般
4、填空题 (12分)X、Y、Z、M是元素周期表前四周期中的四种常见元素,其相关信息如下表:
元素
| 相关信息
|
X
| X的基态原子核外3个能级上有电子,且每个能级上的电子数相等
|
Y
| 常温常压下,Y单质是黄色固体,常在火山口附近沉积
|
Z
| Z和Y同周期,Z的电负性大于Y
|
M
| M的一种核素的质量数为63,中子数为34
|
(1)属于主族元素的原子半径从大到小的顺序是(写化学式,下同)?,Y和Z的最高价氧化物对应的水化物的酸性较强的是?,在H-Y、H-Z两种共价键中,键的极性较强的分子是?。
(2)XY2是一种常用的溶剂,XY2的电子式是?,XY2的分子中存在?个σ键。
(3)M位于周期表第____周期第?族,M的基态原子核外电子排布式是?;M2Y在空气中煅烧生成M2O的化学方程式是?。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:XO(g)+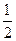 O2(g)= XO2(g)?△H =" -283.0" kJ・mol-1
O2(g)= XO2(g)?△H =" -283.0" kJ・mol-1
Y(g)+ O2(g)= YO2(g)△H = -296.0 kJ・mol-1
写出此反应的热化学方程式____?。
参考答案:(12 分)(1 )S>Cl>C或 r(S)>r(Cl)>r(C),HClO4 , HCl?
(2)CS2电子式略,?2?。
(3)第 四 周期第?ⅠB 族, 1s22s22p63s23p63d104s1或[Ar]3d104s1,
2Cu2S + 3O2  ?2Cu2O+2SO2(共2分,条件1分)
?2Cu2O+2SO2(共2分,条件1分)
(4) 2CO(g)+SO2(g)==2CO2(g)+S(g) ΔH=" -" 270kJ/mol__(方程式2分 ,其余每空1分)
,其余每空1分)
本题解析:略
本题难度:一般
5、选择题 某元素最高价氧化物对应水化物的化学式是H3XO4,该元素的气态氢化物的化学式是(?)
A.H2X
B.HX
C.XH3
D.XH4
参考答案:C
本题解析:由元素最高价氧化物对应水化物的化学式可知X的化合价为+5价,最原子外层从有5个电子,得3个电子达到稳定结构,对应氢化物中X的化合价应为-3价,则化学式为XH3。
故选C。
点评:本题考查化学式的推断,题目难度不大,本题注意根据最高化合价判断元素在周期表的位置以及原子结构。
本题难度:简单