1������� ��֪��A��BΪ�����ķǽ��������Ҿ�Ϊ���壻�ס���Ϊ�������ʣ�����I��Ũ��Һ�з����ۻ���C��H��J����Һ���ʼ��ԣ������ʼ��ת����ϵ����(����������δ��������δע����Ӧ����)��
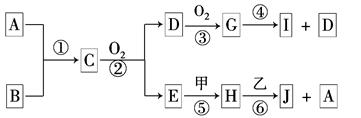
(1)д����Ӧ�ڵĻ�ѧ����ʽΪ_________________________________________��
(2)��Ӧ����ÿ����1 mol G��ת�Ƶ��ӵ����ʵ���Ϊ______________��
(3)��Ӧ�����ӷ���ʽ��___________________________________________��
(4)ʵ�����б���I�ķ�����____________________________��
�ο��𰸣�(1)4NH3��5O2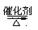 4NO��6H2O( 2��)
4NO��6H2O( 2��)
(2) mol( 2��)?(3)2Al��2H2O��2OH��===2AlO��3H2��( 2��)
(4)��������ɫ�Լ�ƿ�У�����������( 2��)
�����������
�����Ѷȣ���
2������� ijЩ��ѧ��Ӧ������ʽ��ʾ��A+B��C+D+H2O����ش��������⣺
��1����A��C��D��������Ԫ�أ���A�Ļ��ϼ۽���C��D֮�䣬д���÷�Ӧ�����ӷ���ʽ��______��
��2����C��D��Ϊ�����Ҷ���ʹ����ʯ��ˮ����ǣ���A��B�����Ϊ______��
��3����AΪ��ɫ���壬C�ǻ���ɫ�ĵ������壬д���÷�Ӧ�����ӷ���ʽ��______��
��4����AΪNa2O2��BΪ���ᣬ��C��D�Ļ�ѧʽΪ______��
��5����A��C��������Ԫ�أ���C����Ϊ______��______��
��6����AΪ����ɫ�Ľ������ʣ�BΪ�ڶ�����ij��Ԫ�ص�����������ˮ�����д��������ʽ�Ļ�ѧ����ʽ��______��
�ο��𰸣���1��A��C��D�о�������Ԫ�أ���A�е�Cl�Ļ��ϼ۽���C��D֮�䣬�÷�ӦΪ�����ڼ��������µ��绯��Ӧ����Ӧ�����ӷ���ʽΪCl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��2����ʹ�����ʯ��ˮ����ǵ�������SO2��CO2��ӦΪ̼��Ũ����ķ�Ӧ����A��B�����ΪC��ŨH2SO4��
�ʴ�Ϊ��C��ŨH2SO4��
��3��ӦΪMnO2��Ũ����ķ�Ӧ�����ɻ���ɫ����ΪCl2����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��
��4����AΪNa2O2��BΪ���ᣬ����Na2SO4��O2����C��D�Ļ�ѧʽΪNa2SO4��O2���ʴ�Ϊ��Na2SO4��O2��
��5����A��C��������Ԫ�أ�����ˮ����ΪAlCl3�����ǿ���NaAlO2�����ǿ��ķ�Ӧ��C����ΪAlCl3��NaAlO2��
�ʴ�Ϊ��AlCl3��NaAlO2��
��6��BΪ�ڶ�����ij��Ԫ�ص�����������ˮ���ֻ��ΪHNO3����AΪCu��������Ӧ�ķ���ʽΪ
Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O[��3Cu+8HNO3��ϡ��=3Cu��NO3��2+2NO��+4H2O]��
�ʴ�Ϊ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O[��3Cu+8HNO3��ϡ��=3Cu��NO3��2+2NO��+4H2O]��
���������
�����Ѷȣ�һ��
3������� ��9�֣�
A��B��C��D��E����ѧ���������ֻ����A��B�������X��Y�������г����Ľ�����������ʼ�Ĺ�ϵ����ͼ��ʾ��ijЩ��������ȥ����

��1�����Լ�a��NaOH��Һ��
��C��������____?��
��B���Լ�a��Ӧ�����ӷ���ʽ��?��
��2�����Լ�b��ϡH2SO4��
��D�Ļ�ѧʽ��?��
��ij��Ч��ˮ������Y��OH��SO4�ۺϵõ��ġ���ҵ����E��ϡ������������ƣ�NaNO2��Ϊԭ�����Ʊ�Y��OH��SO4����Ӧ����NO���ɣ��÷�Ӧ��ѧ����ʽ�ǣ�?��
�ο��𰸣�

�����������
�����Ѷȣ�һ��
4���ƶ��� A��B��C��D��E����ѧ������5�ֻ����A��B�������Ԫ��X��Y �ĵ����������г����Ľ�����������ʼ�Ĺ�ϵ����ͼ��ʾ��
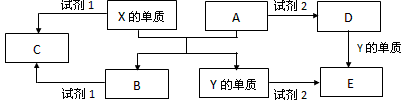
��1��X�ĵ�����A��Ӧ�Ļ�ѧ����ʽ��___________ ��
��2�����Լ�1��NaOH��Һ��X�ĵ������Լ�1��Ӧ�����ӷ���ʽ��____________ ��
��3�����Լ�1���Լ�2����ϡ���ᡣ
�ټ�������D����Һ�н������ӵķ�����___________ ��
�ڽ�����C����ˮ������Һ�����ԣ�ԭ����______________�������ӷ���ʽ��ʾ�� ��
��ij��Ч��ˮ������Y(OH)SO4�ۺϵõ��ġ���ҵ����E��ϡ�������������Ϊԭ�����Ʊ�Y(OH)SO4����Ӧ����NO���ɣ��÷�Ӧ�Ļ�ѧ����ʽ��________________ ��
�ο��𰸣���1��Fe2O3 + 2Al== Al2O3 + 2Fe
��2��2Al + 2H2O + 2OH- ==2AlO2- + 3H2��
��3����ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ�к���Fe3+��
��Al3+ + 3H2O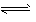 Al(OH)3 + 3H+
Al(OH)3 + 3H+
��2FeSO4 + 2NaNO2 + H2SO4 ==2Fe(OH)SO4 + Na2SO4 + 2NO��
���������
�����Ѷȣ�һ��
5���ƶ��� �ס��ҡ����������ֶ�����Ԫ�ؿ���������п�ͼ�г�Br2��L��������ʣ���ԭ���������������ҿ��γɳ���Һ̬������K������A�к��б�Ԫ�ص���һ�������ӣ�����Ӳ�ṹ����ԭ����ͬ����Ԫ��ԭ�ӵ�����������������Ӳ�����2������һ�������£����и����ʿɷ�����ͼ��ʾ�ı仯����Ӧ�����ɵ�ˮû��д������
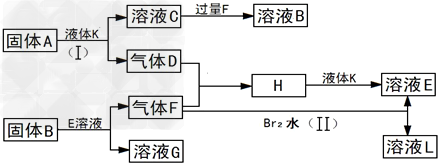
�Իش�
��1����Ԫ�ص�����Ϊ__________����Ԫ�������ڱ���λ��____________��Ԫ�ص������ӽṹʾ��ͼΪ____________��
��2��A�ĵ���ʽΪ________��������ѧ������Ϊ____________��
��3���ҡ���������Ԫ�ص����Ӱ뾶�ɴ�С��˳��Ϊ__________����Ԫ�ط��ű�ʾ��?��
��4����Ӧ��I���Ļ�ѧ����ʽΪ________________��
��5����Ӧ��II�������ӷ���ʽΪ________________��
�ο��𰸣���1���⣻�������ڢ�A�壻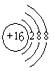
��2��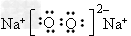 �����Ӽ����ۼ�
�����Ӽ����ۼ�
��3��S2->O2->Na+
��4��2Na2O2+2H2O=4NaOH+O2��
��5��SO2��Br2��2H2O��4H+?+?SO42-��?2Br-
���������
�����Ѷȣ�һ��