1、推断题 下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:反应①______________________ 反应②_______________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途, C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到 该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
参考答案:(1)Fe(OH)3;制造盐酸、漂白剂、农药、合成纤维、消毒杀菌等
(2)2Na+2H2O===2Na++2OH-+H2↑;2Al+2OH-+2H2O===2AlO2-+3H2↑
(3) KSCN(其它合理的答案也对)
(4)Fe(OH)2 + 2Fe(OH)3===Fe3O4 + 4H2O;做丁达尔实验,能产生丁达尔现象(其它合理答案也对)。
本题解析:
本题难度:一般
2、推断题 物质A是由A元素组成的单质,将其在酒精灯火焰上灼烧,火焰 为黄色,B、C、D是含有A元素的三种 不同化合物,A、B、C、D按下图所示关系进行转化:?

(1)写出下列物质的化学式: A____;B____;C___;D____。
(2)写出①②③的离子方程式及④的化学方程式: ①____, ②___, ③____, ④____。
参考答案:(1)Na ;NaOH ;Na2CO3 ;NaCl
(2)①2Na+2H2O=2Na++2OH-+H2↑
②2OH-+CO2=CO32- +H2O
③CO32- +2H+=CO2↑+H2O
④2Na +Cl2  2NaCl
2NaCl
本题解析:
本题难度:一般
3、填空题 A、B、C、D、E五瓶透明溶液,分别是HCl,BaCl2,NaHSO4,Na2CO3,AgNO3中的一种.
①A与B反应有气体生成;②B与C反应有沉淀生成;③C与D反应有沉淀生成;④D与E反应有沉淀生成;⑤A与E反应有气体生成;⑥在②和③的反应中生成的沉淀是同一种物质.请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是______.
(2)A是______;B是______;C是______;D是______;E是______.
参考答案:根据信息①⑤反应有气体,气体只能为CO2,则A为Na2CO3,
其余,先分组:B、E组为HCl、NaHSO4,那么C、D组为AgNO3、BaCl2,
据信息⑥知产生的沉淀为AgCl,所以C物质为AgNO3,结合其他信息知E为NaHSO4,D为BaCl2,B为HCl,
(1)反应③为AgNO3和BaCl2的反应,生成AgCl沉淀,故答案为:AgCl;
(2)由以上分析可知A为Na2CO3,B为HCl,C为AgNO3,D为BaCl2,E为NaHSO4,故答案为:Na2CO3;HC1;AgNO3;BaCl2;NaHSO4.
本题解析:
本题难度:一般
4、简答题 X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可).
(1)当X、Y均为金属时,X的化学式为______,Z为______(填名称).
(2)当X为非金属且为气体,Y为金属且为紫红色时,X的化学式为______,A的化学式为______.
(3)当X为金属、Y为非金属且为固体时,X与A反应的化学方程式为______.
(4)当X、Y均为非金属固体时,X与A反应的化学方程式为______.
参考答案:Z为绿色植物光合作用后的产物之一,应为O2,X+A→Y+B的反应为置换反应,X、Y为单质,A、B为氧化物,则
(1)当X、Y均为金属时,应为铝热反应,则X为Al,Z为氧气,故答案为:Al;氧气;
(2)当X为非金属且为气体,Y为金属且为紫红色时,Y为Cu,X应为H2,故答案为:H2;CuO;
(3)当X为金属、Y为非金属且为固体时,应为Mg和CO2的反应,反应的方程式为2Mg+CO2?△?.?2MgO+C,
故答案为:2Mg+CO2?△?.?2MgO+C;
(4)当X、Y均为非金属固体时,为C和SiO2的反应,反应的方程式为SiO2+2C?高温?.?Si+2CO,
故答案为:SiO2+2C?高温?.?Si+2CO.
本题解析:
本题难度:一般
5、填空题 (每空2分,共12分)已知金属氧化物A和金属单质B在高温条件下反应生成C和D的同时放出大量的热;将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色液体。
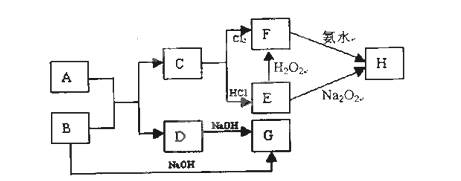
(1)红褐色液体中H粒子的直径大小范围?。
(2)写出D、E的化学式:D?、E?
(3)写出E的酸性溶液与双氧水反应的离子方程式?。
(4)写出F溶液中阳离子的检验方法:??离子方程式为?。
参考答案:(每空2分,其1 2分)
(1)? 1―100nm。
(2)D:Al2O3、E:? FeCl2
(3)? 2Fe2++H2O2+2H+=2Fe3++2H2O?。
(4)取少量F溶液与试管中,滴加几滴KSCN溶液,若变红,说明有Fe3+存在,否则没有。
Fe3++3SCN-=Fe(SCN)3。
本题解析:由图知H为氢氧化铁胶体,C为铁,D为Al2O3,A为Al,B为Fe2O3,E为FeCl2,F为FeCl3,G为NaAlO2.则⑶反应为2Fe2++H2O2+2H+=2Fe3++2H2O。Fe3+的检验可用KSCN溶液。
本题难度:一般