1��ѡ���� ���������������
A.1mol�κ����ʶ�����Լ6.02��1023��ԭ��
B.0.012kg12C����Լ6.02��1023��̼ԭ��
C.��ʹ��Ħ����ʾ���ʵ����ĵ�λʱ��Ӧ�û�ѧʽָ�����ӵ�����
D.���ʵ����ǹ��ʵ�λ�����߸�����������֮һ
�ο��𰸣�A
���������������������⿼�顰���ʵ������Ļ����������ʱӦ�������⣬ע��Ҫѡ���ǡ���ȷ�ġ����ǡ�����ġ�����ȷ�ġ������ڴ�����Ҫ������ѡ������ġ�
ѡ��A��������1mol�κ����ʶ�����Լ6.02��1023��ԭ�ӡ���1molH2Ӧ�ú���2��6.02��1023����ԭ�ӡ���Aѡ�����
ѡ��B����0.012kg12������̼ԭ���������������ֵΪ6.02��1023����1mol���κ����������еĸ����ʵ�������������٤������������ֵΪ6.02��1023����B��ȷ��
ѡ��C����ʹ�����ʵ���ʱ��Ӧ����ָ�����ӵ����࣬�硰1mol�⡱������������ģ������ģ�����ġ��⡱ָ����������������Ϊ�������ɱ�ʾ����ϵ�Ҳ�ɱ�ʾ���ϵģ���Ҳ������Ϊ��ԭ�ӡ�����Ħ����ʾ���ʵ����ĵ�λʱ�������û�ѧ����ָ�����ӵ����ࡣ
ѡ��D�����ʵ����ǹ��ʵ�λ�����߸�����������֮һ��7��������Ϊ���ȡ�������ʱ�䡢����ǿ�ȡ�����ǿ�ȡ��¶ȡ����ʵ�������
���㣺���ʵ���������٤������
�����������Ƕԡ����ʵ������͡�����٤�����������ۺϿ��顣����ʱӦ��ȷ���Եĸ���Լ�����������֮�����ϵ��
1�����ʵ�����n������ʾ����һ����Ŀ���ӵļ����塣��λ��mol
�����0.012kg12C������̼ԭ������
ע�⣺ʹ�����ʵ���ʱ�����û�ѧ����ָ�����ӵ����ࡣ
2������٤��������NA����1mol���κ����������еĸ����ʵ�������������٤������������ֵΪ6.02��1023��
ע�⣺����٤����������ֵ�����¶�ѹǿ�������ĸı���ı䡣
3������֮�����ϵ��N=n��NA?��NΪ������������
�����Ѷȣ�һ��
2��ѡ���� ����˵���������
A.�����ǻ���ɫ�ģ�����������ɫ��
B.������������ȼ��ʱ������ɫ����
C.�����ж������Ƶ���ˮ��Ư���ԣ��������Ӽ���Ҳ��Ư����
D.�����������Ļ������ֻ����ǿ�������²���Ѹ�ٻ��������Ȼ���
�ο��𰸣�D
�����������������������������ڹ��յ������¿���Ѹ�ٻ��������Ȼ��⣬���ڵ�ȼ�������£�����Ҳ������������ȼ�գ�������ɫ���棬ͬʱҲ�����Ȼ��⣬ѡ��D����ȷ������ѡ������ȷ�ģ���ѡD��
���㣺�����������仯���������
�������������ڻ��������⣬�ѶȲ�����Ҫ�Ǽ��ѧ�����ȼ��仯�������ʵ��������ճ̶ȣ�����ʶ���Եġ�
�����Ѷȣ���
3��ѡ���� ����˵����ȷ����
A.�ڱ�״���£�1molˮ�������22.4L
B.1molH2��ռ�����ԼΪ22.4L
C.�ڱ�״���£�NA��������ռ�����ԼΪ22.4L
D.�ڱ�״���£�1molNH3��CO���������ռ�����ԼΪ22.4L
�ο��𰸣�D
���������������A��������Ħ�������ʹ�÷�Χ�жϣ�
B��������Ħ�������ʹ�������жϣ�
C����������Ħ�������ʹ�÷�Χ�жϣ�
D��������Ħ������Ķ����жϣ�
���A������Ħ�������ʹ�÷�Χ�����壬ˮ��Һ�壬��A����
B���ڱ���£�1molH2��ռ�����ԼΪ22.4L��û��ǰ����������B����
C��δע�������ʵ�״̬������ȷ�����������C����
D���ڱ�״���£�1mol�κ�������ռ�����ԼΪ22.4L���κ������ֵ��������ָ������D��ȷ��
��ѡ��D
���������⿼���������Ħ�������ע������Ħ�������ʹ�÷�Χ����������ȷ���ⶨ���С��κΡ��ĺ��壮
�����Ѷȣ�һ��
4��ѡ���� NA���������ӵ�����������˵������ȷ����
A.5.6g?��ϩ�붡ϩ�Ļ�����к��Ҽ�����ĿΪNA
B.25��ʱ��pH=13��Ba��OH��2��Һ�к���OH-����ĿΪ0.1?NA
C.��Ũ���������ط�Ӧ��ÿ����21.3��������ת�Ƶ�����Ϊ0.5NA
D.����£�NO��O2��11.2?L��ϣ����û������ķ�������Ϊ0.75?NA
�ο��𰸣�C
���������������A����ϩ�붡ϩ�������еĦҼ���Ŀ��ͬ��
B��OH-����Ŀ����Һ������йأ�
C��������ʧȥ5mol���ӱ�1mol������õ�������3mol�������˹���ֻת����5NA�ĵ��ӣ�
D������£�11.2L��������ʵ���Ϊ0.5mol���ʻ������������ʵ���Ϊ1mol������һ�������������ܷ�����Ӧ��
���A��������ϩ�붡ϩ�������еĦҼ���Ŀ��ͬ��������ж�5.6g?��ϩ�붡ϩ�Ļ�����еĦҼ���Ŀ����A����
B����֪����Һ�����������OH-����Ŀ����B����
C��6HCl+KClO3�TKCl+3Cl2��+3H2O��ת��ֻ���㵥��ģ�������ʧȥ5mol���ӱ�1mol������õ�������3mol�������˹���ֻת����5NA�ĵ��ӣ�21.3�����������ʵ�����0.3mol����ת�Ƶ�����Ϊ0.5NA����C��ȷ��
D��NO��O2�ڱ���·�Ӧ����NO2�����ݷ�Ӧ�Ļ�ѧ����ʽ���Լ�������ɵ�NO2Ϊ0.5mol��ʣ���O2Ϊ0.25mol����������ܵ����ʵ���Ϊ0.75mol����NO2����һ��ƽ�⣺2NO2 N2O4������ƽ��Ĵ��ھ�ʹ������ܵķ�����С��0.75mol����D����
N2O4������ƽ��Ĵ��ھ�ʹ������ܵķ�����С��0.75mol����D����
��ѡC��
���������⿼�鰢���ӵ���������Ŀ�Ѷ��еȣ�ƽʱע��֪ʶ�Ļ��ۣ�
�����Ѷȣ�һ��
5��ѡ���� ��NAΪ�����ӵ�������ֵ������������ȷ����
A.25�棬pH=1��ϡ�����к��е�H+��Ϊ0.1NA
B.��״���£�224?mL?ˮ���еĵ�����Ϊ0.1NA
C.���³�ѹ�£�0.56?L�����к��еĹ��ۼ���Ϊ0.1NA
D.0.15?mol?NO2��ˮ��ȫ��Ӧʱת�Ƶĵ�����Ϊ0.1NA
�ο��𰸣�D
���������������A��pH=1��ϡ������Һ��H+��Ũ��Ϊ0.1mol/L����Һ�����δ֪������ȷ��H+�����ʵ�����
B����״���£�ˮΪҺ�壬����ʹ������Ħ�������
C�����³�ѹ�£�����Ħ���������22.4L/mol��
D�����ݷ�Ӧʽ��������NO������NO�����ʵ�������ת�Ƶ�����Ŀ��
���A��pH=1��ϡ������Һ��H+��Ũ��Ϊ0.1mol/L������Һ�����Ϊ1L�����е���Һ��H+��Ϊ0.1NA��������Һ���δ֪������ȷ��H+�����ʵ���Ϊ0.1mol����A����
B����״���£�ˮΪҺ�壬����ʹ������Ħ�������224?mLˮ�����ʵ���Զ����0.01mol����B����
C�����³�ѹ�£�����Ħ���������22.4L/mol��0.56?L��������ʵ���Ϊ����0.025mol�����й��ۼ�����0.1NA����C����
D�����ݷ�Ӧʽ3NO2+2H2O=2HNO3+NO��֪������NOΪ0.15mol��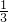 =0.05mol����Ӧ��NԪ�ػ��ϼ���+4�۽���ΪNO+2�ۣ���ת�Ƶ�����ĿΪ0.05mol����4-2������NAmol-1=0.1NA����D��ȷ��
=0.05mol����Ӧ��NԪ�ػ��ϼ���+4�۽���ΪNO+2�ۣ���ת�Ƶ�����ĿΪ0.05mol����4-2������NAmol-1=0.1NA����D��ȷ��
��ѡD��
���������⿼�鳣�û�ѧ�������йؼ��㣬�ѶȲ���ע������Ħ�������ʹ�����������
�����Ѷȣ�����