1、选择题 工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:
CuO+2HCl=CuCl2+H2O
FeO+2HCl=FeCl2+H2O
已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.除去溶液中的Fe2+,可以采用的方法是? ( )
A.直接加碱,调整溶液pH≥9.6
B.加纯铜粉,将Fe2+还原出来
C.先将Fe2+氧化成Fe3+,再调整pH在3~4
D.通入硫化氢,使Fe2+直接沉淀
参考答案:C
本题解析:依据题意,应先把Fe2+氧化为Fe3+,然后再调节溶液的pH值,使Fe3+转化为Fe(OH)3除去,故C正确。
本题难度:简单
2、填空题 某同学实验探究氨气的还原性并进行系列实验。
(1)将光亮的紫红色铜丝绕几圈后,在酒精灯火焰上加热,等铜丝变黑后,趁热将铜丝插入疏松的氯化铵晶体里,即刻发现有白色烟雾生成,拿出铜丝后,铜丝又转变为光亮的紫红色。在焊接铜器时用氯化铵除去铜器表面的氧化铜即利用了该原理,请完成该反应:

(2)利用下列装置,进行与金属氧化物MxOy反应生成M、H2、H2O,通过测量生成水的质量来测定M的相对原子质量。a中试剂是浓氨水。
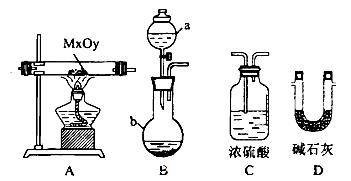
①仪器a的名称为__________,仪器b中装人的试剂可以是____________.
②按气流方向正确的装置连接顺序为(填序号,装置可重复使用):___________。
③实验结束时,应首先__________(填序号)。
I.熄灭A装置的酒精灯
II.停止从a中滴加液体
④若实验中准确称取金属氧化物的质量为mg,完全反应后,测得生成水的质量为ng,则M的相对原子质量为__________(用含X、y、m、n的式子表示)。
(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶液没发生明显变化。推测该固体成分可能是(将化学式填人下表,你认为有几种可能填几种)。

参考答案:(1)4CuO + 2NH4Cl="3Cu" +CuCl2 + 4H2O 。(2)①分液漏斗,,氢氧化钠或碱石灰②BDADC③实验结束时,应首先停止从a中滴加液体,没有必要有多余的氨气制备出。④(18m-16n)y/nx。(3)F铁,或者是铁和三氧化二铁
本题解析:(1)根据化合价升降法进行配平,可得4CuO + 2NH4Cl="3Cu" +CuCl2 + 4H2O 。(2)①仪器a的名称为分液漏斗,仪器b中装人的试剂可以是氢氧化钠或碱石灰,通过吸收水有利于制备出氨气。②从发生装置中出来的氨气带有水份,必须要进行干燥,故B接D,D接A,吸收反应生成的水要用D装置,最后空气中的水不能进入到D中,故要用到C。③实验结束时,应首先停止从a中滴加液体,没有必要有多余的氨气制备出。④由MXOY? ---Y H2O 关系,求得M的相对原子质量为(18m-16n)y/nx。(3)若金属氧化物MxOy为Fe2O3,将反应后固体溶于稀硫酸,然后滴加KSCN溶液没发生明显变化。说明溶液中没有三价铁离子,反应后的固体成分可能全是铁,或者是铁和三氧化二铁,因为Fe +2 Fe3+ = 3Fe2+。
本题难度:一般
3、填空题 将一块铜板浸泡在一定浓度的FeCl3溶液中一段时间后取出,得到一混合溶液,某校化学兴趣小组的同学为分析该混合溶液的组成,进行了如下实验:
①取50.0mL混合溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为86.1 g;
②另取50.0mL混合溶液,向其中加入1.40 g铁粉,结果铁粉全部溶解但未见固体析出;
③再取50.0mL混合溶液,向其中加入20.0 mL稀硝酸,得到一种无色气体,其体积换算成标准状况时为0.448 L;
请根据以上实验中得到的数据分析计算:
⑴?原FeCl3溶液物质的量浓度(反应过程中过程中溶液体积的变化忽略不计);
⑵?所得混合溶液中c(Cu2+)的取值范围;
⑶?若要进一步求得混合溶液中c(Cu2+)的具体数值,在只单独使用AgNO3溶液、铁粉
或稀硝酸的前题下,还可测出哪些数据,必须进行哪些实验?
参考答案:⑴?原FeCl3溶液中c(FeCl3)=
⑵50.0mL混合溶液中n?(Cu2+)的取值范围为:[0.600?mol/L,1.50?mol/L]
⑶?还可测出50.0mL混合溶液中n?(Fe2+)的值,应进行的实验是向50.0mL混合溶液中加入足量的稀硝酸,测出生成的气体体积(标准状况)。
本题解析:⑴?解:由I得50.0mL混合溶液中c(Cl-)=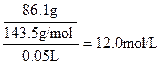 ?
?
所以原FeCl3溶液中c(FeCl3)= ?
?
⑵?解:Ⅱ中加入1.4gFe无固体剩余,即发生的反应为:Fe+2Fe3+=3Fe2+
所以50.0mL混合溶液中至少含有Fe3+: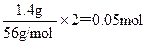 ?
?
Ⅲ中加入20.0mL稀硝酸后产生的气体为NO,反生的反应为
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
即50.0mL混合溶液中至少含有Fe2+: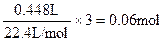 ?
?
50.0mL混合溶液中根据铁元素守恒有:
n?(Fe2+)?+?n?(Fe3+)?=?4.0?mol/L×0.05L=?0.20?mol?
根据电荷守恒有:3n?(Fe3+)+2n?(Fe2+)+2n?(Cu2+)=n?(Cl-)=
当n?(Fe3+)?有最小值时,n?(Fe2+)、n?(Cu2+)有最大值,且由上述两等式可求得
n?(Cu2+)的最大值为0.075?mol?
当n?(Fe2+)有最小值时,n?(Fe3+)?有最大值,n?(Cu2+)有最小值,同样可求得
n?(Cu2+)的最小值为0.03?mol?
所以,50.0mL混合溶液中n?(Cu2+)的取值范围为:[0.600?mol/L,1.50?mol/L]
⑶?解:还可测出50.0mL混合溶液中n?(Fe2+)的值,应进行的实验是向50.0mL混合溶液中加入足量的稀硝酸,测出生成的气体体积(标准状况)。
本题难度:一般
4、计算题 用黄铜矿炼铜按反应物和生成物可将总反应可以写成:
CuFeS2 + SiO2 + O2→ Cu + FeSiO3 + SO2
事实上冶炼反应是分步进行的。(1)黄铜矿在氧气作用下生成硫化亚铜和硫化亚铁;(2)硫化亚铁在氧气作用下生成氧化亚铁,并与二氧化硅反应生成矿渣;(3)硫化亚铜与氧气反应生成氧化亚铜;(4)硫化亚铜与氧化亚铜反应生成铜。
1)?写出上述各个分步反应(1,2,3,4)的化学方程式。
2)?给出总反应方程式的系数。
3)?据最新报道, 有一种叫Thibacillus ferroxidans的细菌在氧气存在下可以将黄铜矿氧化成硫酸盐。反应是在酸性溶液中发生的。试写出配平的化学方程式。
4)?最近我国学者发现,以精CuFeS2矿为原料在沸腾炉中和O2 (空气)反应, 生成物冷却后经溶解、除铁、结晶,得到CuSO4・5H2O,成本降低了许多。实验结果如下:
沸腾炉温度/℃
| 560
| 580
| 600
| 620
| 640
| 660
|
生
成
物
| 水溶性Cu/%
| 90.12
| 91.24
| 93.50
| 92.38
| 89.96
| 84.23
|
酸溶性Cu/%
| 92.00
| 93.60
| 97.08
| 97.82
| 98.16
| 98.19
|
酸溶性Fe/%
| 8.56
| 6.72
| 3.46
| 2.78
| 2.37
| 2.28
|
回答如下问题:
(1) ?CuFeS2和O2主要反应的方程式为:
(2) ?实际生产过程的沸腾炉温度为 600~620℃。控制反应温度的方法是:
(3) ?温度高于600~620℃生成物中水溶性Cu (%)下降的原因是:
参考答案:(1)2CuFeS2 + O2 =Cu2S + 2FeS +SO2?(1分)
(写S、SO3不写SO2不得分)
FeS + O2 =" FeO" + SO2?(1分)
(写S、SO3不写SO2不得分)
FeO + SiO2 = FeSiO3?(1分)?
(写其他产物不得分)
2Cu2S + 3O2 = 2Cu2O+ 2SO2? (1分)
(写S、SO3不写SO2不得分)
Cu2S+ 2Cu2O =" 6Cu" + SO2 ?(1分)
(写S、SO3不写SO2不得分)
不配平不得分。
(2)2CuFeS2 + 2SiO2 + 5O2 =" 2Cu" + 2FeSiO3 + 4SO2
(3)4CuFeS2 + 2H2SO4 + 17O2 = 4CuSO4 + 2Fe2(SO4)3 + 2H2O? (4分)
(注:不写硫酸铁而写硫酸亚铁给一半分)
(4)(1) 4CuFeS2 + 17O2 = 4CuSO4 + 2Fe2O3 + 8SO2? (4分)
(2) ?控制加入CuFeS2的速度,因CuFeS2与O2反应放热。? (2分)
(3) ?CuSO4 =" CuO" + SO3?(2分) ?
?(答SO2 + 1/2O2不扣分)
(注:(1)的反应产物不写氧化铁写氧化亚铁或四氧化三铁也可以给一半分。
虽然实际反应产物是氧化铁, 但对中学生, 做出正确判断根据可能不足。)
本题解析:本题由三个相互独立的问题组成,可以认为是三个题,占总分的较大比例,但由于都是有关黄铜矿的利用问题,因而被编在一起,而且多少相互之间可以起到“条件不同反应不同”的关联作用。与前两题相比,本题的第一部分比较简单,好像是命题人考虑着对前面的试题可能解答得不好的学生起一点安抚鼓励作用。写四个分步反应的方程式的考核点只是把题面的表述转换成化学方程式,但题面并没有指出生成物中的硫的形态。根据中学化学知识,可以想见它是SO2,大多数学生应该不会写错。其中第四个反应就是所谓“冰铜”反应,比较特殊,但试题已经告诉大家反应产物的含铜物质应该只有一种,即金属铜,这就降低了难度,可见应答时永远不应离开试题提供的知识背景。
问题(2)配平总方程式的系数,比较费事,考查机敏。配平的方法很多,条条大路通罗马。比较简单的是不管黄铁矿里的铜、铁和硫应当是什么价态的,假设铁是+2价的,铜也是+2价的,硫是-2价的,这样,铁在反应后价态不变,就省事多了。这种假设不会出现错误,其原因是氧化还原的电子得失总数是一定的。
问题(3)也是写方程式,熟悉过去竞赛试题的选手可能觉得似曾相识,但并非陈题。根据给出的信息,不难首先得出这样的结论:反应得到的溶液由CuSO4和Fe3(SO4)2组成。因为有氧气参加反应,铜和铁均应成水溶液中的稳定高价,似不会弄错。考虑到学生可能的错误,判分标准比较松。这个反应的关键是产物里要添硫酸根,为此题面对反应的条件作了说明:酸性溶液;但为避免暗示过多,没有说要加硫酸。
分析应答结果,许多学生因不会正确书写离子方程式和分子方程式二而失分。他们写的方程式是“非驴非马”的既非离子方程式又非分子方程式的“混杂”方程式。这中错误是严重的,不利于今后的学习,不能给分。我们建议正常课堂教学要针对学生这种错误来训练。
问题(4)比前面的试题更推进一步,信息是以表格中的数据的形式间接地呈现的。表格用沸腾炉的温度首先排除学生对“沸腾”二字的可能误解,这里的“沸腾”并非意味着炉子里有水之类的溶剂(试题设计人估计学生并没有固体在上行气流冲击下如同沸腾的那种工业反应器的概念,并没有考察这样专门的知识,但中学老师说,沸腾炉的概念在讲黄铁矿制硫酸中讲到的)。表格还用水溶性铜、酸溶性铜和酸溶性铁的信息表明,沸腾炉里的含铁产物肯定不是铁的硫酸盐,因为并没有说有水溶性铁,因而可以得出结论:燃烧产物中的铁是以氧化物的方式存在的。(这正是与本题一开始的传统冶炼反应不同之处,否则为什么是最新成果,而且是我国学者的成果呢?)至于铁的氧化物为什么随温度升高溶于酸的程度降低?本题没有要求作答。这个知识大大超过中学生的知识水平。其实,氧化物的酸溶性随煅烧或烧结温度升高而下降是一个普遍现象。例如用作炼钢炉衬里的氧化镁就是经过高温烧结的酸溶性很差的氧化物,还可以举出的典型物质是刚玉(Al2O3),用作坩埚等高温容器,酸溶性极差。这些化学知识似应在优秀中学生中间做点普及,不要以为碱性或两性金属氧化物都易溶于酸(热力学上要溶,动力学上不溶!)。本题给分充分考虑了中学生的知识水平,比较宽松。
本题难度:一般
5、选择题 铁有多种价态,将14.4 g草酸亚铁(FeC2O4)与空气隔绝加热分解,最终得到7.2 g铁的氧化物,则该铁的氧化物是(?)
A.Fe3O4
B.Fe2O3
C.FeO
D.FeO和Fe3O4
参考答案:C
本题解析:方法一:因隔绝空气,FeC2O4中的C、O两种元素在这种条件下不具有氧化性,铁的价态不会改变,仍是+2价,即FeO。
FeC2O4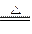 FeO+CO↑+CO2↑
FeO+CO↑+CO2↑
方法二:FeC2O4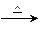 FexOy
FexOy
144? M
14.4 g? 7.2 g
M=72,即铁的氧化物的化学式为FeO。
方法三:质量守恒(铁元素),由题意推得在所得铁的氧化物中,m(Fe)="14.4" g×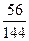 ="5.6" g
="5.6" g
m(O)="7.2" g-5.6 g="1.6" g
所以n(Fe)∶n(O)=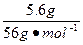 ∶
∶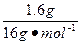 =1∶1
=1∶1
故该氧化物的化学式为FeO。
本题难度:简单