1������� �������һ�ֳ��õ��̬���ʣ��±�������炙���Ʒ�ʵ���Ҫָ�꣮?
ָ��
��Ŀ | �ŵ�Ʒ | һ��Ʒ | �ϸ�Ʒ
���
��ɫ�ᾧ���ɼ���е���� | �ɼ���е����
����N������
��21.0%
��21.0%
��20.5%
|
ij��ѧ�о���ѧϰС��Ϊ����ũҵ��������ijũ��Ʒ�̵���۵�һ��Ʒ����炙��ʵ�Ʒ�ʽ���̽��
��?
[�۲����]
?������炙����ɼ���е���ʣ�?
[ʵ��̽��]
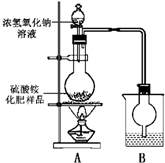
?����ͼ��ʾװ�ý���ʵ�飮?
��1����ƿ�ڷ�����Ӧ�����ӷ���ʽΪ��______�ձ���ʢ�ŵ��Լ������______���Ũ���ᡱ����ϡ���ᡱ��ˮ����
��2��ʵ������У�������ƿ�м�������Ũ����������Һ����ּ��ȵ�ԭ����______
[��������]
��ͬѧ�����ݴ�ʵ���õ����ݣ���������炙��ʵĺ���������ƫ�ߣ���Ϊʵ��װ���д���һ������ȱ���ǣ�______
��ͬѧ��ʵ��װ���л�������һ������ȱ���ǣ�______
������ҳ������һ����Ϊ����Լס�����λͬѧָ����ʵ��װ���д��ڵ�����ȱ�ݣ���Ľ�ʵ��װ�ã����½���ʵ��
[̽������]
��ȡ13.5g����炙�����Ʒ���øĽ����ʵ��װ�����½���ʵ�飬���ʵ���Bװ������3.4g���ó�̽������Ϊ______��
�ο��𰸣���1������狀��������Ʒ�Ӧ���������ơ�ˮ�Ͱ�������Ӧ����ʽΪ����NH4��2SO4+2NaOH?��?.?Na2SO4+2NH3��+2H2O�����ӷ�ӦΪNH4++OH-?��?.?NH3��+H2O���ձ���ʢ�ŵ��Լ����������հ����ģ�������ϡ���ᣬ
�ʴ�Ϊ��NH4++OH-?��?.?NH3��+H2O��ϡ���
��2���������Ƶ�Ũ��Һ�������������������Ũ�ȴ���笠����ӷ�Ӧ������������Ũ�ȴ����¶ȸߣ���Ӧ�ٶȿ죬���ԣ���������Ũ����������Һ����ּ��ȣ���ʹ����麟�ַ�Ӧ��ȫת��ΪNH3��
�ʴ�Ϊ��ʹ����麟�ַ�Ӧ��ȫת��ΪNH3��
[��������]��ȡ����Ϊ����������Һ������粒��巴Ӧ���������ɵİ����к���ˮ�������氱��һͬ����Bװ���У�Ӱ�찱����������Ӱ�캬�����IJⶨ������������һ������װ�ã���Ӧװ���и����ֶ������������轫��Ӧװ���в����İ����ϳ���
�ʴ�Ϊ��A��Bװ�ü�ȱһ������װ�ã�ȱ�ٸϾ���Ӧװ���в���������װ�ã�
[̽������]
���ص�3.4gΪ�����������13.5g��Ʒ�к��У�NH4��2SO4������Ϊx��
��NH4��2SO4+2NaOH?��?.?Na2SO4+2NH3��+2H2O
?132? ?34
? x? ? ?3.4g
132��34=x��3.4g? ��ã�x=13.2g? 13.2g132g/mol=0.1mol����0.2mol��ԭ�ӣ���������Ϊ2.8g��
2.8g13.5g��100%=20.7%? 20.5%��20.7%��21.0%��Ϊ�ϸ�Ʒ��
�ʴ�Ϊ���û���Ϊ�ϸ�Ʒ��
���������
�����Ѷȣ�һ��
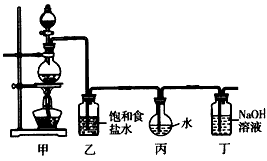
2��ʵ���� ����ͼ��ʾ��װ����ȡ�϶����ı�����ˮ��̽��������ˮ���й����ʡ�
�ش��������⣺
(1)д��װ�ö��з����Ļ�ѧ��Ӧ����ʽ��_____________________��
(2)֤����ˮ�ѱ��͵�������________________��
(3)��ȡ����ʱ��װ�ñ��е�Һ�庬�е�����________________���������ű�ʾ����
(4)�ⶨ������ˮ��pH������____������ȥװ���ң�ֱ�ӽ�װ�üͱ���������������ʵ��ⶨ�����Ӱ����____________________��
(5)������ˮ��ʯ��ʯ��Ӧ����ȡ��ŨHClO��Һ�ķ���֮һ����ͼ��ʾ��
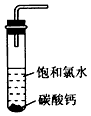
�����Թ��м�������Ŀ�״̼��ƣ��ټ���Լ20 mL������ˮ����ַ�Ӧ�����������ݲ�������Һ����ɫ��ȥ��
����ˣ�����Һ������ɫ�����ϣ����������ˮ��Ư���Ը�ǿ��
��Ϊ��ȷ����Ӧ�������Һ��Ϊ���ݣ��ֱ��������ʵ�飺
��һ����ʯ��ˮ��ϣ���������������ɫ������
�ڶ�����ϡ�����ϣ���������������ɫ���壻
�������ݼ��ȣ�������Һ��������д�����ɫ�������������⣬����ʵ���в�������ɫ�����ΪCO2���塣
�����ñ�����ˮ��ʯ��ʯ��Ӧ�Ʊ���ŨHClO��Һ��ԭ����____��
����������ʵ�����֪�������Һ�е����ʳ�CaCl2��HClO�ͼ������������⣬������_____________��д��ѧʽ����
��д��������У��ڶ�����Һ���������ӷ�Ӧ����ʽ��____________________��
�ο��𰸣�(1)Cl2+2NaOH=NaCl+NaClO+H2O
(2)����Һ��ʻ���ɫ�����ϲ��ռ�ʻ���ɫ���л���ɫ������붡��
(3)H2O��Cl-��H+��Cl2��HClO��OH-��ClO-
(4)��pH��ֱ�Ӳⶨ����pH��ֽ�ⶨ�����֣��������Ȼ���δ�����ᵼ���Ƶõ���ˮ������ǿ����õ�pHƫС
(5)�ٱ�����ˮ�д�������ƽ�⣺Cl2+H2O HCl+HClO��Ӧ���������ʯ��ʯ������Һ�е����ᷴӦ��ʹ����Ũ�ȼ�С��ƽ��������Ӧ�����ƶ�����������HClO
HCl+HClO��Ӧ���������ʯ��ʯ������Һ�е����ᷴӦ��ʹ����Ũ�ȼ�С��ƽ��������Ӧ�����ƶ�����������HClO
��Ca(HCO3)2
��H++HCO3-=H2O+CO2��
���������
�����Ѷȣ�һ��
3��ѡ���� ����ʵ����Ʒ����У����е���
A���ü�������ͭ�۵ķ�����ȥCu(NO3)2��Һ�л��е�AgNO3
B����ij��ɫδ֪��Һ�н�����BaCl2��Һ���Լ���δ֪��Һ��SO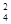 ��
��
C����ϴ��ƿ�е�NaOH��Һ��ȥCO2�л��е�HCl����
D���Ⱥ����ӷ�̪��Һ��BaCl2��Һ�������ᡢ���ᡢ�����ơ��������ƺ������������ɫ��Һ����
�ο��𰸣�A
���������
��ȷ�𰸣�A
A��Cu��2Ag��=2Ag��Cu2�� ��B��Ҳ������Ag�� ��C��CO2Ҳ�����գ�D��HCl��KNO3������
�����Ѷȣ�һ��
4��ʵ���� (16��)��֪��������茶���Ϊdz��ɫ��������ˮ���������Ҵ�����ˮ�е��ܽ�ȱ�FeSO4��(NH4)2SO4��ҪС����ˮ�⣻���л�ԭ�ԣ��������������ȶ���
�����ǽ��̷�(FeSO4?7H2O)���������������ʵ�����Ͽ��Ƶ�Ħ���ξ��������ͼ��������ͼ�ش�
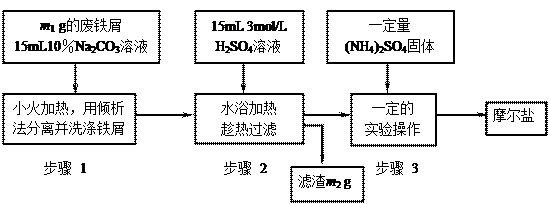
(1)Ϊ��������м��������ۣ���10��Na2CO3��Һ��ϴ���������ӷ���ʽ��ʾNa2CO3��Һ�ʼ��Ե�ԭ��? ��?��
(2)����1�в����������������м�������ʺ�������������? ��?��
A.�����Ŀ����ϴ�? B.�������׳���? C.�����ʽ�״? D.��������״
(3)����2 ����м������Ŀ����(�����ӷ���ʽ��ʾ)��?��?������2����Һ���ȹ��˵�ԭ����? ��?��
����м������Ŀ����(�����ӷ���ʽ��ʾ)��?��?������2����Һ���ȹ��˵�ԭ����? ��?��
(4)����3�У�����(NH4)2SO4�����Ӧ ���ȵ�? ��?ʱ��ֹͣ���ȡ��辭����ʵ�����������? ��?����������������ѹ����(�����)�ȵõ���Ϊ? ��?�ľ��塣
���ȵ�? ��?ʱ��ֹͣ���ȡ��辭����ʵ�����������? ��?����������������ѹ����(�����)�ȵõ���Ϊ? ��?�ľ��塣
(5)����װ�õ������У�? ��?��? ��?����ȫƿ����������ɡ�
(6)��Ʒ��Fe2���Ķ���������
�Ƶõ�Ħ������Ʒ���������м�������Fe3+��Ϊ�˲ⶨĦ���β�Ʒ��Fe2+�ĺ� ����һ���������������KMnO4��Һ�ζ��ķ�����
����һ���������������KMnO4��Һ�ζ��ķ�����
��ȡ4.0 g��Ħ������Ʒ������ˮ������������ϡ���ᡣ��0.2 mo1/L KMnO4��Һ�ζ�������Һ��Fe2+ȫ��������ʱ������KMnO4��Һ��� 10.00 mL��
������ɵζ������з��������ӷ���ʽ��
?Fe2����?MnO4����(? )="?" ?Mn2����?Fe3����?H2O
�ڱ�ʵ���ָʾ��? ��?��
A.��̪? B.����? C.ʯ��? D.����Ҫ
��KMnO4��Һ����? ��? (��ʽ����ʽ)�ζ�����
���յ���ɫ�ı仯��? ��?��
�ݲ�Ʒ��Fe2+����������Ϊ? ��?��
 (7)��25��ʱ����ͬ���ʵ���Ũ�ȵ�(NH4)2 CO3��(NH4)2SO4��Ħ������������Һa,b,c����笠�����Ũ����С���������˳��Ϊ��? ��?��(��a,b,c�ش�)
(7)��25��ʱ����ͬ���ʵ���Ũ�ȵ�(NH4)2 CO3��(NH4)2SO4��Ħ������������Һa,b,c����笠�����Ũ����С���������˳��Ϊ��? ��?��(��a,b,c�ش�)
�ο��𰸣���16�֣�ÿ��1�֣�(1)? CO32�� +H2O  HCO3�� + OH��
HCO3�� + OH��
��2�� A��B
��3��Fe + 2Fe3�� = 3Fe2������ֹ��Һ��ȴʱ��������������������ʧ��
��4����Һ������־�Ĥ������Ũ������ȴ�ᾧ�������5������©��������ƿ��
��6��5 Fe2����1 MnO4������ 8H+?�� = ?1 Mn2����?5 Fe3����?4 H2O
D?����ʽ����Һ���ޣ�dz �̣�ɫ��Ϊdz��ɫ��������ڲ���ɫ��14%��
�̣�ɫ��Ϊdz��ɫ��������ڲ���ɫ��14%��
��7��a<b<c
�����������
�����Ѷȣ�һ��
5��ʵ���� ��12�֣�ij����С��Ϊ�˲ⶨij�Ȼ��ȣ�SrCl2����Ʒ�Ĵ��ȣ���������·�����
��ȡ1.0g��Ʒ�ܽ�������ˮ�У������м��뺬AgNO32.38g��AgNO3��Һ����Һ�г�Cl�D�⣬����������Ag+��Ӧ���ɳ��������ӣ���Cl�D����ȫ��������Ȼ���ú�Fe3+����Һ��ָʾ������0.2mol/L��NH4SCN����Һ�ζ�ʣ���AgNO3��ʹʣ���Ag+��AgSCN��ɫ��������ʽ�������Բⶨ�Ȼ�����Ʒ�Ĵ��ȡ���ش��������⣺
��1���ζ���Ӧ�ﵽ�յ��������?��
��2��ʵʩ�ζ�����Һ�Գ�?��ѡ����ԡ��������ԡ����ԡ���Ϊ�ˣ���
?���ѧʽ���Լ��ɴﵽ��һĿ�ģ�
��3�����յ㵽��֮ǰ�ĵζ������У����ֳ����������������Ag+���費�Ͼ���ҡ����ƿ�������ʹn (Cl��)�IJⶨ���?��ѡ�ƫ�ߡ�����ƫ�͡�����Ӱ�족����
��4�������յ�����������ҡ����ƿ������ʱ���þ���ҡ�����Լ�����������������ʹn (Cl��)�ⶨֵƫ�ͣ���˵�����ߵ��ܽ�ȣ�AgCl ??AgSCN���������������
��5������Fe3+����Һ��ָʾ������NH4SCN����Һ�ζ�ʣ���AgNO3ʱ����ȥ����Ũ�ȵ�NH4SCN��Դ:91������ 91EXAm.org��Һ20.0mL����ԭ�Ȼ�����Ʒ�Ĵ���Ϊ?��
�ο��𰸣���1����Һ����ɫ��ΪѪ��ɫ?��2������?HNO3
��3��ƫ��?��4����?��5��79.5%
�����������1�������������ܺ�NH4SCN��Ӧʹ��Һ�Ժ�ɫ�������յ�ʱ����������Һ����ɫ��ΪѪ��ɫ��
��2�������ڼ�����Һ�������Ӻ����������γ��������������������ҺӦ�������ԡ����ڲ����������ʣ��������������ữ��
��3�������������������Ag+�����Իᵼ�²��������ӣ��Ӷ����²ⶨ���ƫ�ߡ�
��4����������ʹn (Cl��)�ⶨֵƫ�ͣ���˵��������ת��ΪAgSCN����������Ȼ������ܽ�ȴ���AgSCN�ġ�
��5������0.2mol/L��NH4SCN�����ʵ�����0.004mol����������2.38g��170g/mol��0.014mol�����Ժ������ӷ�Ӧ����������0.014mol��0.004mol��0.01mol������Ȼ��ȵ�������0.005mol��156g/mol��0.795g������ԭ�Ȼ�����Ʒ�Ĵ���Ϊ79.5%��
�����Ѷȣ�һ��