|
�߿���ѧ֪ʶ���ܽᡶ��ѧƽ�⡷���⼼�ɣ�2019�����°棩(��)
2019-07-04 01:06:03
�� �� �� ��
|
1��ѡ���� ���淴ӦmA(g)��nB(g) pC(g)+qD(g)��v-tͼ��������ͼ�����������������䣬ֻ���ڷ�Ӧǰ������ʵĴ���������v-tͼ��������ͼ����a1��a2��a1��a2��b1��b2��b1��b2 ��t1��t2��t1=t2 ����ͼ����Ӱ���������� ����ͼ����Ӱ���������������˵������ȷ����(����) pC(g)+qD(g)��v-tͼ��������ͼ�����������������䣬ֻ���ڷ�Ӧǰ������ʵĴ���������v-tͼ��������ͼ����a1��a2��a1��a2��b1��b2��b1��b2 ��t1��t2��t1=t2 ����ͼ����Ӱ���������� ����ͼ����Ӱ���������������˵������ȷ����(����)
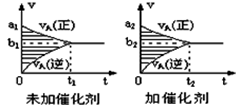
A���ڢۢݢ�
B���٢ܢޢ�
C���ڢܢݢ�
D���٢ۢޢ�
|
�ο��𰸣�C
���������ʹ�ô����ķ�Ӧ�����ʿ죬����ƽ���ʱ��̣�����a1��a2��t1��t2��ƽ��ʱ�ķ�Ӧ���ʿ죬����b1��b2����Ϊ������ƽ����Ӱ�죬��������Ũ�ȵĸı�����ͬ������Ӱ�����ͬ�����Դ�ѡC��
���㣺���黯ѧƽ����ʹ�ô����벻ʹ�ô����ıȽ�
�����Ѷȣ�һ��
2������� ��һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g����H2��g��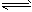 CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±� CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±�

�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��_________��
��2���÷�ӦΪ_________��Ӧ��ѡ����ȡ��������ȡ�����
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������_________����ѡ�۷֣���
a��������ѹǿ����
b�����������c��CO������
c��������H2�������棨H2O��
d��c��CO2����c��CO��
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c��CO2����c��H2����c��CO����c��H2O�������жϴ�ʱ���¶�Ϊ
_________�档
�ο��𰸣���1��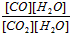
��2������
��3��bc
��4��830
���������
�����Ѷȣ�һ��
3��ѡ���� ��һ�������£���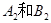 ��������ͨ���ܱ������У���Ӧ�� ��������ͨ���ܱ������У���Ӧ��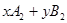 = = 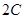 ���У� ���У�
2���Ӻ�Ӧ�������£�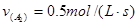 �� ��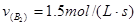 �� �� ����x��y��ֵ�ֱ�Ϊ��?�� ����x��y��ֵ�ֱ�Ϊ��?��
A��3��2
B��1��3
C��3��1
D��4��5
�ο��𰸣�B
�����������Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ�����x��y֮����1�U3.��ѡB��
�����Ѷȣ�һ��
4��ѡ���� ��һ�������£���ѧ��ӦN2+3H2?2NH3�ﵽƽ��״̬�ı�־Ϊ��������
A��������ƽ����Է�����������ʱ��仯
B��N2��H2��NH3��Ũ��֮��Ϊ1��3��2
C��N2���ٵ����ʺ�NH3���ɵ�����֮��Ϊ1��2
D���������Ϊ��ʼ�����һ��
�ο��𰸣�A����Ӧ��������Ļ�ѧ������֮�Ͳ���ȣ�������������䣬M=mn������������ƽ����Է�����������ʱ��仯��˵�����淴Ӧ������ȣ��ﵽ��ƽ��״̬����A��ȷ��
B��Ũ��֮�Ȳ����жϸ���ֵ�Ũ���Ƿ�仯�����淴Ӧ�����Ƿ���ȣ����ж��Ƿ�ﵽ��ƽ��״̬����B����
C�������ļ��ٺͰ��������ɶ�������Ӧ���ʣ����ж����淴Ӧ������ȣ���C����
D������Ӧ�������С�ķ�Ӧ���������Ϊ��ʼ�����һ�룬���жϸ���ֵ�Ũ���Ƿ��ٱ仯�����ж��Ƿ�ﵽ��ƽ��״̬����D����
��ѡ��A��
���������
�����Ѷȣ�һ��
5������� ��һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g��+H2��g��?

CO��g��+H2O��g���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t/�� | 700 | 800 | 830 | 1000 | 1200
K
0.6
0.9
1.0
1.7
2.6
|
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=______��
��2���÷�ӦΪ______��Ӧ������ȡ������ȡ�����
�ο��𰸣���1����ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮��������K=c(CO)?c(H2O)c(CO2)?c(H2)���ʴ�Ϊ��c(CO)?c(H2O)c(CO2)?c(H2)��
��2����ѧƽ�ⳣ���Ĵ�Сֻ���¶��йأ������¶ȣ�ƽ�������ȵķ����ƶ����ɱ���֪�������¶ȣ���ѧƽ�ⳣ������˵����ѧƽ�������ƶ����������Ӧ�������ȣ��ʴ�Ϊ�����ȣ�
���������
�����Ѷȣ�һ��
|