1��ʵ���� �̷���FeSO4?7H2O��������ȱ����ƶѪ����Чҩ��ijѧУ�Ļ�ѧ��ȤС���ͬѧ���̷����������µ�̽����
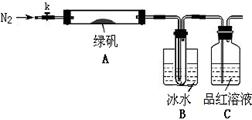
FeSO4?7H2O���Ʊ�
�û�ѧ��ȤС���ͬѧ��ʵ����ͨ������ʵ���ɷ���м������������ͭ�������������ʣ��Ʊ�FeSO4��7H2O���壺
�ٽ�5%Na2CO3��Һ���뵽ʢ��һ��������м���ձ��У����������ӣ�����������ȥ
Na2CO3��Һ��Ȼ����м��ˮϴ��2��3�顣
����ϴ�ӹ��ķ���м�м��������ϡ���ᣬ�����¶���50��80��֮������м�ľ���
�۳��ȹ��ˣ�����Һת�뵽�ܱ������У����á���ȴ�ᾧ��
�ܴ��ᾧ��Ϻ��˳����壬��������ˮϴ��2��3�Σ�������ֽ���������ɣ�
�ݽ��Ƶõ�FeSO4��7H2O�������һ��С���ƿ�У��ܱձ��档
��ش��������⣺
��1��ʵ�鲽��ٵ�Ŀ��������������������������������
��2��ʵ�鲽������Բ���������������������������������������
��3��Ϊ��ϴ�ӳ�ȥ������渽�ŵ���������ʣ�ʵ�鲽�������������ˮϴ�Ӿ��壬ԭ������������������������������������������ ��
������̽���̷���FeSO4��7H2O���ȷֽ�IJ���
��֪SO3���۵���16.8��C���е���44.8��C����С���������ͼ��ʾ��ʵ��װ�ã�ͼ�м��ȡ��г������Ⱦ�ʡ�ԣ���
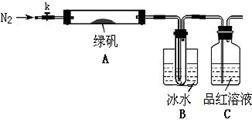
��ʵ����̡�
���������Ӻ��װ��A��B�����ԣ�
��ȡһ�����̷���������A�У�ͨ��N2������װ���ڵĿ������ر�k���þƾ��Ƽ���Ӳ�ʲ����ܣ�
�۹۲쵽A �й��������ɫ��B���Թ��ռ�����ɫҺ�壬C����Һ��ɫ��
�ܴ�A�з�Ӧ��ȫ����ȴ�����º�ȡ������Ӧ��������Թ��У����������ܽ⣬ȡ�������뼸��KSCN��Һ����Һ���ɫ��
����Bװ�õ��Թ��е��뼸��BaCl2��Һ����Һ����ǡ�
(4��ʵ��������
����1��B���ռ�����Һ����?��
����2��C����Һ��ɫ������֪��������?��
����3���ۺ���������ʵ��ۺܿ͢���֪�������һ����Fe2O3��
��ʵ�鷴˼��
��5����ָ����С����Ƶ�ʵ��װ�õ����Բ��㣺?��
��6���ֽ��Ĺ����п��ܺ�������FeO��ȡ����ʵ����������ܽ�����Һ�������Թ��У�ѡ��һ���Լ����𣬸��Լ�����ʵ���?��
a����ˮ��KSCN��Һ? b������KMnO4��Һ? c��H2O2? d��NaOH��Һ
�ο��𰸣������������ۣ�
��2��Ӧ����м��������Ӧ����Һ�б�������ʣ�ࣩ��������Һ�п�����Fe3+���ڣ�
��3���ñ�ˮϴ�ӿɽ���ϴ�ӹ�����FeSO4��7H2O����ģ�
��4��H2SO4��Һ��SO2��
��5����Cװ�ú�����һ��β������װ�ã�?
��6��b��
�����������1��̼������Һ�����м�ijɷ־����ܷ�Ӧ����ֻ��ȥ���۵����ã���2����Ϸ���м�ijɷֺͺ�ߵIJ����֪�����뱣֤����ʣ�࣬���ܱ�֤��Һ��û�������ӣ���3�������¶ȣ���С�̷����ܽ�ȣ���4��������������������ˮ�������ɣ���������������۵��֪����ˮ�ܽ����������ˮҺ������B�з�Ӧ�������C�������ɵĶ�������ʹƷ����Һ��ɫ����5����������Ҫ����β����������6��������������������������������������ɣ�Ҫ�����������Ĵ��ڣ��������������ӵĻ�ԭ�ԣ�ʹ���Ը��������Һ��ɫ����ѡb��
�����Ѷȣ�����
2��ѡ���� ��֪����Һ�з�����Ӧ��2Fe3+ + Cu=2Fe2+ + Cu2+������Fe��Cu��Fe2O3������ɵĻ���ﹲmg��ǡ���ܽ���100 mL 1. 00 moL/L�������С������ж�һ����ȷ����
[? ]
A��Fe2O3��������Χ����ȷ��
B��m��ֵ����ȷ��
C����Ӧ�пɹ۲쵽�������ݲ���
D����Ӧ�����Һ�μ�KSCN��Һ����Ѫ��ɫ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� �����йش�����������ȷ����(? )
A���۵�������ĵ�
B������ͬŨ�ȵ����ᷴӦ�������������ʱ������Ŀ�
C���ڳ�ʪ�����б��������ױ���ʴ
D�������Ũ�����пɶۻ�
�ο��𰸣�D
�������������������̼�ĺϽ����ںϽ���۵�ͨ��������һ��ɲ��ֵ��۵㣬��A�����������ᷴӦ���ڳ�ʪ�Ŀ����о��ȴ�����ö࣬��B��C�������ڳ�������Ũ���ᡢŨ�����з����ۻ���D��ȷ��
�����Ѷȣ���
4�������� ����п�Ͻ�8.5g����ϡH2SO4�У���ַ�Ӧ���Ƶ�0.300gH2����Ͻ���Fe��Zn�ĺ����ֱ�Ϊ���ٿˡ�?
�ο��𰸣�m (Fe)= 5.60g��m (Zn) =3.25g
���������������Ͻ��ƽ��Ħ����������Fe �� H2��Zn �� H2 ���Ͻ�� H2��
��Ͻ��ƽ��Ħ������Ϊ��8.5 g /��0.300/2��mol= 59.0g/mol��ƽ��������Ϊ59.0��

��Fe��Zn�ֱ����H2�����ʵ���֮��Ϊ6.0�U3.0 = 2�U1���Ӷ���֪�Ͻ���Fe��Zn�������ֱ�Ϊ��
m (Fe)= 56g/mol����0.300/2��mol��2/3 = 5.60g
m (Zn) = 65g/mol����0.300/2��mol��1/3 = 3.25g
�����Ѷȣ���
5��ѡ���� ��14gͭ���Ͻ���������һ��Ũ�ȵ�������Һ��Ӧ���ѷų����������״�������Ϊ1.12L��O2��Ϻ���ͨ��ˮ�У�ǡ��ȫ�������գ���Ͻ���ͭ������Ϊ
A��3.2g
B��4.8g
C��6.4g
D��10.8g
�ο��𰸣�A
�����������Ӧ�кϽ�ʧ���ӣ������õ��ӣ�����������Ȼ�����ᣬ����Ϊû�е��ӵĵ�ʧ
��ͭ�������ʵ����ֱ�Ϊx��y����64x+108y=14
�ɵ��ӵĵ�ʧ�غ�ã�2x+y=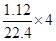
��ã�x=0.05mol? y=0.1mol
Ǧ������Ϊ3.2g
�����Ѷȣ�һ��