| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《铁的氧化物》高频试题巩固(2019年最新版)(六)
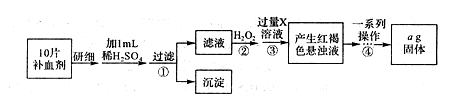 ①步骤④中一系列操作依次是:过滤、洗涤、______、冷却、称量。 ②假设实验过程中Fe无损耗,则每片补血剂含铁元素的质量______g(用含a的代数式表示)。 ③若步骤③加入X溶液的量不足,则最后测出每片补血剂含铁元素的质量将______(填“偏大,’.“偏小”或“不变”)。 参考答案:(1)除去废铁屑表面的油污(1分),倾倒法(1分) (2)趁热过滤(2分) 本题解析:(1)CO32-水解生成OH-,溶液显碱性,酯在碱性条件下完全水解,所以可用纯碱溶液除油污。铁是不溶于水的金属,要分离铁可以直接倾倒法。 本题难度:困难 4、选择题 在一定量的Fe、FeO、Fe2O3的混合物中,加入100mL、1.1mol/L的盐酸反应并放出标准状况下224mL气体,反应后溶液中阳离子只有Fe2+、H+,且溶液的pH=1(不考虑盐的水解及溶液体积的变化)。则反应后溶液Fe2+的物质的量浓度(mol·L-1)为 参考答案:B 本题解析:在一定量的Fe、FeO、Fe2O3的混合物中,加入100mL1.1mol/L的盐酸反应并放出标准状况下224mL气体,反应后溶液中阳离子只有Fe2+、H+,且溶液的pH=1,则反应后溶液为氯化亚铁和盐酸的混合液,根据题意及电荷守恒知,2c(Fe2+)+c(H+)=c(Cl-)。即2c(Fe2+)+0.1mol/L=1.1mol/L ,则反应后溶液Fe2+的物质的量浓度为0.5mol·L-1,选B。 本题难度:一般 5、选择题 将适量铁粉投入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是(? ) 参考答案:A 本题解析:设原Fe3+为x,已反应的Fe3+为y, 本题难度:简单 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《化学平衡》.. | |