1��ѡ���� ��һ���ܱ������н��з�Ӧ��2SO2(g)��O2(g) 2SO3(g)����֪��Ӧ������ijһʱ�̣�SO2��O2��SO3�ֱ���0.2mol/L��0.1mol/L��0.2mol/L������Ӧ�ﵽƽ��ʱ�����ܴ��ڵ�������?
2SO3(g)����֪��Ӧ������ijһʱ�̣�SO2��O2��SO3�ֱ���0.2mol/L��0.1mol/L��0.2mol/L������Ӧ�ﵽƽ��ʱ�����ܴ��ڵ�������?
A��SO2Ϊ0.4mol/L��O2Ϊ0.2mol/L
B��SO3(g)Ϊ0.4mol/L
C��SO2��SO3(g)��Ϊ0.15mol/L
D��SO2Ϊ0.25mol/L
�ο��𰸣�D
����������ɲ��ü�ֵ������ȫ��ת��Ϊ�������SO3��Ũ����0.4mol/L����ȫ��ת��Ϊ��Ӧ����SO2��O2��Ũ�ȷֱ�Ϊ0.4mol/L��0.2mol/L����Ϊ�ǿ��淴Ӧ������ѡ��A��B�����ܡ�����ԭ���غ��֪��SO2��SO3��Ũ��֮��Ӧ����0.4mol/L����CҲ�����ܡ�����D��
�����Ѷȣ���
2��ѡ���� �Կ��淴Ӧ4NH3(g)+5O2(g)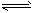 4NO(g)+6H2O(g)������������ȷ����
4NO(g)+6H2O(g)������������ȷ����
[? ]
A���ﵽ��ѧƽ��ʱ��4v��(O2)=5v��(NO)
B������λʱ��������xmolNO��ͬʱ������xmolNH3����Ӧ�ﵽƽ��״̬
C���ﵽ��ѧƽ��ʱ������Сѹǿ��������Ӧ���ʼ�С���淴Ӧ��������
D����ѧ��Ӧ���ʹ�ϵ��2v��(NH3)=3v��(H2O)
�ο��𰸣�A
���������
�����Ѷȣ�һ��
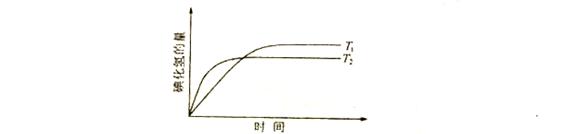
3��ѡ���� ���ܱյ������н������µķ�Ӧ��H2(G��I2(g) 2HI(g)�����¶�T1��T2ʱ�����������ʱ��Ĺ�ϵ����ͼ��ʾ������ͼ�����ȷ���ж���(? )
2HI(g)�����¶�T1��T2ʱ�����������ʱ��Ĺ�ϵ����ͼ��ʾ������ͼ�����ȷ���ж���(? )
A��T1��T2����H��0
B��T1��T2����H��0
C��T1��T2����H��0
D��T1��T2����H��0
�ο��𰸣�D��
������������ݡ��ȹ���ƽ���ִ�ԭ��ͼ���Կ�������Ӧʱ���¶�T2��T1�����¶�Խ�ߣ�HI����Խ�٣�˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ������÷�Ӧ������Ӧ���ڷ��ȷ�Ӧ����H��0��
�����Ѷȣ�һ��
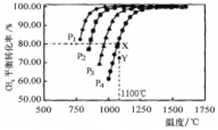
4��ѡ���� ���ܱ�������ͨ�����ʵ���Ũ�Ⱦ�0.1mol��L-1��CH4��CO2����һ�������·�����Ӧ�� �����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ�������й�˵��һ����ȷ����
�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ�������й�˵��һ����ȷ����
A��������Ӧ�ġ�H>0
B��ѹǿP1>P2>P3>P4
C��1100��÷�Ӧ��ƽ�ⳣ��Ϊ64mol2��L-1
D��ѹǿΪP4ʱ����Y�㣺v(��)<v(��)
�ο��𰸣�A
���������A����ͼ��֪���¶�����CH4��ƽ��ת���������¶�����ƽ�������ƶ����ʷ�ӦΪ���ȷ�Ӧ��H>0����ȷ��B���ɷ���ʽ��֪ѹǿ����ƽ��������У�CH4��ƽ��ת���ʼ�С����P4>P3>P2>P1������
C��? CO2 + CH4 2CO + 2H2
2CO + 2H2
ʼ��? 0.1? 0.1? 0? 0
ת����? 0.08? 0.08? 0.16? 0.16
ƽ����? 0.02? 0.02? 0.16? 0.16
ƽ�ⳣ��Ϊk=0.162��0.162�£�0.02��0.02��=1.6384
����
D���õ㴦�����ת���ʵͣ�ƽ��Ӧ�����ƶ���v(��)��v(��)������
�����Ѷȣ�һ��
5������� (14��)��ҵ���������Ҫ��Ӧ��4NH3(g)+5O2(g)  ?4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
?4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
(1)�����4molNH3��5molO2���������У��ﵽƽ��ʱ���ų�����0.8akJ����Ӧʱת�Ƶĵ�����Ϊ
?mol
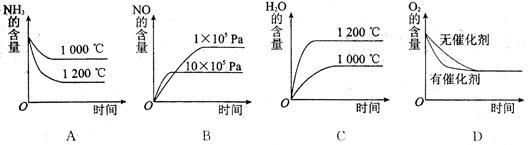
(2)�������������䣬���й�ϵͼ�д������?��ѡ����ţ�
(3)t��ʱ�����ݻ��̶����ܱ������з���������Ӧ�������ڸ����ʵ�Ũ�����±�
?Ũ��(mol/L)?
ʱ��(min)
| c(NH3)
| c(O2)
| c(NO)
| c(H2O)
|
��?ʼ
| 4.0
| 5.5
| 0
| 0
|
��2min
| 3.2
| x
| 0.8
| 1.2
|
��4min
| 2.0
| 3.0
| 2.0
| 3.0
|
��6min
| 2.0
| 3.0
| 2.0
| 3.0
|
?
�ٷ�Ӧ�ڵ�2mim����4mimʱ����Ӧ����v(O2)=?
�ڵ�2minʱ�ı����������ı������������?
A�������¶�? B��ʹ���˴���? C����Сѹǿ? D��������������
������ͬ���¶��£���ʼ�������м���NH3��O2��NO��H2O(g)��Ũ�ȶ�Ϊ1mol/L����÷�Ӧ����? _______�������(�����Ӧ��.���淴Ӧ��.�����ƶ���)
��4����ҵ����ˮ���ն��������������ᣬ���ɵ�NO2���徭��������������յ�ѭ������ʹ����ת��Ϊ���ᣨ�ٶ�������������������ʧ��������23��NO2����2���������յõ�20�G��ϡ����?�֡�
��5����Ʒ�����Ũ��Ϊ60%��70%��Ϊ����Ũ���ᣬ����Mg(NO3)2����ˮ����Ȼ�����������CaCl2��MgCl2����ˮ����ԭ����__________________________________________
�ο��𰸣�(ÿ��2�֣���14��)
(1)16
(2)AC
(3)��0.75mol.L-1.min-1?��AB?������Ӧ?
(4)140��
(5) ��ֹ�����ӷ���HCl����HNO3��.
���������
��1�����ݷ���ʽ��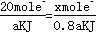 �����x=16��
�����x=16��
��2���¶����ߣ�ƽ�������ƶ��������ĺ������ӣ�ˮ�����������ͣ�AC����
��3����x=4.5��v(O2)= 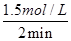 =0.75mol/(L��min)���ڵڶ���2min�ڣ���Ӧ��������䣬�����ʼӿ죬����Ϊ�����¶Ȼ����������۸���ƽ�ⳣ�����м��㣬���Եõ��������ƶ���
=0.75mol/(L��min)���ڵڶ���2min�ڣ���Ӧ��������䣬�����ʼӿ죬����Ϊ�����¶Ȼ����������۸���ƽ�ⳣ�����м��㣬���Եõ��������ƶ���
��4�������������չ�ϵΪ3NO2~2HNO3+NO~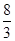 HNO3���ʵõ�20%������140t��
HNO3���ʵõ�20%������140t��
�����Ѷȣ�����