1、实验题 A~D是中学化学实验中常见的几种温度计装置示意图(图2-1-5)。
(1)请从①~⑧中选出必须使用温度计的实验,把编号填入最适宜的装置图A~C下的空格中(多选要倒扣分)。
①酒精和浓硫酸混合加热制乙烯
②电石跟水反应制乙炔
③分离苯和硝基苯的混合物
④苯跟溴的取代反应
⑤石油分馏实验
⑥浓盐酸和二氧化锰混合加热制氯气
⑦测定硝酸钾在水中的溶解度
⑧食盐和浓硫酸混合加热制氯化氢

(2)选用装置D做苯的硝化实验,D中长玻璃管的作用是:
参考答案:(1)A①;B③,⑤;C⑦。
(2)起冷凝回流作用(或答减少苯的挥发;或答起冷凝器的作用)。
本题解析:
【错解分析】常见错解分析:第(1)问:①在A下的空格中填入了②、③、④、⑥、⑦多个序号。②在B下的空格中只填入了序号⑤,漏填了序号③。③在C下的空格中填入了①、③、④、⑤、⑦、⑧多个序号。第(2)问:①导气;减压;排气作用;用手握住玻璃管上方,使试管底部不与烧杯底接触。②冷却;降温;冷凝剂。③冷凝回流硝酸。④冷凝回流溴苯。⑤冷凝,防回流。出现①误区,是由于不知道该反应装置,没做过(或没看见老师做过)苯的硝化实验,不懂得该实验的原理,导致失误。出现②误区,是由于不能正确表达冷凝器的作用所致。出现③误区,是由于没有抓住问题的实质,不了解长玻璃管的作用是回流苯,以减少苯的挥发。出现④误区,属于答非所问。出现⑤误区,属于自相矛盾。
【正解】第(1)问:以“必须使用温度计”为“筛子”,按A~C中学实验中常见的几种温度计装置示意图,对①~⑧实验进行分析,先确定必须使用温度计的实验是①、③、⑤、⑦,然后再逐一确定应填入A~C下哪个空格中。“①酒精和浓硫酸混合加热制乙烯”,属于液―液反应,反应需在170℃进行,温度计水银球应插在液面下。故“①”应填在A下的空格中。出现①误区是由于不知道哪些反应必须使用温度计,也不知道温度计水银球的位置,造成失误。“③分离苯和硝基苯的混合物”,液―液有机物可利用沸点不同,进行分馏以分离之,温度计水银球应位于蒸馏烧瓶侧管口处。故“③”应填在B下的空格中。“⑤石油分馏实验”,与“③”相同,也应填在B下的空格中。出现②误区,是由于不掌握液态有机物利用沸点不同分离的原理所致。“⑦测定硝酸钾在水中的溶解度”,温度计是用来测水温的,温度计插入试管中,水银球浸在液面下,且试管(连水带温度计)放在烧杯里进行水浴。故“⑦”应填在C下的空格中。出现③误区,是由于不清楚C装置的原理所致。
第(2)问:可直接从头脑中调出制取硝基苯的演示实验装置,回答长玻璃管的作用。也可以将酚醛树脂学生实验装置中,长玻璃管的作用迁移至此。回答是起冷凝回流作用(或答减少苯的挥发;或答起冷凝器的作用)。
本题难度:一般
2、选择题 下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是(?)
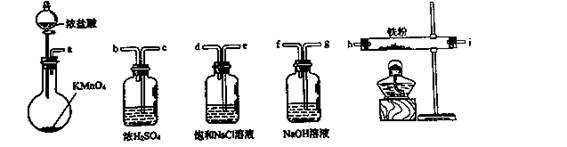
A.a-b-c-d-e-e-f-g-h
B.a-e-d-c-b-h-i-g
C.a-d-e-c-b-h-i-g
D.a-c-b-d-e-h-i-f
参考答案:B
本题解析:制备的氯气中含有氯化氢和水蒸气,用食盐水除去氯化氢,有水蒸气不能制得氯化铁,除去水蒸气用浓硫酸,应先除去水蒸气干燥氯气,干燥的氯气通入玻璃管中和铁反应生成无水氯化铁,最后吸收尾气中未反应的氯气,防止污染空气,洗气装置导气管长进短处,导气管口连接顺序为:a-e-d-c-b-h-i-g;
本题难度:一般
3、实验题 硫酸铜是一种应用广泛的化工原料,实验室中可通过不同途径制取硫酸铜溶液和胆矾(CuSO4・5H2O),其中一种流程如下:
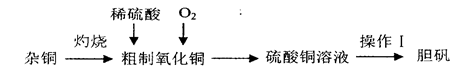
(1)操作I具体为__________、___________、过滤、烘干。
(2)杂铜(含少量有机物)灼烧后的产物除氧化铜还含少量铜,原因可能是___________(填字母代号)。
a.灼烧过程中部分氧化铜被还原
b.灼烧不充分.铜未被完全氧化
c.氧化铜在加热过程中分解生成铜
d.该条件下铜无法被氧气氧化
(3)若将杂铜换为纯净的铜粉,可直接向其中加入稀硫酸和Fe2(SO4)3溶液,不断通入氧气。反应完全后向其中加入过量_______________(填化学式,下同),调节pH至4,生成_________沉淀,过滤得硫酸铜溶液[已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4]。
(4)通过下述图1装置也可制取硫酸铜溶液(已知:2NaOH+2NO2=NaNO3+NaNO2+H2O)。

烧瓶内发生反应的离子方程式为____________________________________________;
图2是图1的改进装置,其优点有①__________________________,②_________________________。
参考答案:(16分)(1)蒸发浓缩(2分);冷却结晶(2分) (2)ab(2分,选对1个1分,有错误不得分)
(3)CuO(2分,其它合理答案也可) Fe(OH)3(2分)
(4)Cu+4H++2NO3-=Cu2++2H2O+2NO2↑;3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑(2分,写对1个即得2分) ①防止NaOH溶液倒吸进入发生装置(2分) ②NO、NO2有毒气体能被完全吸收(2分)
本题解析:(1)硫酸铜能溶于水,所以从硫酸铜溶液中得到硫酸铜晶体得操作应该是蒸发浓缩、冷却结晶,然后过滤烘干即可。
(2)灼烧后的产物除氧化铜还含少量铜,这说明a.灼烧过程中部分氧化铜被还原,a正确;b.灼烧不充分.铜未被完全氧化,b正确;c.氧化铜稳定,在加热过程中不可能分解生成铜,c不正确;d.铜极易被氧化生成氧化铜,d不正确,答案选ab。
(3)由于反应中不能再引入新的杂质,所以要调节溶液的pH小于进入氧化铜或氢氧化铜。由于氢氧化铁沉淀的pH小于氢氧化铜沉淀的pH,所以首先生成氢氧化铁沉淀,过滤得硫酸铜溶液。
(4)硝酸具有强氧化性,能把铜氧化生成硝酸铜,但随着反应的进行,硝酸浓度逐渐降低,其还原产物将逐渐变为NO,因此有关反应的化学方程式是Cu+4H++2NO3-=Cu2++2H2O+2NO2↑、3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。由于NO2与氢氧化钠溶液反应时,溶液容易倒吸,且NO与氢氧化钠溶液不反应,易造成环境污染,所以图2中通入氧气可以氧化NO而不完全吸收,即装置2的优点是①防止NaOH溶液倒吸进入发生装置;②NO、NO2有毒气体能被完全吸收。
本题难度:一般
4、选择题 制取硝酸铜的以下三种方案的叙述中,不正确的是
①2Cu+O2 2CuO,CuO+2HNO3="=" Cu(NO3)2 + H2O
2CuO,CuO+2HNO3="=" Cu(NO3)2 + H2O
②3Cu+8HNO3(稀) 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
③Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
A.三种方案中所涉及的反应都属于氧化还原反应
B.三种方案中硝酸的利用率:②>①>③
C.制取相同量的硝酸铜,②产生的有害气体比③多
D.三种方案中,①方案最优
参考答案:ABC
本题解析:略
本题难度:一般
5、实验题 (1)下图是一套实验室制气装置,用于发生、干燥和收集气体,下列各组物质中能利用这套装置进行实验的是?_?(填代号)。

①亚硫酸钠和硫酸②二氧化锰和浓盐酸③浓氨水和生石灰④石灰石和稀硫酸⑤锌和稀硫酸⑥硫化亚铁与稀硫酸⑦双氧水和二氧化锰
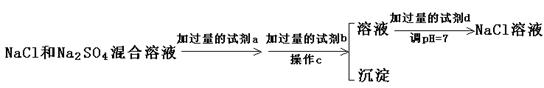
(2)有两瓶失去标签的物质的量浓度相同的碳酸钠溶液和碳酸氢钠溶液,请你加以鉴别:
①下列试剂中,可选用的一种试剂是_______(填代号)。?
A.氢氧化钠溶液
B.甲基橙溶液
C.稀盐酸
D.澄清石灰水
 ?。
?。