1、简答题 工业上“固定”和利用CO2能有效地减轻“温室效应”.
(1)目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝.已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
则反应2CO2(g)+4H2O(g)═2CH3OH(l)+3O2(g)△H=______kJ?mol-1
(2)T℃时,已知反应:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0.在T℃下,将2mol?CO2和2mol?H2充入1L的密闭容器中,测得H2的物质的量随时间的变化情况如图中曲线I所示.
①按曲线I计算反应从0到4min时,υ(H2)=______.
②在T℃时,若仅改变某一外界条件时,测得H2的物质的量随时间的变化情况如图中曲线Ⅱ所示,则改变的外界条件为______.计算该反应按曲线II进行,达到平衡时,容器中c(CO2)=______.
(3)已知25℃时,乙酸和碳酸的电离平衡常数如下表:
| 物质的化学式 | CH3COOH | H2CO3
电离平衡常数
K=1.8×10-5
?K1=4.3×10-7
?K2=5.6×10-11
|
①用饱和氨水吸收CO2可得到NH4HCO3溶液.若已知CH3COONH4溶液pH=7,则?NH4HCO3溶液显______(填“酸性”、“碱性”或“中性”).
②在25℃时,在乙酸溶液中加入一定量的NaHCO3,保持温度不变,所得混合液的pH=6,那么混合液中=______.
③向0.1mol?L?-1CH3COOH溶液中加入少量CH3COONa晶体,保持温度不变,下列有关说法正确的是______(填代号).
a.溶液的pH增大?b.CH3COOH的电离程度增大
c.溶液的导电能力减弱? d.溶液中c(OH-)?c(H+)不变.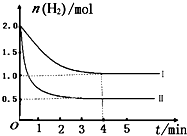
参考答案:(1)已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
根据目标方程式,改写方程式①和②,把方程式①反写乘以2,再把方程②反写,然后二者相加,即得到目标方程,所以△H=-△H1×2-△H2=+1275.68kJ/mol,
故答案为:+1275.68;
(2)①△n=2.0-1.0=1.0mol△c=△nV=1mol/L? v=△ct=1mol/L4=0.25mol/(L?min),故答案为:0.25mol/(L?min);
②根据到达平衡的时间减少,氢气也减少,平衡正移,说明增大二氧化碳的浓度,故答案为:增大二氧化碳的浓度;
(3)①根据盐类水解规律,已知CH3COONH4溶液pH=7,又因为H2CO3酸性比CH3COOH弱,水解程度更大,所以 NH4HCO3显碱性,故答案为:碱性;
②根据PH可知c(H+)=10-6mol/L和醋酸的电离常数Ka=c(CH3COO-)?c(H+)c(CH3COOH)=1.8×10-5计算出中c(CH3COO-)c(CH3COOH)=18,故答案为:18;
③根据影响电离平衡的因素:CH3COOH?CH3COO-+H+,加入少量CH3COONa晶体,
a、平衡逆移,氢离子浓度减小PH增大,故a正确;
b、平衡逆移,CH3COOH的电离程度减小,故b错误;
c、CH3COONa晶体为强电解质,溶液中带电离子浓度增大,导电能力增强,故c错误;
d、由于温度没变,所以溶液中c(OH-)?c(H+)不变,故d正确.
故答案为:ad.
本题解析:
本题难度:一般
2、选择题 已知:Fe2O3(s)+3/2C(s)= 3/2CO2(g)+2Fe(s) △H =+234.1kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1 则2Fe(s)+3/2O2(g)=Fe2O3(s)的△H是
[? ]
A.-824.4kJ·mol-1
B.-627.6kJ·mol-1
C.-744.7kJ·mol-1
D.-169.4kJ·mol-1
参考答案:A
本题解析:
本题难度:一般
3、填空题 丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) == 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) ==C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) == 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2 (g) == 2H2O(l) ΔH=-d kJ·mol-1 (a、b、c、d均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 ______(填“大于”、“等于”或“小于”)途径II放出的热量。
(2)由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量,那么在化学反应时。反应物就需要______(填“放出”、或“吸收”)能量才能转化为生成物,因此其反应条件是______________。
(3)b 与a、c、d的数学关系式是______________。
参考答案:(1)等于
(2)小于;吸收;加热
(3)b=c/2+d/2-a
本题解析:
本题难度:一般
4、填空题 常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为kJ/mol)下表是一些键能数据(kJ·mol-1)
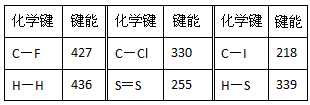
回答下列问题:
(1)由表中数据规律预测C-Br键的键能范围:_________<C-Br键能<_________
(2)热化学方程式2H2(g)+S2(g) ==2H2S(g) △H= QkJ·mol-1;则Q=___________
(3)已知下列热化学方程式:
O2(g) == O2+(g) +e- △H1= +1175.7 kJ·mol-1
PtF6(g) + e-== PtF6-(g) △H2= -771.1 kJ·mol-1
O2+PtF6-(s) == O2+(g) + PtF6-(g) △H3= +482.2 kJ·mol-1
则反应O2(g) +_________(g) = O2+PtF6-(s)的△H=_____________ kJ·mol-1。
参考答案:(1)218kJ·mol-1;330kJ·mol-1
(2)-229
(3)PtF6;-77.6
本题解析:
本题难度:一般
5、选择题 一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:
①CH4?(?g?)+4NO2(?g?)═4NO(?g?)+CO2(?g?)+2H2O(?g?)△H=-574kJ?mol-1
②CH4?(?g?)+4NO(?g?)═2N2(?g?)+CO2(?g?)+2H2O(?g?)△H=-1160kJ?mol-1.
下列正确的选项是( ? )
A.CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(l)△H=-867kJ?mol-1
B.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子总数为3.2mol
C.若0.2molCH4还原NO2至N2,在上述条件下放出的热量为173.4kJ
D.若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为3.2mol
参考答案:C
本题解析:
本题难度:一般