1、选择题 小明体检的血液体验单中,葡萄糖为5.9×10-3mol/L,表示该体检指标的物理量是(?)
A.溶解度(S)
B.物质的量浓度(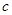 )
)
C.质量分数(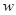 )
)
D.摩尔质量(M)
参考答案:B
本题解析:从表示葡萄糖数据的单位可确定为物质的量浓度。
本题难度:简单
2、选择题 下列叙述正确的是(?)
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质的体积都约为22.4L
参考答案:C
本题解析:质量的单位是g,摩尔质量的单位是g/mol,所以选项A、B都是不正确的;3.01×1023个SO2分子是0.5mol,质量是0.5mol×64g/mol=32g,选项C正确;标准状况下,1 mol任何气体的体积都约为22.4L,选项D不正确,答案选C。
本题难度:一般
3、选择题 取质量为44g的Zn、Fe、Al三种金属构成的混合物粉末,与一定质量的20%硫酸溶液恰好完全反应,得到无水盐140g,则生成气体的体积(标准状况下)为
A.11.2L
B.22.4L
C.33.6L
D.44.8L
参考答案:B
本题解析:蒸发后的固体为混合物,反应前的固体是三种金属的质量为44g,所以140g-44g=96g为硫酸根的质量,在硫酸中,氢元素与硫酸根的质量比为(1×2):96,则硫酸中含氢的质量为2g,所以产生的氢气的物质的量为1mol,其标准状况下体积为22.4L,故选B。
点评:本题考查质量守恒定律的灵活运用和解答问题的能力
本题难度:一般
4、选择题 实验室欲配制100 mL、1mol/L的NaCl溶液,请回答:
(1)不需要使用的仪器是?。
A、烧杯B、500 mL容量瓶C、量筒? D、胶头滴管? E、玻璃棒 ?F、100 mL容量瓶
(2)配制时用托盘天平应称取NaCl?g。
(3)配制溶液的操作顺序是(用字母表示) ?。
A、称量? B、洗涤? C、定容? D、溶解? E、摇匀? F、转移
参考答案:(1)B?(2) 5.9?(3)A D F B C E
本题解析:(1)准确配制100ml、一定浓度的溶液需要烧杯、量筒、玻璃棒、100ml的容量瓶、胶头滴管,不需要500 mL容量瓶,选项为:B.(2)n(NaCl)=C・V=1mol/L×0.1L=0.1mol.m(NaCl)=n・M=0.1mol×58.5g/mol=5.85g.由于天平的准确度为0.1.四舍五入,需要称量的氯化钠的质量为5.9g.(3)准确配制一定体积、一定浓度的溶液的步骤为:计算、称量、溶解、转移溶液、洗涤、定容、摇匀。所以操作顺序是A D F B C E。
本题难度:一般
5、填空题 试回答下列问题:
(1) 标准状况下11.2L NH3中含____个氨分子,??mol氢原子;
(2) 等质量的SO2和SO3所含的原子个数之比是??,物质的量之比是??;
(3)6.8gNH3中所含氢原子数与??g水所含氢原子数相等;
参考答案:(1)0.5NA? 1.5?(2)15:16? 5:4?(3)10.8
本题解析:(1)标准状况下11.2L NH3的物质的量是11.2L÷22.4L/mol=0.5mol,则根据氨气的分子式可知分子中含0.5NA个氨分子,1.5mol氢原子。
(2)等质量的SO2和SO3物质的量之比是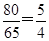 ,所以根据分子式可知所含的原子个数之比是
,所以根据分子式可知所含的原子个数之比是 。
。
(3)6.8gNH3中所含氢原子的物质的量是 ,所以相应水的物质的量是0.6mol,质量是0.6mol×18g/mol=10.8g。
,所以相应水的物质的量是0.6mol,质量是0.6mol×18g/mol=10.8g。
点评:在进行物质的量的有关计算时,关键是熟练应用几个关系式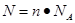 、n=m/M、
、n=m/M、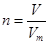 、
、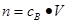 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
本题难度:一般