1、选择题 下列叙述正确的是(?)
A.金属元素的原子只有还原性,离子只有氧化性
B.用乙烷(CH3CH3)或乙烯(CH2=CH2)制一氯乙烷(CH3CH2Cl)的反应类型相同
C.煤油是通过煤干馏获得,可用作燃料和保存少量金属钠
D.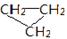 和CH3-CH=CH2互称为同分异构体
和CH3-CH=CH2互称为同分异构体
参考答案:D
本题解析:A、金属元素的原子只有还原性,但离子不只有氧化性,如亚铁离子也具有还原性,错误;B、乙烷制一氯乙烷是取代反应,乙烯制一氯乙烷是加成反应,错误;C、煤油是通过石油分馏制得,错误;D、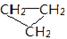 和CH3-CH=CH2分子式相同,但结构不同,属于同分异构体,正确,答案选D。
和CH3-CH=CH2分子式相同,但结构不同,属于同分异构体,正确,答案选D。
本题难度:一般
2、选择题 在反应3Cl2+8 NH3 ?= N2+6NH4Cl中,氧化剂与还原剂的物质的量之比为(? )
A.8:3
B.3:8
C.3:2
D.1:3
参考答案:C
本题解析:在反应3Cl2+8 NH3 ?= N2+6NH4Cl中:氯元素由反应前Cl2的0价变为反应后NH4Cl的-1价,化合价降低,得到电子,作氧化剂;氮元素由反应前NH3中的-3价变为反应后N2中的0价,化合价升高,失去电子作还原剂。在参加反应的8个NH3中有2个被氧化,起还原剂的作用。故氧化剂与还原剂的物质的量之比为3:2。选项为C。
本题难度:一般
3、填空题 除去下列物质中所含杂质(括号内为杂质),写出除去杂质的化学方程式.
(1)Fe2O3[Fe(OH)3]______;(2)Fe(Al)______.
参考答案:(1)因Fe(OH)3加热分解得到Fe2O3和H2O,可除去Fe(OH)3,故答案为:2Fe(OH)3?△?.?Fe2O3+3H2O;
(2)因铝可以与碱反应,而Fe不与碱反应,通过过滤得到铁,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
本题解析:
本题难度:一般
4、选择题 化学概念是对化学现象与事实的总结和概括。下列说法中正确的是
A.分散系只包括溶液和胶体
B.使空气中游离态的氮转化为含氮化合物叫做氮的固定,氨的合成即为固氮。
C.单位物质的量的物质所具有的质量叫摩尔质量,摩尔质量与1 mol物质的质量完全相同
D.物质失电子的反应为还原反应
参考答案:B
本题解析:A分散系也包括悬浊液和乳浊液
B?由单质变为化合态都叫做氮的固定
C?摩尔质量与1 mol物质的质量,数值上相同,单位不同
D 得电子的反应为还原反应
本题难度:简单
5、填空题 (5分)氯酸钾与浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,反应的化学方程式为:2KClO3 + 4HCl(浓) === 2KCl + 2ClO2↑+ Cl2↑+ 2H2O
(1)用双线桥表示上述反应中电子转移的方向和数目。
(2)浓盐酸在该反应中表现的性质是________(填序号)。
① 只有还原性 ② 还原性和酸性 ③ 只有氧化性 ④ 氧化性和酸性
(3)上述反应产生0.2 mol Cl2时,转移的电子数约为______________。
参考答案:(5分)
(1) (2分,若写成2e-也得分)
(2分,若写成2e-也得分)
(2)② (2分)
(3)2.408×1023 (1分)
本题解析:(2)浓盐酸在反应中部分氯失电子生成氯气,表现还原性,部分转变为氯化钾,表现酸性
(3)由(1)可知,当产生0.2 mol Cl2时,反应有0.4 mol e―转移,
本题难度:一般